Clear Sky Science · tr
SfTRÜktürel analizler, sülfat azaltan bakterilerde proteaz-adezin etkileşimlerini ve c-di-GMP reseptör regülasyonunu ortaya koyuyor
Neden yapışkan bakteriler önemli?
Bakteriler sıklıkla tek hücreler halinde değil, biyofilmler adı verilen sıkışık, sümüksü topluluklar halinde yaşar. Bu topluluklar boruları, gemi gövdelerini, yeraltı kayalarını ve hatta tıbbi cihazları kaplayabilir. Desulfovibrio vulgaris gibi sülfat‑azaltan bakterilerde biyofilm hem avantaj hem dezavantajtır: kirli çevreleri temizlemeye yardım ederler, ancak metallerin korozyonunu da hızlandırırlar. Bu çalışma, görmesi basit ama etkileri büyük bir soruyu gündeme getiriyor: bu bakteriler bir yüzeye ne zaman sıkıca tutunacaklarına, ne zaman ayrılacaklarına nasıl karar veriyor?
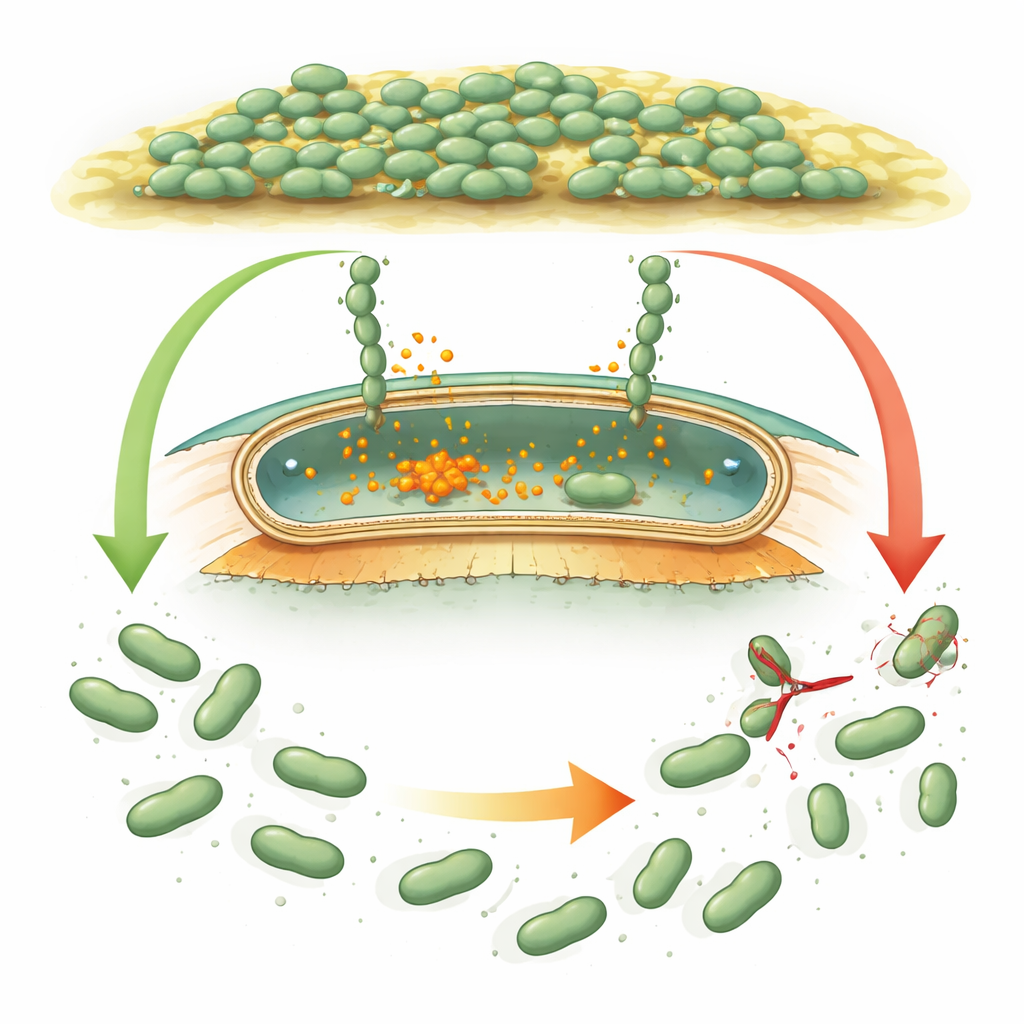
Mikroplar nasıl tutunur ve serbest bırakır
Birçok bakteri, hücreleri yüzeylere ve birbirine yapıştıran devasa “cırt cırt benzeri” proteinler olan adezinleri kullanır. Pseudomonas gibi iyi incelenmiş türlerde bu adezinler, bakterilerin biyofilm oluşturması gerektiğinde yükselen ve dağılması gerektiğinde düşen içsel bir kimyasal sinyal olan siklik di‑GMP ile kontrol edilir. Sinyal yüksek olduğunda adezinler hücrenin dış katmanına bağlı kalır. Düşünce, küçük bir protein kesici (proteaz) adezinin hücre yüzeyine yakın kısmını keser ve yapışkan bölüm serbest kalarak hücrelerin ayrılmasına yardımcı olur. Desulfovibrio vulgaris benzer genetik araçlara sahip görünse de, düzenleyici proteinleri dizilim ve biçim açısından o kadar farklıdır ki bilim insanları aynı mantığı mı yoksa tamamen yeni bir stratejiyi mi kullandığını ayırt edememişti.
Özelleşmiş moleküler makas
Yazarlar önce adezinleri kesen proteazın Desulfovibrio versiyonu olan DvhG'ye odaklandı. Yapı tahmini ve biyokimyasal testler kullanarak DvhG'nin diğer bakterilerdeki karşılıklarıyla aynı çekirdek katlanışa ve katalitik mekanizmaya sahip olduğunu ve çalışması için kalsiyuma ihtiyaç duyduğunu gösterdiler. DvhG, Desulfovibrio'nun biyofilm oluşumu için ihtiyaç duyduğu iki büyük adezini, bu proteinleri dış zar içinde tutan küçük bir “tutma” segmentinin hemen sonrasında neredeyse aynı noktalardan hassas şekilde keser. İlginç bir şekilde ekip, DvhG'nin sadece kısa bir hedef dizisini tanımaktan daha fazlasını yaptığını buldu. Her adezinin hacimli tutma bölgesi proteazla geniş temas yüzeyi oluşturuyor ve bu büyük rıhtım yüzeyi kesme verimliliğini artırıyor. Bu rıhtım yamayı bozan mutasyonlar DvhG'yi çok daha az etkili kılıyor; bu da benzer sistemlere kıyasla ek bir özgüllük katmanı olduğunu ortaya koyuyor.
Hücre içinde sinyal algılayan bir anahtar
İkinci kilit oyuncu olan DvhD, iç zar üzerinde yer alır ve hem hücre içi hem zarlar arasındaki boşluğa uzanır. Araştırmacılar DvhD parçalarının birden çok üç boyutlu yapısını çözdü. Hücre dışında, periplazmik bölgesi küçük molekülleri bağlayan yaygın bir sensör mimarisi olan dCache domaini oluşturur. Hücre içinde ise DvhD, genellikle siklik di‑GMP'yi parçalayan enzimlerde bulunan bir modül olan HD‑GYP domainini taşır. Ancak burada kritik metal bağlayıcı kalıntılar eksiktir ve dikkatli testler DvhD'nin sinyali yok etmediğini; bunun yerine siklik di‑GMP'yi çok sıkı şekilde bağladığını gösterdi. Yapı anlık görüntüleri, iki farklı bağlanma cepleri ortaya koydu; burada en fazla üç siklik di‑GMP molekülü bir çift HD‑GYP domainini köprüleyerek onları yeni bir dizilime zorlayabilir ve reseptörün geri kalanına bağlanan uzun heliksleri ayırabilir.
İçsel sinyalden yüzey davranışına
DvhD'nin “boş” ve sinyal bağlı formlarını karşılaştırarak ekip, siklik di‑GMP bağlanmasının reseptör dimerini nasıl yeniden şekillendirebileceğini ortaya koydu. Bu değişikliklerin iç zardan geçerek periplazmik dCache domaininin yeniden konumlanmasına yol açması ve bunun da DvhG ile etkileşime girmesi bekleniyor. Modellemede, DvhD DvhG'ye bağlandığında proteazın adezinlere erişimini engellediği ve hatta kalsiyum bağlama sitesini bozarak makası “kapalı” konuma getirebileceği öne sürülüyor. Siklik di‑GMP seviyeleri düştüğünde reseptörün şekli gevşer, DvhG serbest kalır; böylece adezinlerin tutma domainlerine tutunup onları kesebilir ve adezinlerin dış kısımları—dolayısıyla biyofilm matriksi—hücre yüzeyinden kayarak uzaklaşabilir. Bu yolla Desulfovibrio, içinde bulunduğu koşulların kimyasal bir iç okumasını mekanik bir karara çevirir: bağlı kalmak mı yoksa dağılmak mı.
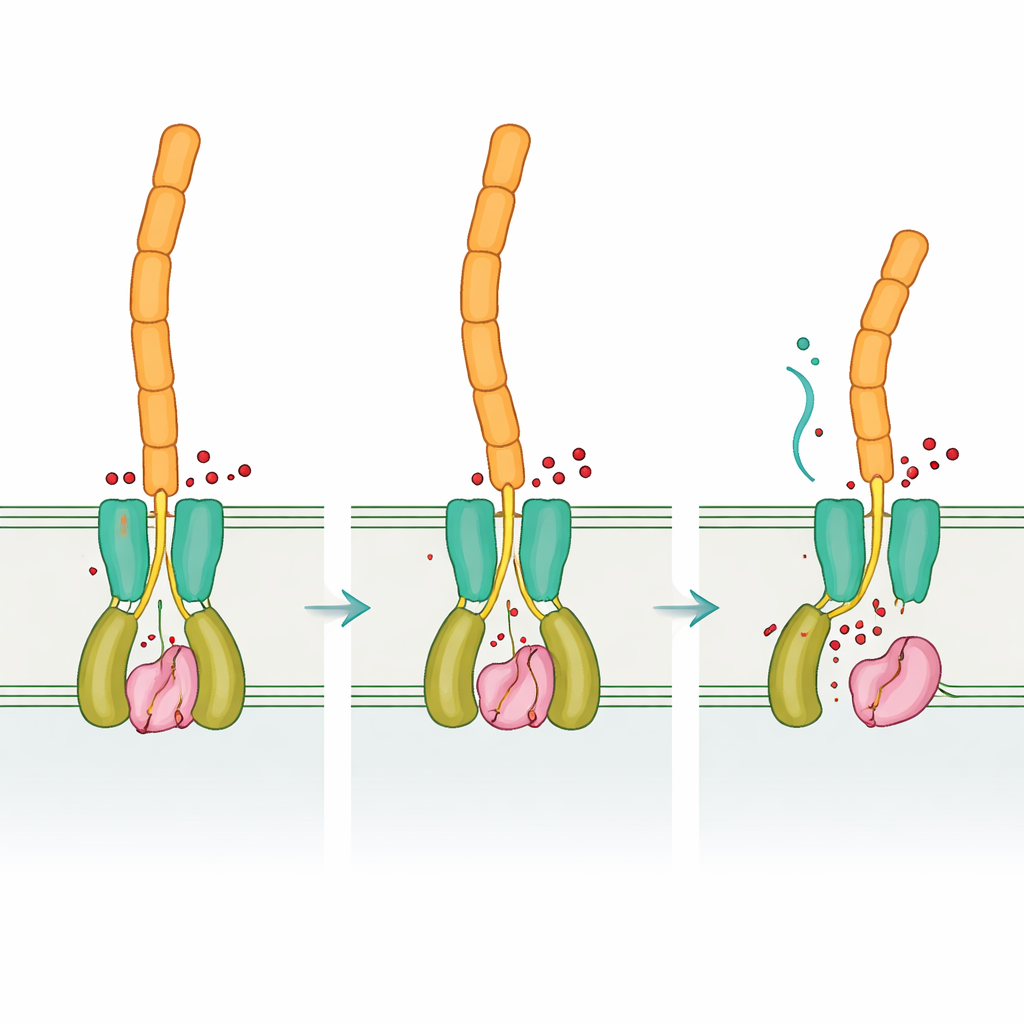
Aynı mantık, farklı donanım
Bir arada değerlendirildiğinde sonuçlar, Desulfovibrio vulgaris'in genel düzenleyici mantığı daha tanıdık bakterilerle aynı şekilde kullandığını gösteriyor—siklik di‑GMP bir reseptörü kontrol eder, bu da bir proteazı kısıtlar veya serbest bırakır ve proteaz yüzey adezinlerini keser—ancak bunu çok farklı bir protein “parça” setiyle uygular. Korunma ve yeniden icat karışımı, evrimin başarılı sinyal fikirlerini yeniden kullanırken bu işlevleri yürüten molekülleri nasıl yeniden şekillendirebileceğini gösterir. Bu esnek tasarımın anlaşılması, biyofilmlerin birçok bakteri grubunda nasıl oluşup parçalandığına dair anlayışımızı derinleştirmekle kalmaz; aynı zamanda biyoremediasyonda yararlı biyofilmleri teşvik etmek veya metal korozyonuna ve kronik enfeksiyonlara yol açan zararlı biyofilmleri bozmak için daha akıllı stratejilere işaret edebilir.
Atıf: Font, M.E., Karbelkar, A.A., Lormand, J.D. et al. Structural analyses uncover protease-adhesin interactions and c-di-GMP receptor regulation in sulfate-reducing bacteria. Nat Commun 17, 3564 (2026). https://doi.org/10.1038/s41467-026-71936-5
Anahtar kelimeler: bakteriyel biyofilmler, Desulfovibrio vulgaris, siklik di-GMP sinyalleşmesi, adezin proteazı, sülfat azaltan bakteriler