Clear Sky Science · sv
Strukturanalyser avslöjar proteas‑adhesin‑interaktioner och c‑di‑GMP‑receptorreglering hos sulfat‑reducerande bakterier
Varför klibbiga bakterier spelar roll
Bakterier lever ofta inte som ensamma celler utan som trånga, slemmiga samhällen kallade biofilmer. Dessa samhällen kan täcka rör, fartygsskrov, underjordiska berg och till och med medicintekniska implantat. Hos sulfat‑reducerande bakterier som Desulfovibrio vulgaris är biofilmer ett tveeggat svärd: de hjälper till att rengöra förorenade miljöer men påskyndar också korrosion av metaller. Denna studie ställer en enkel fråga med stora följder: hur bestämmer sig dessa bakterier för när de ska fästa hårt vid en yta och när de ska släppa taget?
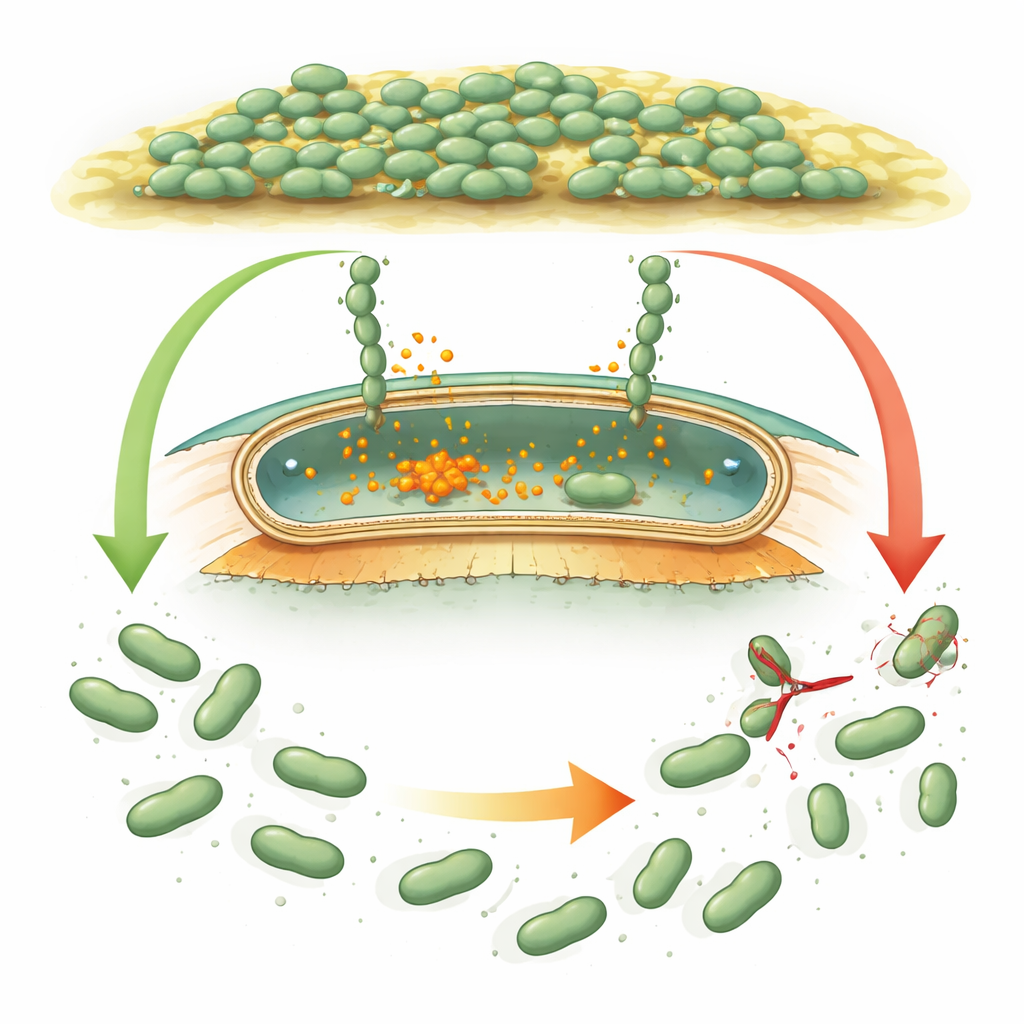
Hur mikrober greppar och släpper
Många bakterier använder jätte‑"Velcro‑liknande" proteiner, kallade adhesiner, som får celler att fästa vid ytor och vid varandra. I välstuderade arter som Pseudomonas regleras dessa adhesiner av en intern kemisk signal, cyklisk di‑GMP, som ökar när bakterier bör bilda biofilm och sjunker när de bör sprida sig. När signalen är hög sitter adhesinerna kvar förankrade i cellens yttre skal. När den sjunker skär en liten proteinkutter (en proteas) av adhesinet nära cellytan, och den klibbiga delen driver iväg, vilket hjälper cellerna att lossa. Desulfovibrio vulgaris bär vad som ser ut att vara ett liknande genetiskt verktyg, men dess regulatoriska proteiner skiljer sig så mycket i sekvens och form att forskarna inte kunde avgöra om den använder samma logik eller en helt ny strategi.
En specialiserad molekylär sax
Författarna fokuserade först på DvhG, Desulfovibrio‑varianten av adhesin‑klippande proteasen. Genom strukturprognoser och biokemiska tester visade de att DvhG har samma grundläggande veckning och katalytiska maskineri som motsvarigheter i andra bakterier och kräver kalcium för att fungera. Den klipper precist två stora adhesiner som Desulfovibrio behöver för biofilmsbildning, på nästan identiska positioner strax efter en liten "retentions"‑sekvens som håller dessa proteiner fastsatta i det yttre membranet. Intressant nog fann teamet att DvhG gör mer än att bara känna igen en kort målsekvens. Den skrymmande retentionsdomänen hos varje adhesin gör omfattande kontakter med proteasen och bildar en stor dockningsyta som ökar klippeffektiviteten. Mutationer som stör denna dockningsyta gör DvhG mycket mindre effektiv, vilket avslöjar ett extra lager av specificitet jämfört med närbesläktade system.
En signalsensor‑brytare inne i cellen
Den andra huvudspelaren, DvhD, sitter i det inre membranet och sträcker sig in i både cellens inre och utrymmet mellan membranen. Forskarna bestämde flera tredimensionella strukturer av DvhD‑fragment. Utanför cellen bildar dess periplasmiska region en dCache‑domän, en vanlig sensorarkitektur som ofta binder små molekyler. Inuti cellen bär DvhD en HD‑GYP‑domän, en modul som vanligtvis finns i enzymer som bryter ner cyklisk di‑GMP. Här saknas dock de avgörande metallbindande resterna, och noggranna analyser visade att DvhD inte förstör signalen; istället binder den cyklisk di‑GMP mycket starkt. Strukturella ögonblicksbilder visade två distinkta bindningsfickor där upp till tre cykliska di‑GMP‑molekyler kan binda ihop ett par HD‑GYP‑domäner och tvinga dem in i en ny arrangemangsform, vilket prånglar isär långa helixar som kopplar till resten av receptorn.
Från intern signal till ytbeteende
Genom att jämföra den "tomma" och signalbundna formen av DvhD avslöjade teamet hur bindning av cyklisk di‑GMP kan omforma receptor‑dimetern. Dessa förändringar förväntas färdas genom det inre membranet och ompositionera den periplasmiska dCache‑domänen, som i sin tur interagerar med DvhG. Modellering antyder att när DvhD engagerar DvhG blockerar den proteasens åtkomst till adhesiner och kan till och med snedvrida dess kalciumbindande plats, vilket slår "av" saxen. När nivåerna av cyklisk di‑GMP sjunker slappnar receptorens form av, släpper DvhG så att den kan greppa adhesinernas retentionsdomäner och klippa dem, vilket tillåter adhesinernas yttre delar — och därmed biofilmsmatrisen — att glida bort från cellytan. På så sätt översätter Desulfovibrio en intern kemisk avläsning av omständigheterna till ett mekaniskt beslut: sitta kvar eller sprida sig.
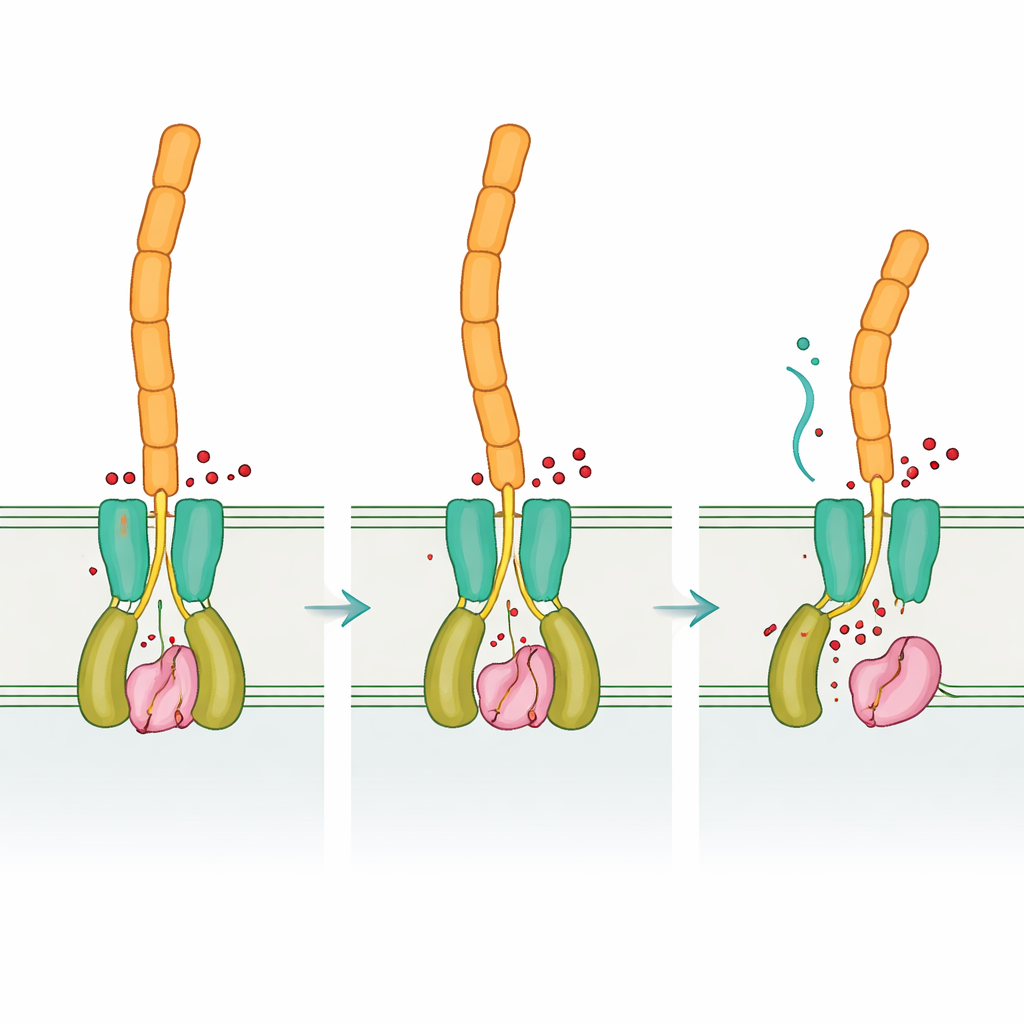
Samma logik, annan hårdvara
Tillsammans visar resultaten att Desulfovibrio vulgaris använder samma övergripande regulatoriska logik som mer välkända bakterier — cyklisk di‑GMP kontrollerar en receptor som i sin tur håller tillbaka eller släpper en proteas som klipper ytfästande adhesiner — men implementerar den med en mycket annorlunda uppsättning protein"delar." Denna blandning av bevarande och nyskapande illustrerar hur evolutionen kan återanvända framgångsrika signalidéer samtidigt som den omformar molekylerna som utför dem. Att förstå denna flexibla design fördjupar inte bara vår förståelse av hur biofilmer bildas och bryts upp hos många bakteriegrupper, utan kan också peka mot smartare strategier för att antingen främja hjälpsamma biofilmer vid bioremediering eller störa skadliga sådana som orsakar metallkorrosion och kroniska infektioner.
Citering: Font, M.E., Karbelkar, A.A., Lormand, J.D. et al. Structural analyses uncover protease-adhesin interactions and c-di-GMP receptor regulation in sulfate-reducing bacteria. Nat Commun 17, 3564 (2026). https://doi.org/10.1038/s41467-026-71936-5
Nyckelord: bakteriella biofilmer, Desulfovibrio vulgaris, cyklisk di‑GMP‑signalering, adhesin‑proteas, sulfat‑reducerande bakterier