Clear Sky Science · zh
由鞘氨醇‑1‑磷酸衍生的2‑十六烯醛通过抑制鞘氨醇‑1‑磷酸受体5成为眼部新生血管形成的关键介质
这项研究为何与视力相关
像糖尿病性眼病这样的疾病导致的视力丧失,常常源于视网膜后部生长出脆弱且渗漏的血管。现有治疗可以挽救视力,但费用高昂、具有侵入性,并非对所有人都有效。本研究揭示了一个此前未被注意到的化学元凶及免疫细胞上的一个新靶点分子,这两者共同推动了有害的血管生长,为未来开发更安全、口服类药物的可能途径打开了希望。
由有益脂质生成的隐秘祸根
故事始于一种类脂质信使——鞘氨醇‑1‑磷酸(S1P)。S1P通常有助于维持血管稳定并防止渗漏,作用于其受体的药物已用于多发性硬化等疾病。但当S1P被降解时,会形成一种反应性副产物2‑十六烯醛,一种小而不稳定的醛类分子。直到现在,几乎没人知道这种副产物在活体血管,尤其在眼内,会产生何种影响。作者怀疑,如果2‑十六烯醛不能被妥善清除,可能会损伤细胞并扰乱为感光视网膜提供营养的精细血管网络。
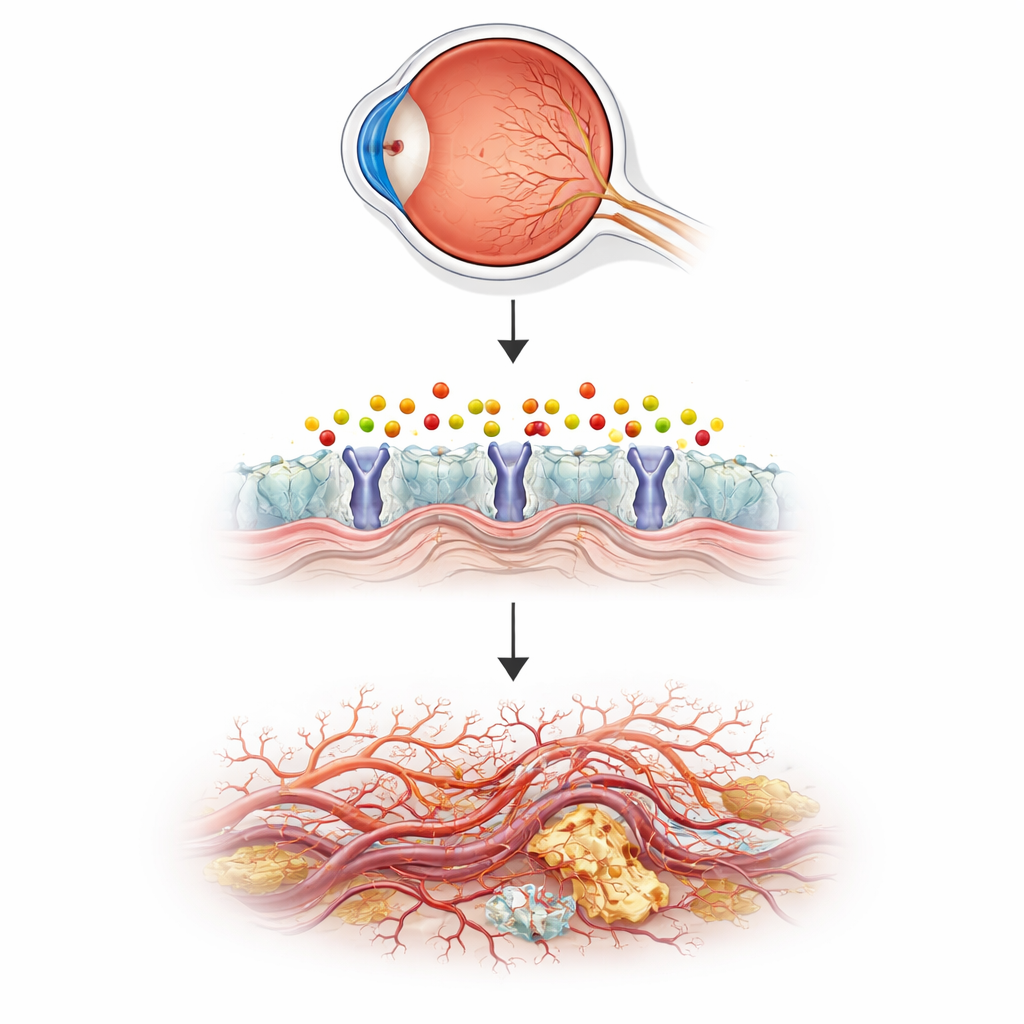
用小鱼模拟病变人眼
为检验这一假设,研究团队选择了斑马鱼,这种小型观赏鱼的透明胚胎让科学家可以直接观察血管形成过程。他们敲除了名为 aldh3b1 的基因,该基因编码一种能解毒2‑十六烯醛的酶,并追踪眼内血管的生长。缺失该酶的鱼在视网膜中出现过度的细小新生枝条和分支,模式类似于人类疾病的早期表现,而体内较大的血管保持正常。当正常鱼仅被浸泡在2‑十六烯醛中时,其眼部血管也以相同方式过度生长。一种能吸收反应性醛类的天然分子——肉碱(carnosine)逆转了这些改变,直接将异常生长与这一单一脂质衍生化合物的积累联系起来。
铁稳态失衡与一种灼热般的细胞死亡形式
研究者接着探究这种小分子如何强力重塑血管。他们结合基因活性谱分析与详尽的化学检测,发现过量的2‑十六烯醛扰乱了细胞处理铁的方式,并将细胞推向铁死亡(ferroptosis)——一种近年被认识到的以铁驱动并伴随脂质过氧化失控的细胞死亡形式。在鱼眼中,脂质损伤和铁超载的标志物升高,而通常阻止铁死亡的关键保护系统(包括FSP1蛋白和抗氧化酶GPX4)被下调。用专门的抑制剂阻断铁死亡可以缓解异常血管生长,而直接阻断FSP1会复制出疾病样改变,这表明该通路位于损伤的核心。
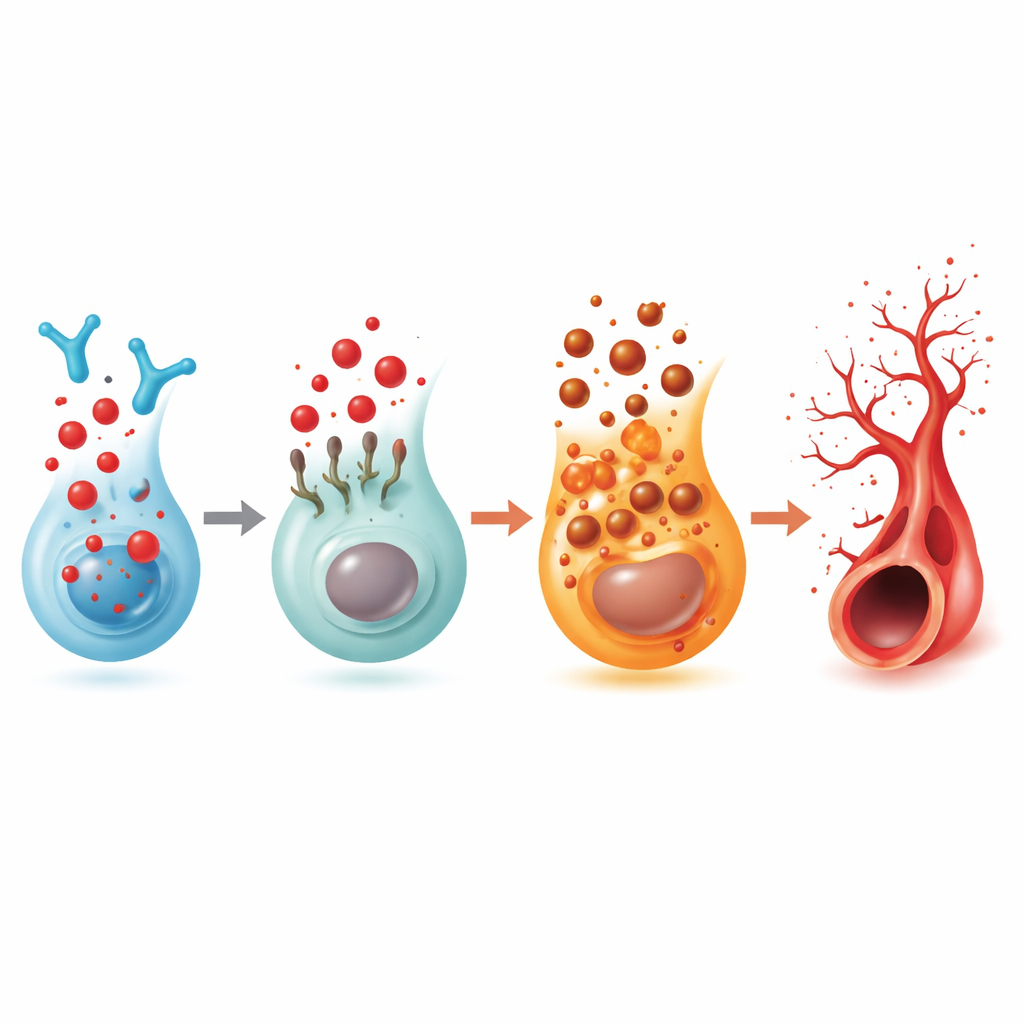
一个将脂质信号、免疫细胞与血管联系起来的受体转换
由于2‑十六烯醛由S1P衍生,团队检查了S1P的五种已知受体。只有一种受体——称为S1PR5——在2‑十六烯醛积累时在鱼眼中持续下调。单独下调S1PR5就会导致相同的过度萌发,并同时降低FSP1,将该受体与抑制铁死亡的机制联系起来。一种选择性激活S1PR5的药物在2‑十六烯醛处理和酶缺陷的鱼中都能恢复较为正常的血管模式。生物物理和计算建模工作显示,2‑十六烯醛可以直接与S1PR5结合并触发其内吞,使其细胞表面信号减弱。在人类单细胞视网膜数据中,S1PR5主要存在于自然杀伤(NK)免疫细胞上;在晚期糖尿病性眼病患者的样本中,S1PR5水平显著升高,同时与鞘磷脂、免疫信号和铁死亡相关的通路发生改变,这些改变与斑马鱼的发现相符。
这对糖尿病性眼病患者意味着什么
总体而言,研究勾勒出一个简单而有力的图景:当酶ALDH3B1无法清除由S1P衍生的醛类2‑十六烯醛时,这一反应性副产物扰乱免疫细胞上的S1PR5信号,削弱细胞针对铁驱动损伤的内在防御系统,并促发一种类似“生锈”的细胞死亡,从而助长纠结且脆弱的血管侵入视网膜。鉴于已有针对S1PR的药物且部分可口服,这一新描绘的2‑十六烯醛–S1PR5–铁死亡轴提供了一条切实可行的途径,未来或可开发出减少眼内注射频率、延缓或预防糖尿病性视网膜病变视力丧失的治疗策略。
引用: Qian, X., Ge, R., Chu, Y. et al. Sphingosine-1-Phosphate-derived 2-Hexadecenal is a central mediator of ocular neovascularization by inhibiting Sphingosine-1-Phosphate receptor 5. Nat Commun 17, 3488 (2026). https://doi.org/10.1038/s41467-026-71792-3
关键词: 糖尿病性视网膜病变, 视网膜血管, 脂质信号传导, 铁死亡, 鞘氨醇‑1‑磷酸受体