Clear Sky Science · de
Vom Sphingosin-1‑phosphat abgeleitetes 2‑Hexadecenal ist ein zentraler Vermittler der okulären Neovaskularisation durch Hemmung des Sphingosin-1‑Phosphat-Rezeptors 5
Warum diese Studie für das Sehvermögen wichtig ist
Sehverlust durch Erkrankungen wie die diabetische Netzhauterkrankung entsteht häufig durch das Wachstum fragiler, undichter Blutgefäße in der Netzhaut im hinteren Bereich des Auges. Bestehende Therapien können das Sehen retten, sind aber teuer, invasiv und wirken nicht bei allen Betroffenen. Diese Studie deckt einen zuvor verborgenen chemischen Verursacher und ein neues Zielmolekül auf Immunzellen auf, die zusammen dieses schädliche Gefäßwachstum antreiben, und eröffnet damit einen möglichen Weg hin zu sichereren, tablettenartigen Therapien in der Zukunft.
Ein verborgener Störenfried, gebildet aus einem nützlichen Fett
Die Geschichte beginnt mit einem fettähnlichen Botenstoff namens Sphingosin‑1‑phosphat (S1P). S1P hilft normalerweise dabei, Blutgefäße stabil und undurchlässig zu halten, und Wirkstoffe, die an seinen Rezeptoren wirken, werden bereits bei Erkrankungen wie Multipler Sklerose eingesetzt. Wenn S1P jedoch abgebaut wird, kann daraus ein reaktives Abbauprodukt namens 2‑Hexadecenal entstehen, ein kleines, instabiles Aldehyd. Bislang war kaum bekannt, welche Wirkung dieses Nebenprodukt in lebenden Gefäßen, insbesondere im Auge, hat. Die Autorinnen und Autoren vermuteten, dass sich bei mangelhafter Beseitigung von 2‑Hexadecenal Zellen schädigen und das feine Gefäßnetz, das die lichtempfindliche Netzhaut versorgt, gestört werden könnte.
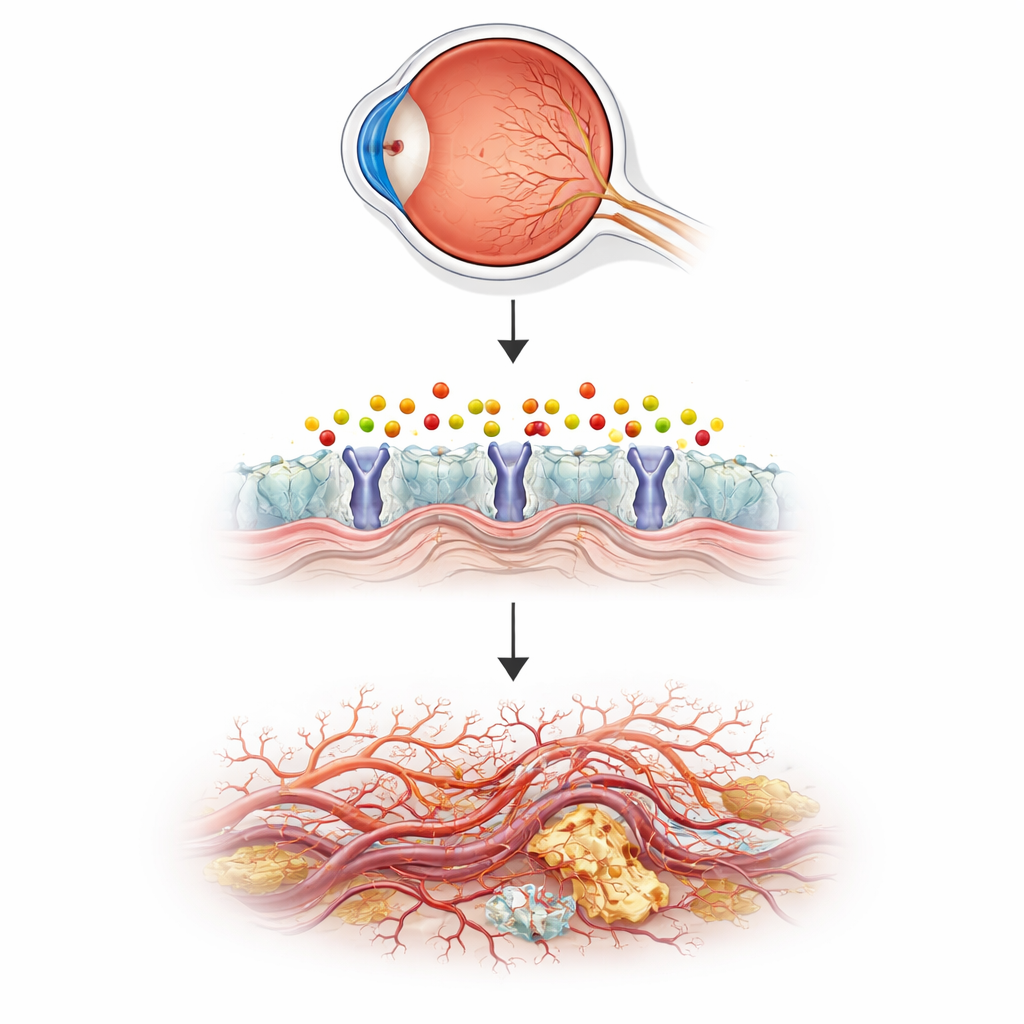
Kranke menschliche Augen mit winzigen Fischen modelliert
Um diese Idee zu prüfen, verwendete das Team Zebrafische, kleine Aquarienfische, deren transparente Embryonen es erlauben, die Gefäßbildung direkt zu beobachten. Sie schalteten ein Gen namens aldh3b1 aus, das ein Enzym produziert, das 2‑Hexadecenal entgiftet, und verfolgten das Gefäßwachstum im Auge. Fische ohne dieses Enzym entwickelten zu viele feine Sprosse und verzweigende Gefäße in der Netzhaut, in einem Muster ähnlich dem frühen Stadium der menschlichen Erkrankung, während größere Gefäße im Körper normal blieben. Wurden normale Fische kurz 2‑Hexadecenal ausgesetzt, überwucherten ihre Augengefäße auf ähnliche Weise. Ein natürliches Molekül namens Carnosin, das reaktive Aldehyde binden kann, kehrte diese Veränderungen um und verknüpfte so das abnorme Wachstum direkt mit der Anreicherung dieser einzigen lipidabgeleiteten Chemikalie.
Eisenungleichgewicht und eine feurige Form des Zelltods
Die Forschenden fragten dann, wie dieses kleine Molekül Gefäße so stark umgestalten kann. Durch die Kombination von Genaktivitätsprofilen und detaillierter chemischer Analyse fanden sie heraus, dass überschüssiges 2‑Hexadecenal den Umgang der Zellen mit Eisen stört und sie in Richtung Ferroptose treibt, einer jüngst beschriebenen, eisengetriebenen Form des Zelltods, die sich durch unkontrollierte Lipidoxidation auszeichnet. Marker für Lipidschäden und Eisenüberladung stiegen in den Fischaugen an, während zentrale Schutzsysteme, die normalerweise Ferroptose verhindern—darunter das Protein FSP1 und das antioxidative Enzym GPX4—herunterreguliert waren. Die Blockade der Ferroptose mit einem spezialisierten Inhibitor milderte das abnorme Gefäßwachstum, während die direkte Hemmung von FSP1 krankheitsähnliche Veränderungen nachahmte und diesen Signalweg in den Mittelpunkt des Schadens rückte.
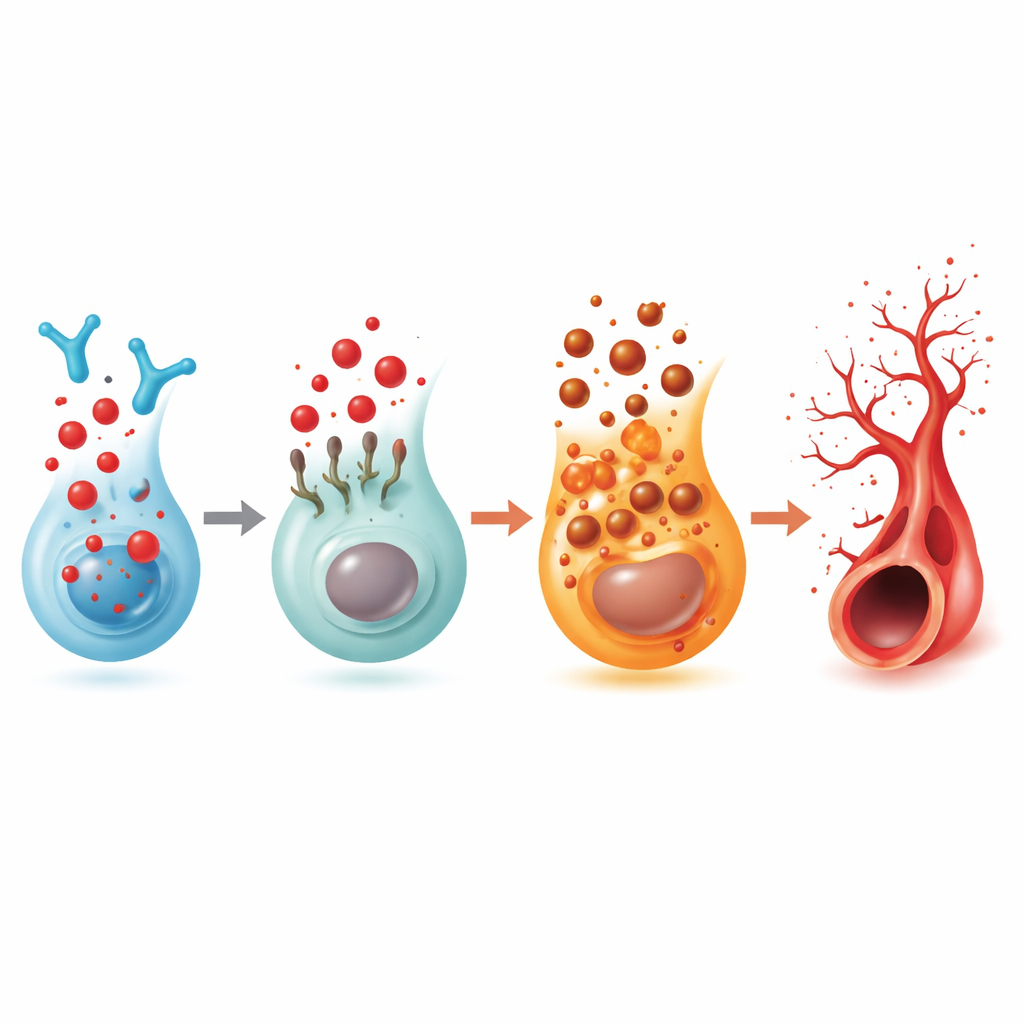
Ein Rezeptorschalter, der Fett‑Signale, Immunzellen und Gefäße verbindet
Da 2‑Hexadecenal aus S1P stammt, untersuchte das Team S1P und seine fünf bekannten Rezeptoren. Nur einer von ihnen, S1PR5 genannt, sank in den Fischaugen konsequent, wenn 2‑Hexadecenal anstieg. Das Herausschalten von S1PR5 allein führte zu derselben übermäßigen Verzweigung und senkte gleichzeitig FSP1, womit dieser Rezeptor an die Ferroptose‑Bremse gekoppelt wurde. Ein selektiver S1PR5‑Aktivator stellte in sowohl 2‑Hexadecenal‑behandelten als auch enzymdefizienten Fischen normalere Gefäßmuster wieder her. Biophysikalische und computermodellierende Untersuchungen zeigten, dass 2‑Hexadecenal direkt an S1PR5 binden und dessen Internalisierung in die Zellen auslösen kann, wodurch das Signalsignal an der Zelloberfläche abgeschwächt wird. In humanen Einzell‑Netzhautdaten war S1PR5 hauptsächlich auf natürlichen Killerzellen (NK‑Zellen) nachweisbar, und in Proben von Patientinnen und Patienten mit fortgeschrittener diabetischer Augenerkrankung waren die S1PR5‑Spiegel deutlich erhöht, während verwandte Wege, die Sphingolipide, Immun‑Signalgebung und Ferroptose betreffen, in einer Weise verändert waren, die zu den Befunden im Zebrafisch passt.
Was das für Menschen mit diabetischer Augenerkrankung bedeuten könnte
Insgesamt zeichnet die Studie ein einfaches, aber kraftvolles Bild: Wenn das Enzym ALDH3B1 das aus S1P stammende Aldehyd 2‑Hexadecenal nicht beseitigen kann, stört dieses reaktive Abbauprodukt das S1PR5‑Signal auf Immunzellen, schwächt ein inneres Abwehrsystem gegen eisengetriebene Schäden und löst eine „rostähnliche“ Form des Zelltods aus, die das Eindringen verworrener, fragiler Gefäße in die Netzhaut fördert. Da bereits S1PR‑zielgerichtete Medikamente existieren und einige davon oral eingenommen werden können, bietet diese neu beschriebene 2‑Hexadecenal–S1PR5–Ferroptose‑Achse einen plausiblen Ansatz für künftige Behandlungen, die das Fortschreiten der diabetischen Retinopathie verlangsamen oder verhindern könnten und die möglicherweise weniger Injektionen in das Auge erfordern.
Zitation: Qian, X., Ge, R., Chu, Y. et al. Sphingosine-1-Phosphate-derived 2-Hexadecenal is a central mediator of ocular neovascularization by inhibiting Sphingosine-1-Phosphate receptor 5. Nat Commun 17, 3488 (2026). https://doi.org/10.1038/s41467-026-71792-3
Schlüsselwörter: diabetische Retinopathie, retinale Blutgefäße, Lipid‑Signalgebung, Ferroptose, Sphingosin-1‑Phosphat-Rezeptor