Clear Sky Science · ar
المركب 2-هكساديسينال المستمد من سفينغوسين-1-فوسفات هو وسيط مركزي لتكوّن أوعية دموية جديدة في العين عبر تثبيط مستقبل سفينغوسين-1-فوسفات 5
لماذا تهم هذه الدراسة البصر
فقدان البصر الناتج عن أمراض مثل اعتلال العين السكري غالباً ما ينجم عن نمو أوعية دموية هشة ومتسرِّّبة في الشبكية في خلفية العين. العلاجات الحالية قادرة على إنقاذ البصر، لكنها مكلفة وغالباً ما تكون تدخلية ولا تنجح لدى الجميع. تكشف هذه الدراسة عن مركب كيميائي كان خفياً سابقاً وجزيئ هدف جديد على خلايا الجهاز المناعي يعملان معاً على دفع هذا النمو الوعائي الضار، ما يفتح طريقاً محتملاً لعلاجات مستقبلية أكثر أماناً على شكل حبوب.
مشكِل خفي ينتج من دهون نافعة
تبدأ القصة مع رسول شبيه بالدهون يسمى سفينغوسين‑1‑فوسفات (S1P). عادةً يساعد S1P في الحفاظ على استقرار الأوعية الدموية ومقاومتها للتسرب، والأدوية التي تؤثر على مستقبلاته تُستخدم بالفعل في أمراض مثل التصلب المتعدد. لكن عندما يتحلل S1P، يمكن أن يشكل ناتجاً تفاعلياً يسمى 2‑هكساديسينال، وهو ألدهيد صغير وغير مستقر. حتى الآن، كان القليل جداً معروفاً عن تأثير هذا الناتج في الأوعية الحية، وخصوصاً في العين. افترض الباحثون أنه إذا لم يُزل 2‑هكساديسينال بشكل صحيح، فقد يضر الخلايا ويؤثر على الشبكة الدقيقة للأوعية التي تغذي الشبكية الحساسة للضوء.
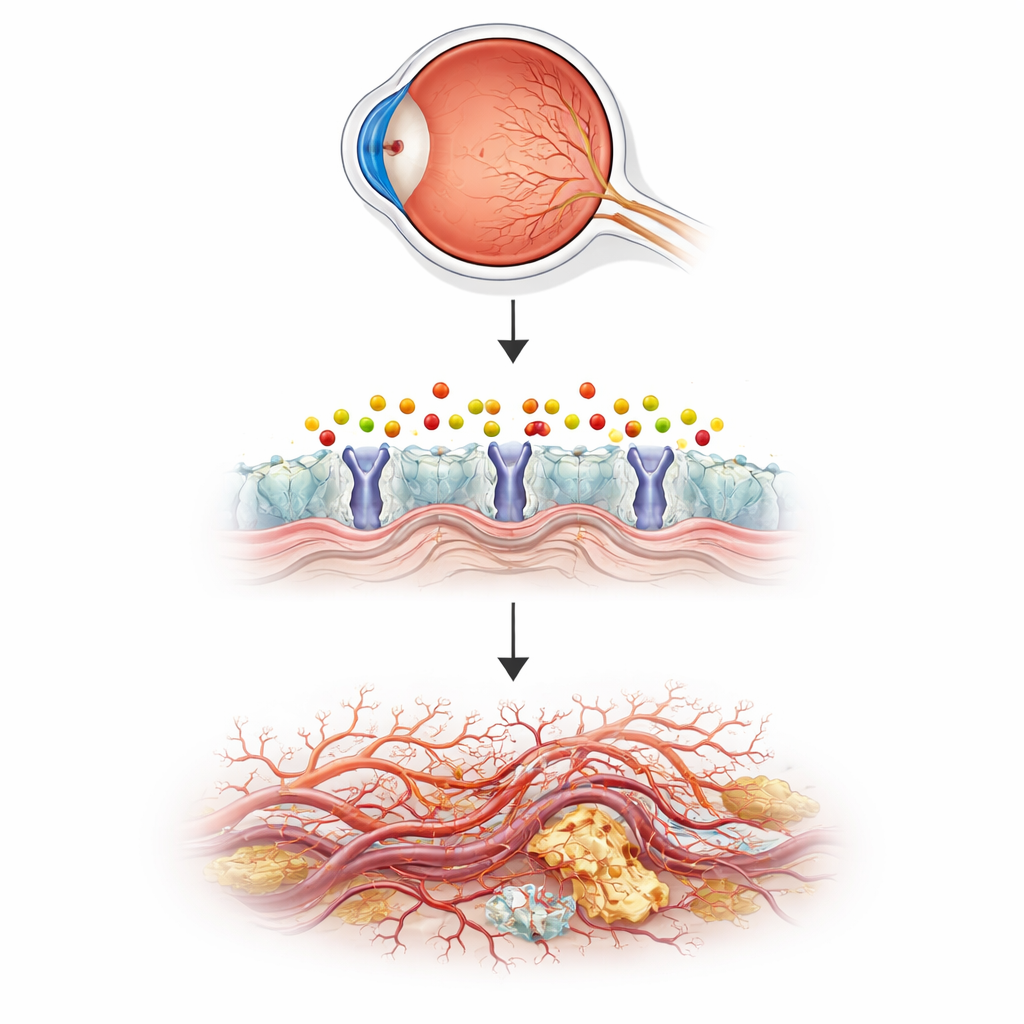
استخدام أسماك صغيرة كنموذج لعيون بشرية مريضة
لاختبار هذه الفكرة، لجأ الفريق إلى سمكة الزبرافش، وهي سمكة صغيرة أجنة شفافة تسمح للعلماء بمراقبة تكوّن الأوعية الدموية مباشرة. أوقفوا جيناً يدعى aldh3b1، الذي يصنع إنزيمًا يزيل سمّية 2‑هكساديسينال، وتابعوا نمو الأوعية في العين. طورت الأسماك التي تفتقر إلى هذا الإنزيم فروعًا وعديدات تشعب دقيقة مفرطة في الشبكية، بنمط مشابه للمرض البشري المبكر، بينما بقيت الأوعية الكبيرة في الجسم طبيعية. عندما غُمرت أسماك طبيعية ببساطة في محلول يحتوي على 2‑هكساديسينال، نمت أوعيتها العينية بشكل مفرط بنفس الطريقة. جزيء طبيعي يسمى كارنوسين، والذي يمكنه امتصاص الألدهيدات التفاعلية، عكس هذه التغيرات، ما ربط النمو الشاذ مباشرة بتراكم هذا المركب المستمد من الدهون.
اختلال حديدي وشكل مؤجج من موت الخلايا
سأل الباحثون بعد ذلك كيف يمكن لهذا الجزيء الصغير أن يعيد تشكيل الأوعية بقوة كهذه. من خلال الجمع بين تحليل نشاط الجينات والتحليل الكيميائي التفصيلي، وجدوا أن فائض 2‑هكساديسينال يعطل طريقة تعامل الخلايا مع الحديد ويدفعها نحو الفيروبتوزيس، وهو شكل حديث الاعتراف من موت الخلايا يقوده الحديد ويتسم بأكسدة شديدة للدهون. ارتفعت مؤشرات تلف الدهون والحمولة الحديدية في عيون الأسماك، بينما انخفضت أنظمة الحماية الرئيسية التي تمنع الفيروبتوزيس عادةً، بما في ذلك بروتين يسمى FSP1 وإنزيم مضاد للأكسدة وهو GPX4. إن حجب الفيروبتوزيس بمثبط متخصص خفف من نمو الأوعية الشاذ، بينما أدى حجب FSP1 مباشرة إلى تقليد التغيرات الشبيهة بالمرض، مما يضع هذا المسار في قلب الضرر.
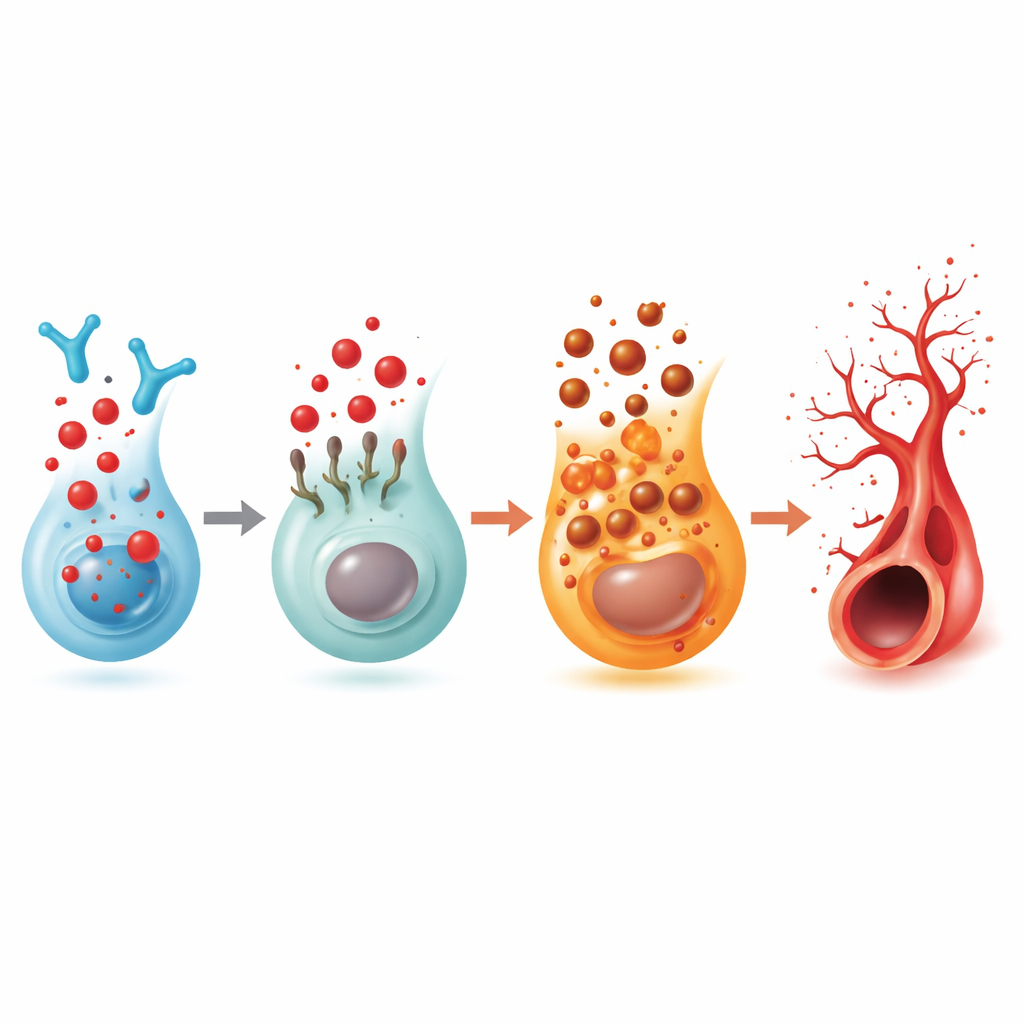
تبديل في المستقبل يربط إشارات الدهون وخلايا المناعة والأوعية
بما أن 2‑هكساديسينال ينبع من S1P، فحص الفريق المستقبلات الخمسة المعروفة لـS1P. وجدوا أن واحداً فقط، يدعى S1PR5، انخفض باستمرار في عيون الأسماك عند تراكم 2‑هكساديسينال. أدت خفض S1PR5 وحده إلى نفس النمو المفرط للفروع، وفي الوقت نفسه خفضت مستوى FSP1، ما ربط هذا المستقبل بكبح الفيروبتوزيس. عقار منشط انتقائي لـS1PR5 أعاد أنماط أوعية أقرب إلى الطبيعية في كل من الأسماك المعالجة بـ2‑هكساديسينال وتلك الناقصة في الإنزيم. أظهرت دراسات بيوفيزيائية ونمذجة حاسوبية أن 2‑هكساديسينال يمكن أن يرتبط مباشرة بـS1PR5 ويحفز إدخاله داخل الخلايا، مما يضعف إشارته السطحية. في بيانات شبكية بشرية على مستوى الخلية الواحدة، وُجد S1PR5 بشكل أساسي على خلايا قاتلة طبيعية (NK)، وفي عينات من مرضى لديهم اعتلال عيني سكري متقدم، كانت مستويات S1PR5 أعلى بشكل ملحوظ بينما تَعدَّلت المسارات المرتبطة بالسفينغوليبيدات وإشارات المناعة والفيروبتوزيس بطرق تتوافق مع نتائج الزبرافش.
ما الذي قد يعنيه هذا للناس المصابين بمرض العين السكري
تجمع هذه الدراسة، بصورة مبسطة لكنها مقنعة، صورة مفادها: عندما لا يستطيع إنزيم ALDH3B1 إزالة ألدهيد S1P المشتق 2‑هكساديسينال، يزعزع هذا الناتج التفاعلي إشارة S1PR5 على خلايا الجهاز المناعي، ويضعف جهاز حماية داخلي ضد الضرر المدفوع بالحديد، ويسهم في إطلاق شكل من موت الخلايا «يشبه الصدأ» الذي يشجع الأوعية المتشابكة والهشة على غزو الشبكية. وبما أن أدوية تستهدف مستقبلات S1PR موجودة بالفعل وبعضها يؤخذ عن طريق الفم، فإن المحور الجديد المرسوم 2‑هكساديسينال–S1PR5–الفيروبتوزيس يقدم مساراً معقولاً لعلاجات مستقبلية قد تبطئ أو تمنع فقدان البصر في اعتلال الشبكية السكري مع تقليل الحاجة للحقن داخل العين.
الاستشهاد: Qian, X., Ge, R., Chu, Y. et al. Sphingosine-1-Phosphate-derived 2-Hexadecenal is a central mediator of ocular neovascularization by inhibiting Sphingosine-1-Phosphate receptor 5. Nat Commun 17, 3488 (2026). https://doi.org/10.1038/s41467-026-71792-3
الكلمات المفتاحية: اعتلال الشبكية السكري, الأوعية الدموية الشبكية, إشارات الدهون, النفروز الحديدي (الفيروبتوزيس), مستقبل سفينغوسين-1-فوسفات