Clear Sky Science · sv
2‑Hexadecenal som härstammar från sphingosin‑1‑fosfat är en central mediator av okulär neovaskularisation genom att hämma sphingosin‑1‑fosfat‑receptor 5
Varför denna studie är viktig för synen
Synförlust vid sjukdomar som diabetisk ögonsjukdom uppstår ofta på grund av tillväxt av sköra, läckande blodkärl i näthinnan längst bak i ögat. Befintliga behandlingar kan rädda synen, men de är dyra, invasiva och fungerar inte för alla. Denna studie avslöjar en tidigare dold kemisk gärningsman och ett nytt målmolekyl på immunceller som tillsammans driver denna skadliga kärltillväxt, och öppnar en möjlig väg mot säkrare, tablettbaserade behandlingar i framtiden.
En dold inkräktare skapad av ett hjälpsamt fett
Berättelsen börjar med ett fettliknande budbärarmolekyl kallad sphingosin‑1‑fosfat (S1P). S1P hjälper normalt till att hålla blodkärl stabila och motståndskraftiga mot läckage, och läkemedel som verkar på dess receptorer används redan mot sjukdomar som multipel skleros. Men när S1P bryts ner kan det bildas en reaktiv biprodukt kallad 2‑hexadecenal, ett litet, instabilt aldehyd. Fram tills nu har man vetat nästan ingenting om vad denna biprodukt gör i levande blodkärl, särskilt i ögat. Författarna misstänkte att om 2‑hexadecenal inte rensas bort ordentligt kan det skada celler och störa det fina kärlnät som försörjer den ljuskänsliga näthinnan.
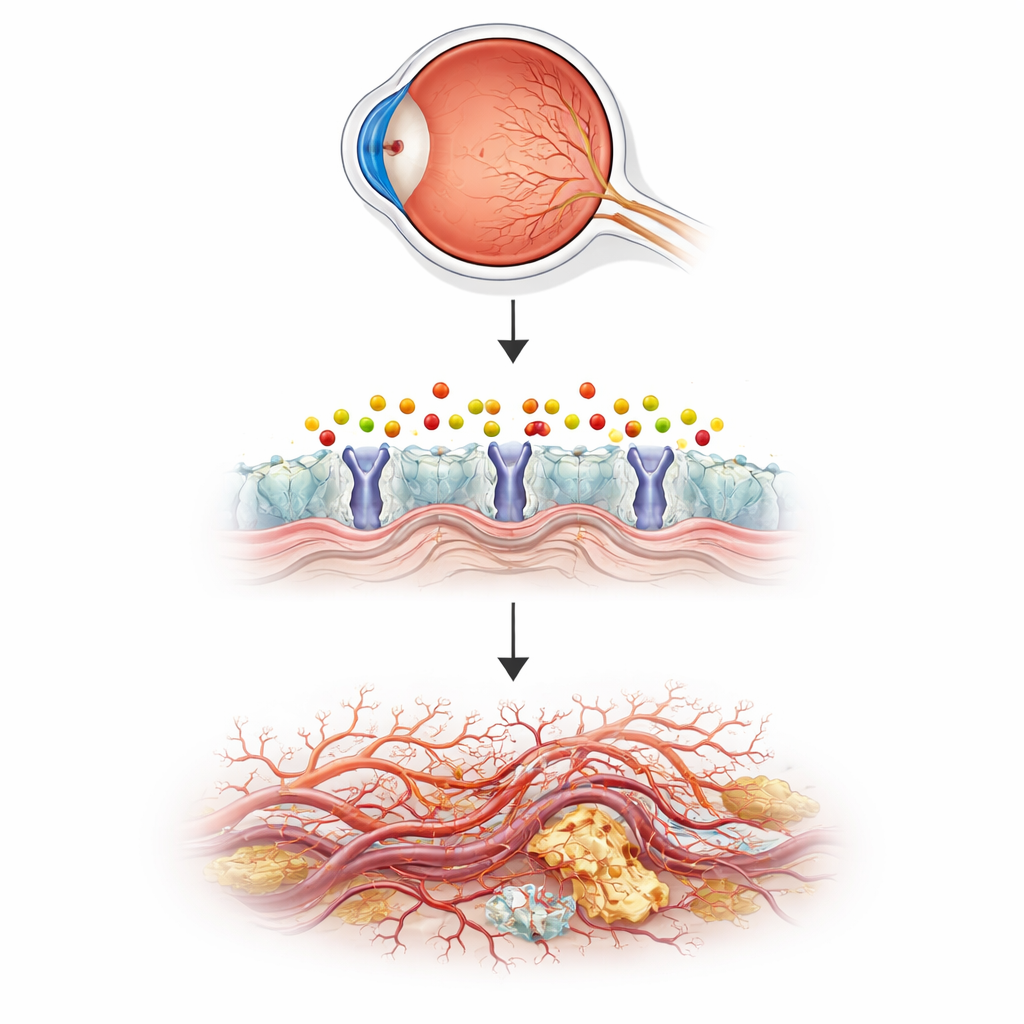
Att använda små fiskar för att modellera sjuka mänskliga ögon
För att testa idén vände teamet sig till zebrafisk, en liten akvariefisk med genomskinliga embryon som låter forskare direkt iaktta blodkärl när de bildas. De stängde av en gen kallad aldh3b1, som kodar för ett enzym som avgiftar 2‑hexadecenal, och följde kärltillväxten i ögat. Fiskar som saknade detta enzym utvecklade för många fina skott och förgrenade kärl i näthinnan, i ett mönster som liknar tidig mänsklig sjukdom, medan större kroppskärl förblev normala. När normala fiskar helt enkelt badades i 2‑hexadecenal växte deras ögonkärl på samma sätt. Ett naturligt ämne kallat karnosin, som kan fånga upp reaktiva aldehyder, reverserade dessa förändringar och kopplade den abnorma tillväxten direkt till ansamlingen av denna enda lipid‑härledda kemikalie.
Järnbalans och en brännande form av celldöd
Forskarna frågade sedan hur denna lilla molekyl kunde omforma kärl så kraftfullt. Genom att kombinera genaktivitetsprofilering och detaljerad kemisk analys fann de att överskott av 2‑hexadecenal störde hur celler hanterar järn och pressade dem mot ferroptos, en nyligen erkänd, järn‑driven form av celldöd präglad av okontrollerad fettoxidation. Markörer för lipidskada och järnöverskott ökade i fisköga, medan nyckelskyddssystem som normalt stoppar ferroptos, inklusive ett protein kallat FSP1 och antioxidantenzymet GPX4, nedreglerades. Att blockera ferroptos med en specialiserad hämmare lindrade den abnorma kärltillväxten, medan direkt blockad av FSP1 efterliknade sjukdomsliknande förändringar och placerade denna väg i centrum för skadan.
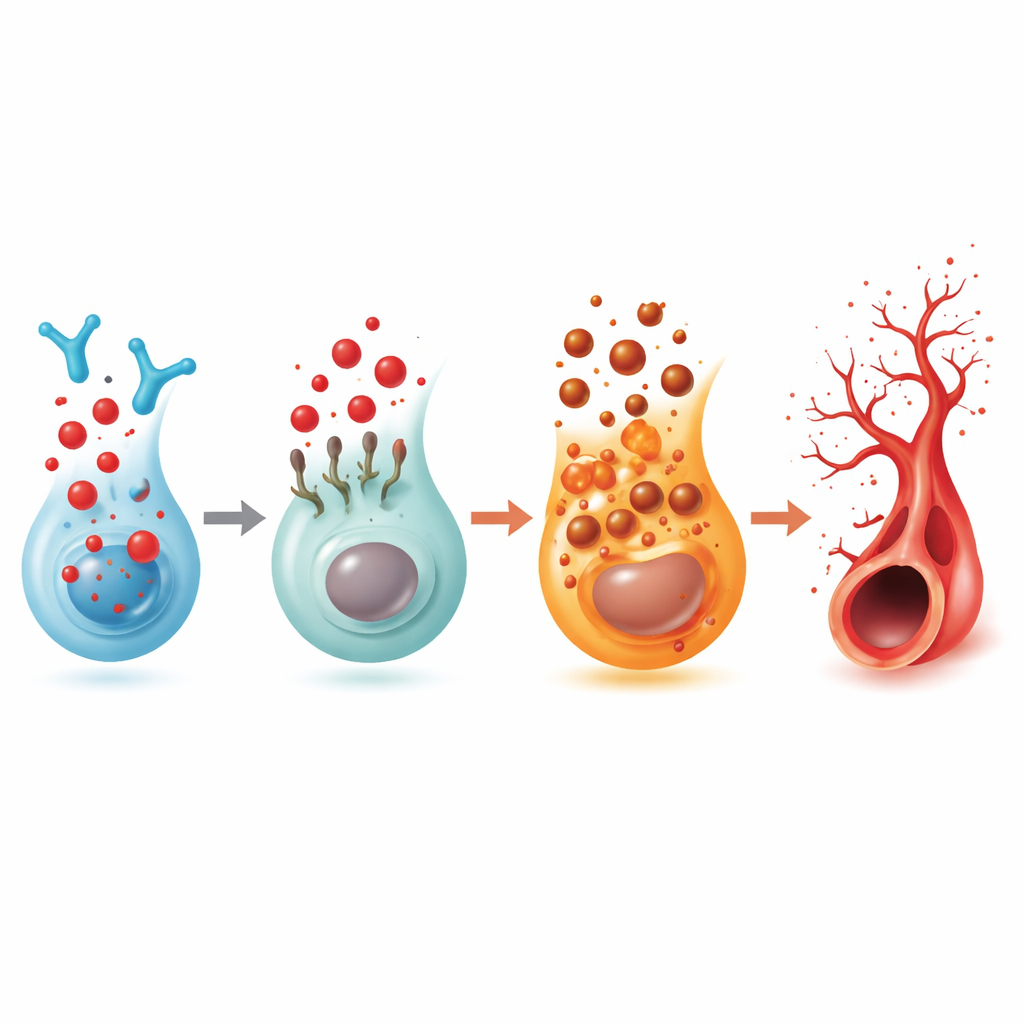
En receptorväxling som länkar fettsignaler, immunceller och kärl
Där 2‑hexadecenal kommer från S1P undersökte teamet S1P:s fem kända receptorer. Bara en, kallad S1PR5, sjönk konsekvent i fiskögonen när 2‑hexadecenal ackumulerades. Nedreglering av S1PR5 ensam orsakade samma överdrivna utstickande kärl och sänkte samtidigt FSP1, vilket kopplade denna receptor till ferroptosens broms. Ett selektivt S1PR5‑aktiverande läkemedel återställde mer normala kärlmönster både i 2‑hexadecenal‑behandlade och enzym‑defekta fiskar. Biofysisk och datorbaserad modellering visade att 2‑hexadecenal kan binda direkt till S1PR5 och trigga dess internalisering i celler, vilket försvagar dess signal från ytan. I mänskliga enkellcells‑näthinnedata fanns S1PR5 huvudsakligen på naturliga mördarceller (NK‑celler), och i prover från patienter med avancerad diabetisk ögonsjukdom var S1PR5‑nivåerna markant högre medan närliggande vägar som involverar sfingolipider, immunsignalering och ferroptos var förändrade på sätt som överensstämmer med fynden i zebrafisk.
Vad detta kan betyda för människor med diabetisk ögonsjukdom
Tillsammans ger studien en enkel men kraftfull bild: när enzymet ALDH3B1 inte kan rensa bort S1P‑härledda aldehyden 2‑hexadecenal stör denna reaktiva biprodukt S1PR5‑signalen på immunceller, försvagar ett internt försvar mot järn‑driven skada och bidrar till att utlösa en form av ”rostlik” celldöd som uppmuntrar trassliga, sköra kärl att invadera näthinnan. Eftersom S1PR‑riktade läkemedel redan finns och några kan tas i tablettform erbjuder denna nykartlagda 2‑hexadecenal–S1PR5–ferroptos‑axel en rimlig väg mot framtida behandlingar som kan bromsa eller förhindra synförlust vid diabetisk retinopati med färre injektioner i ögat.
Citering: Qian, X., Ge, R., Chu, Y. et al. Sphingosine-1-Phosphate-derived 2-Hexadecenal is a central mediator of ocular neovascularization by inhibiting Sphingosine-1-Phosphate receptor 5. Nat Commun 17, 3488 (2026). https://doi.org/10.1038/s41467-026-71792-3
Nyckelord: diabetisk retinopati, retinala blodkärl, lipidsignalering, ferroptos, sphingosin‑1‑fosfat‑receptor