Clear Sky Science · pl
2‑Heksadekenal pochodzący z sfingozyno‑1‑fosforanu jest kluczowym mediatorem neowaskularyzacji oka poprzez hamowanie receptora S1P5
Dlaczego to badanie ma znaczenie dla wzroku
Utrata wzroku w chorobach takich jak cukrzycza choroba oczu często wynika z powstawania kruchych, przeciekających naczyń krwionośnych w siatkówce z tyłu oka. Obecne terapie potrafią uratować wzrok, ale są kosztowne, inwazyjne i nie działają u wszystkich. To badanie ujawnia dotąd ukryte chemiczne zagrożenie oraz nowy docelowy receptor na komórkach odpornościowych, które wspólnie napędzają szkodliwy wzrost naczyń, otwierając potencjalną drogę do bezpieczniejszych, doustnych terapii w przyszłości.
Ukryty sprawca powstały z pomocnego lipidu
Historia zaczyna się od tłuszczopodobnego przekaźnika zwanego sfingozyno‑1‑fosforanem (S1P). S1P zwykle pomaga utrzymywać naczynia krwionośne stabilne i odporne na przecieki, a leki działające na jego receptory są już stosowane w chorobach takich jak stwardnienie rozsiane. Jednak gdy S1P ulega rozkładowi, może powstać reaktywny produkt uboczny zwany 2‑heksadekenalem, mały, niestabilny aldehyd. Do tej pory prawie nic nie wiadomo było o działaniu tego produktu ubocznego w żywych naczyniach, szczególnie w oku. Autorzy podejrzewali, że jeśli 2‑heksadekenal nie jest prawidłowo usuwany, może uszkadzać komórki i zaburzać delikatną sieć naczyń odżywiających światłoczułą siatkówkę.
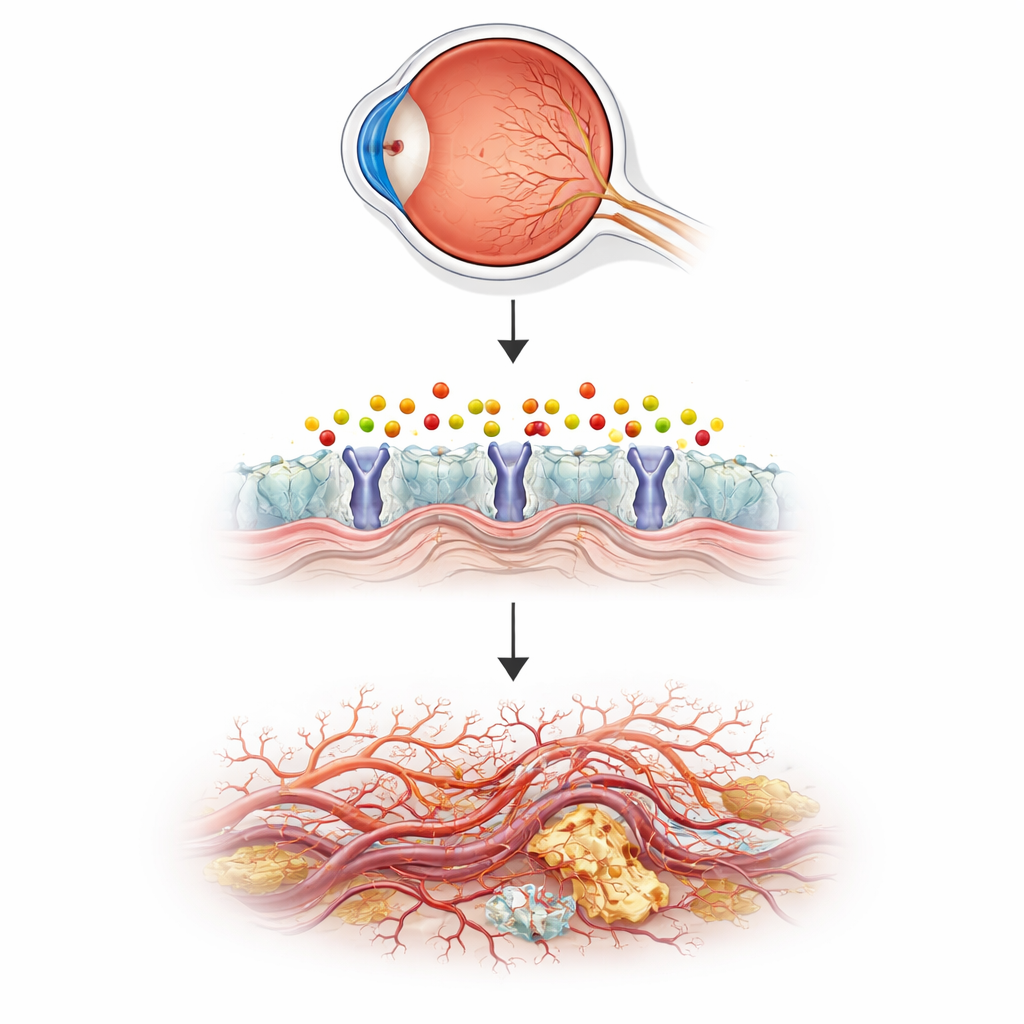
Wykorzystanie drobnych ryb do modelowania chorych ludzkich oczu
Aby sprawdzić ten pomysł, zespół sięgnął po larwy danio pręgowanego (zebrafish), małą rybę akwariową, której przezroczyste embriony pozwalają naukowcom bezpośrednio obserwować tworzenie się naczyń. Wyłączyli gen aldh3b1, który koduje enzym detoksyfikujący 2‑heksadekenal, i śledzili rozwój naczyń w oku. Ryby pozbawione tego enzymu rozwijały zbyt wiele drobnych rozgałęzień i pączków naczyniowych w siatkówce, w wzorcu podobnym do wczesnej choroby u ludzi, podczas gdy większe naczynia w ciele pozostawały prawidłowe. Gdy normalne ryby wystawiono jedynie na działanie 2‑heksadekenalu, naczynia w oku nadmiernie rosły w ten sam sposób. Naturalna cząsteczka karnozyna, która może wychwytywać reaktywne aldehydy, odwróciła te zmiany, wiążąc nieprawidłowy wzrost bezpośrednio z nagromadzeniem tego pojedynczego związku pochodzenia lipidowego.
Nierównowaga żelaza i „ognista” forma śmierci komórki
Naukowcy zastanawiali się następnie, jak ta mała cząsteczka może tak silnie przekształcać naczynia. Łącząc profilowanie aktywności genów z dokładną analizą chemiczną, stwierdzili, że nadmiar 2‑heksadekenalu zaburza gospodarkę żelazem w komórkach i popycha je w kierunku ferroptozy — niedawno rozpoznanej, zależnej od żelaza formy śmierci komórki charakteryzującej się niekontrolowaną oksydacją lipidów. Wskaźniki uszkodzeń lipidów i przeciążenia żelazem wzrosły w oczach ryb, podczas gdy kluczowe systemy ochronne przeciwdziałające ferroptozie, w tym białko FSP1 i enzym antyoksydacyjny GPX4, zostały osłabione. Zablokowanie ferroptozy specjalnym inhibitorem złagodziło nieprawidłowy wzrost naczyń, natomiast bezpośrednie zahamowanie FSP1 naśladowało zmiany przypominające chorobę, umieszczając tę ścieżkę w centrum uszkodzeń.
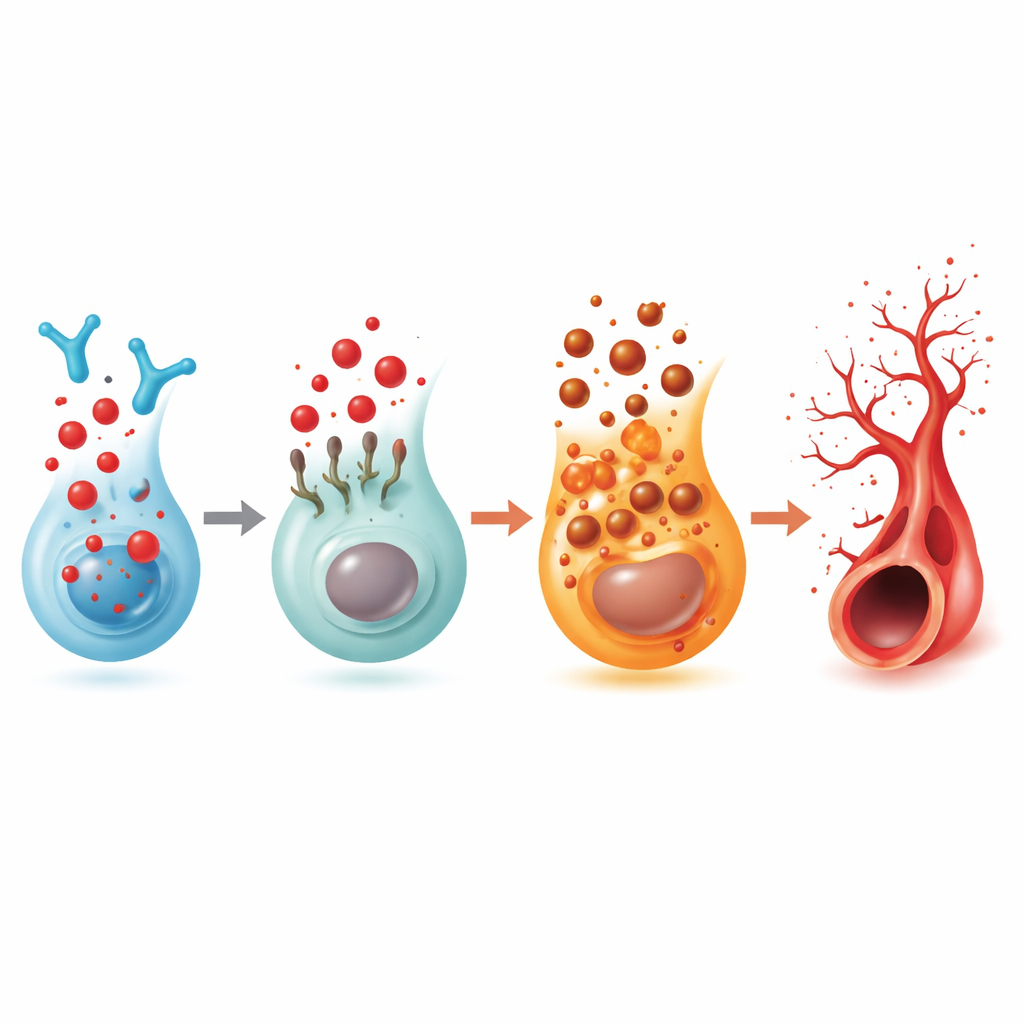
Przełączenie receptora łączące sygnały lipidowe, komórki odpornościowe i naczynia
Ponieważ 2‑heksadekenal pochodzi z S1P, zespół przebadał pięć znanych receptorów S1P. Tylko jeden, nazwany S1PR5, systematycznie obniżał poziom w oczach ryb przy nagromadzeniu 2‑heksadekenalu. Wyłączenie samego S1PR5 powodowało ten sam nadmierny rozrost pączków, a jednocześnie obniżało poziom FSP1, łącząc ten receptor z hamulcem ferroptozy. Selektywny lek aktywujący S1PR5 przywracał bardziej normalny wzorzec naczyń zarówno u ryb traktowanych 2‑heksadekenalem, jak i u ryb z niedoborem enzymu. Badania biofizyczne i modelowanie komputerowe wykazały, że 2‑heksadekenal może wiązać się bezpośrednio z S1PR5 i wywoływać jego internalizację do wnętrza komórek, osłabiając sygnał z powierzchni. W ludzkich danych pojedynczych komórek siatkówki S1PR5 występował głównie na komórkach odpornościowych typu natural killer (NK), a w próbkach od pacjentów z zaawansowaną cukrzycową chorobą oka poziomy S1PR5 były wyraźnie podwyższone, podczas gdy powiązane szlaki obejmujące sfingolipidy, sygnalizację immunologiczną i ferroptozę były zmienione w sposób zgodny z obserwacjami u danio pręgowanego.
Co to może znaczyć dla osób z cukrzyczą chorobą oczu
Podsumowując, badanie przedstawia prosty, ale przekonujący mechanizm: gdy enzym ALDH3B1 nie usuwa aldehydu 2‑heksadekenalu pochodzącego z S1P, ten reaktywny produkt zaburza sygnalizację S1PR5 na komórkach odpornościowych, osłabia wewnętrzny system obronny przeciwko uszkodzeniom napędzanym żelazem i sprzyja formie „rdzewienia” komórek — ferroptozie — która ułatwia inwazję poskręcanych, kruchych naczyń do siatkówki. Ponieważ leki celujące w receptory S1PR już istnieją i niektóre można podawać doustnie, nowo zmapowana oś 2‑heksadekenal–S1PR5–ferroptoza oferuje realistyczną ścieżkę do przyszłych terapii, które mogłyby spowolnić lub zapobiec utracie wzroku w retinopatii cukrzycowej, wymagając mniej zastrzyków do oka.
Cytowanie: Qian, X., Ge, R., Chu, Y. et al. Sphingosine-1-Phosphate-derived 2-Hexadecenal is a central mediator of ocular neovascularization by inhibiting Sphingosine-1-Phosphate receptor 5. Nat Commun 17, 3488 (2026). https://doi.org/10.1038/s41467-026-71792-3
Słowa kluczowe: retinopatia cukrzycowa, naczynia krwionośne siatkówki, sygnalizacja lipidowa, ferroptoza, receptor sfingozyno‑1‑fosforanu