Clear Sky Science · nl
Sphingosine-1-fosfaat-afgeleid 2-hexadecenaal is een centrale mediator van oculaire neovascularisatie door remming van sphingosine-1-fosfaat receptor 5
Waarom deze studie van belang is voor het gezichtsvermogen
Gezichtsverlies door aandoeningen zoals diabetische oogaandoeningen ontstaat vaak door de groei van fragiele, lekkende bloedvaten in het netvlies achter in het oog. Huidige behandelingen kunnen het gezichtsvermogen redden, maar ze zijn duur, invasief en werken niet voor iedereen. Deze studie onthult een eerder verborgen chemische veroorzaker en een nieuw doelmolecuul op immuuncellen die samen deze schadelijke vaatgroei aansturen, en opent daarmee een mogelijke weg naar veiligere, pillenachtige therapieën in de toekomst.
Een verborgen boosdoener gemaakt uit een nuttig vet
Het verhaal begint met een vetachtig boodschapper genaamd sphingosine‑1‑fosfaat (S1P). S1P helpt normaal gesproken de bloedvaten stabiel en lekbestendig te houden, en geneesmiddelen die op zijn receptoren werken worden al gebruikt bij ziekten zoals multiple sclerose. Maar wanneer S1P wordt afgebroken, kan het een reactief bijproduct vormen genaamd 2‑hexadecenaal, een klein, onstabiel aldehyde. Tot nu toe was er bijna niets bekend over wat dit bijproduct doet in levende bloedvaten, vooral in het oog. De auteurs vermoedden dat als 2‑hexadecenaal niet goed wordt afgevoerd, het cellen kan beschadigen en het fijne netwerk van vaten dat het lichtgevoelige netvlies voedt kan verstoren.
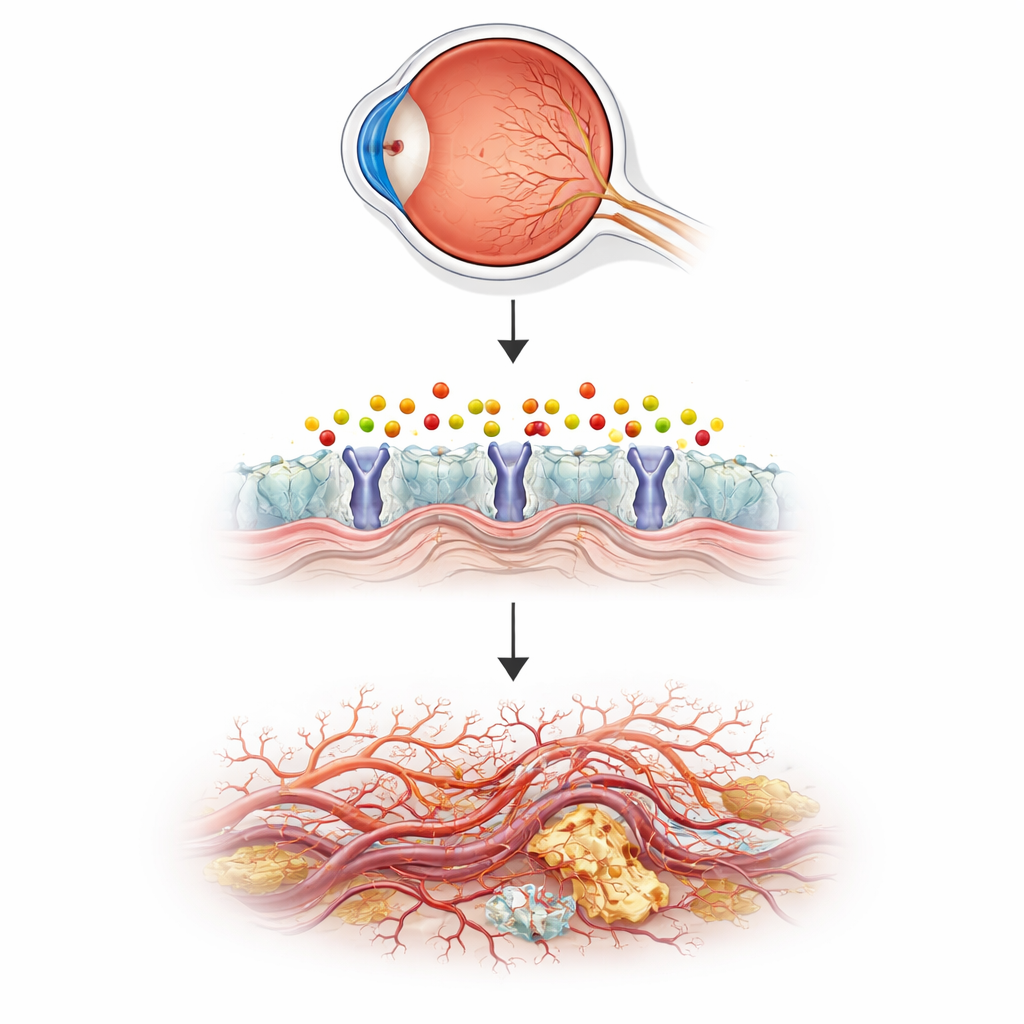
Gebruik van kleine visjes om zieke menselijke ogen te modelleren
Om dit idee te testen, wendde het team zich tot zebravisjes, een kleine aquariumvis waarvan de transparante embryo’s wetenschappers in staat stellen om bloedvaten tijdens de vorming direct te observeren. Ze schakelden een gen uit dat aldh3b1 heet, dat een enzym maakt dat 2‑hexadecenaal detoxt, en volgden de vaatgroei in het oog. Vissen zonder dit enzym ontwikkelden te veel fijne spruiten en vertakkende vaten in het netvlies, in een patroon vergelijkbaar met vroege menselijke ziekte, terwijl grotere lichaamsvaten normaal bleven. Toen normale vissen eenvoudigweg in 2‑hexadecenaal werden gebaad, groeiden hun oogaangezette vaten op dezelfde manier te veel. Een natuurlijke stof genaamd carnosine, die reactieve aldehyden kan binden, keerde deze veranderingen om, waardoor de abnormale groei direct werd gekoppeld aan de ophoping van deze enkelvoudige lipide‑afgeleide chemische stof.
IJzerbalans en een vurige vorm van celdood
De onderzoekers vroegen zich vervolgens af hoe dit kleine molecuul vaten zo krachtig kon hervormen. Door gen‑activiteitsprofilering te combineren met gedetailleerde chemische analyse, ontdekten ze dat overtollig 2‑hexadecenaal de manier verstoorde waarop cellen met ijzer omgaan en hen richting ferroptose duwde, een recent erkende, door ijzer aangedreven vorm van celdood die wordt gekenmerkt door ongecontroleerde vetoxidatie. Markers van lipideschade en ijzeroverschot stegen in de ogen van de vissen, terwijl belangrijke beschermende systemen die normaal ferroptose tegengaan, waaronder een eiwit genaamd FSP1 en het antioxidatieve enzym GPX4, werden teruggebracht. Het blokkeren van ferroptose met een gespecialiseerd remmingsmiddel verlichtte de abnormale vaatgroei, terwijl directe blokkade van FSP1 ziekteachtige veranderingen nabootste, waarmee dit pad centraal kwam te staan in de schade.
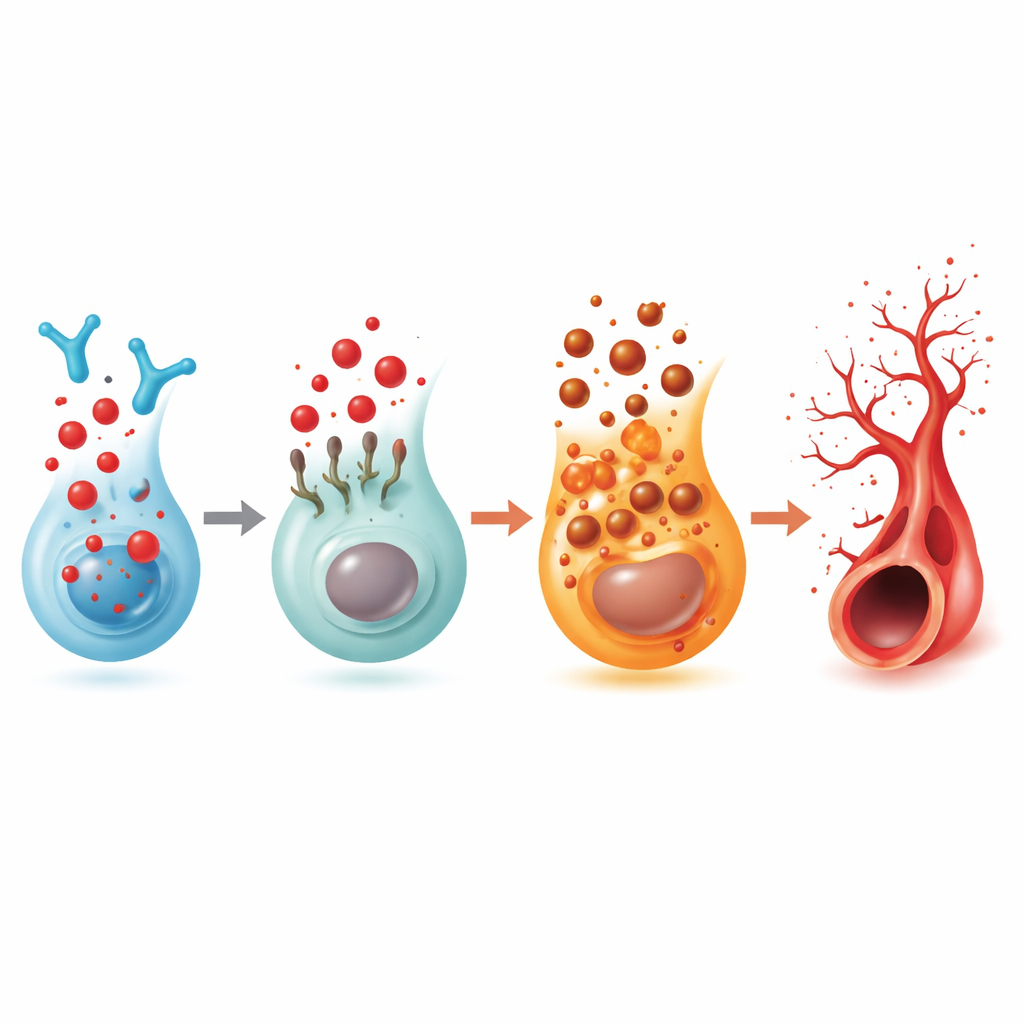
Een receptorwissel die vetsignalen, immuuncellen en vaten verbindt
Aangezien 2‑hexadecenaal afkomstig is van S1P, onderzocht het team de vijf bekende receptoren van S1P. Slechts één, genaamd S1PR5, daalde consequent in de vissenogen wanneer 2‑hexadecenaal zich ophoopte. Het uitschakelen van S1PR5 alleen veroorzaakte dezelfde overmatige sprouting en verlaagde tegelijkertijd FSP1, waarmee deze receptor aan de ferroptose‑rem werd gekoppeld. Een selectief S1PR5‑activerend middel herstelde meer normale vaatpatronen in zowel 2‑hexadecenaal‑behandelde als enzym‑deficiënte vissen. Biofysisch en computer‑modellering werk toonden aan dat 2‑hexadecenaal direct aan S1PR5 kan binden en de internalisatie ervan in cellen kan triggeren, waarmee het signaal aan het celoppervlak verzwakt wordt. In menselijke enkelcel‑retina‑gegevens werd S1PR5 voornamelijk gevonden op natural killer (NK) immuuncellen, en in monsters van patiënten met gevorderde diabetische oogaandoeningen waren de S1PR5‑niveaus opvallend hoger terwijl verwante routes die sphingolipiden, immuunsignaalgeving en ferroptose omvatten, waren veranderd op manieren die overeenkomen met de bevindingen in zebravissen.
Wat dit zou kunnen betekenen voor mensen met diabetische oogaandoening
Gezamenlijk schetst de studie een eenvoudig maar krachtig beeld: wanneer het enzym ALDH3B1 het S1P‑afgeleide aldehyde 2‑hexadecenaal niet kan opruimen, verstoort dit reactieve bijproduct het S1PR5‑signaal op immuuncellen, verzwakt het een intern verdedigingssysteem tegen ijzergedreven schade en helpt het een vorm van “roest‑achtige” celdood te veroorzaken die verwrongen, fragiele vaten aanmoedigt het netvlies binnen te dringen. Omdat S1PR‑gerichte geneesmiddelen al bestaan en sommige oraal kunnen worden ingenomen, biedt deze nieuw in kaart gebrachte 2‑hexadecenaal–S1PR5–ferroptose‑as een plausibele route naar toekomstige behandelingen die het verlies van gezichtsvermogen bij diabetische retinopathie mogelijk kunnen vertragen of voorkomen met minder injecties in het oog.
Bronvermelding: Qian, X., Ge, R., Chu, Y. et al. Sphingosine-1-Phosphate-derived 2-Hexadecenal is a central mediator of ocular neovascularization by inhibiting Sphingosine-1-Phosphate receptor 5. Nat Commun 17, 3488 (2026). https://doi.org/10.1038/s41467-026-71792-3
Trefwoorden: diabetische retinopathie, retinale bloedvaten, lipidesignaalgeving, ferroptose, sphingosine-1-fosfaat receptor