Clear Sky Science · es
El 2‑hexadecenal derivado de esfingosina‑1‑fosfato es un mediador central de la neovascularización ocular al inhibir el receptor 5 de esfingosina‑1‑fosfato
Por qué este estudio importa para la vista
La pérdida de visión por enfermedades como la retinopatía diabética suele deberse al crecimiento de vasos sanguíneos frágiles y permeables en la retina, en la parte posterior del ojo. Los tratamientos actuales pueden salvar la vista, pero son costosos, invasivos y no funcionan para todos. Este estudio revela un culpable químico hasta ahora oculto y una nueva molécula diana en células inmunitarias que, en conjunto, impulsan ese crecimiento vascular perjudicial, abriendo una vía posible hacia terapias orales más seguras en el futuro.
Un alborotador oculto formado a partir de una grasa útil
La historia comienza con un mensajero similar a una grasa llamado esfingosina‑1‑fosfato (S1P). El S1P normalmente ayuda a mantener los vasos sanguíneos estables y poco permeables, y fármacos que actúan sobre sus receptores ya se usan en enfermedades como la esclerosis múltiple. Pero cuando el S1P se descompone, puede formar un subproducto reactivo llamado 2‑hexadecenal, un aldehído pequeño e inestable. Hasta ahora, casi nada se sabía sobre lo que hace este subproducto en vasos sanguíneos vivos, especialmente en el ojo. Los autores sospecharon que si el 2‑hexadecenal no se elimina adecuadamente, podría dañar células y alterar la delicada red de vasos que nutre la retina, que capta la luz.
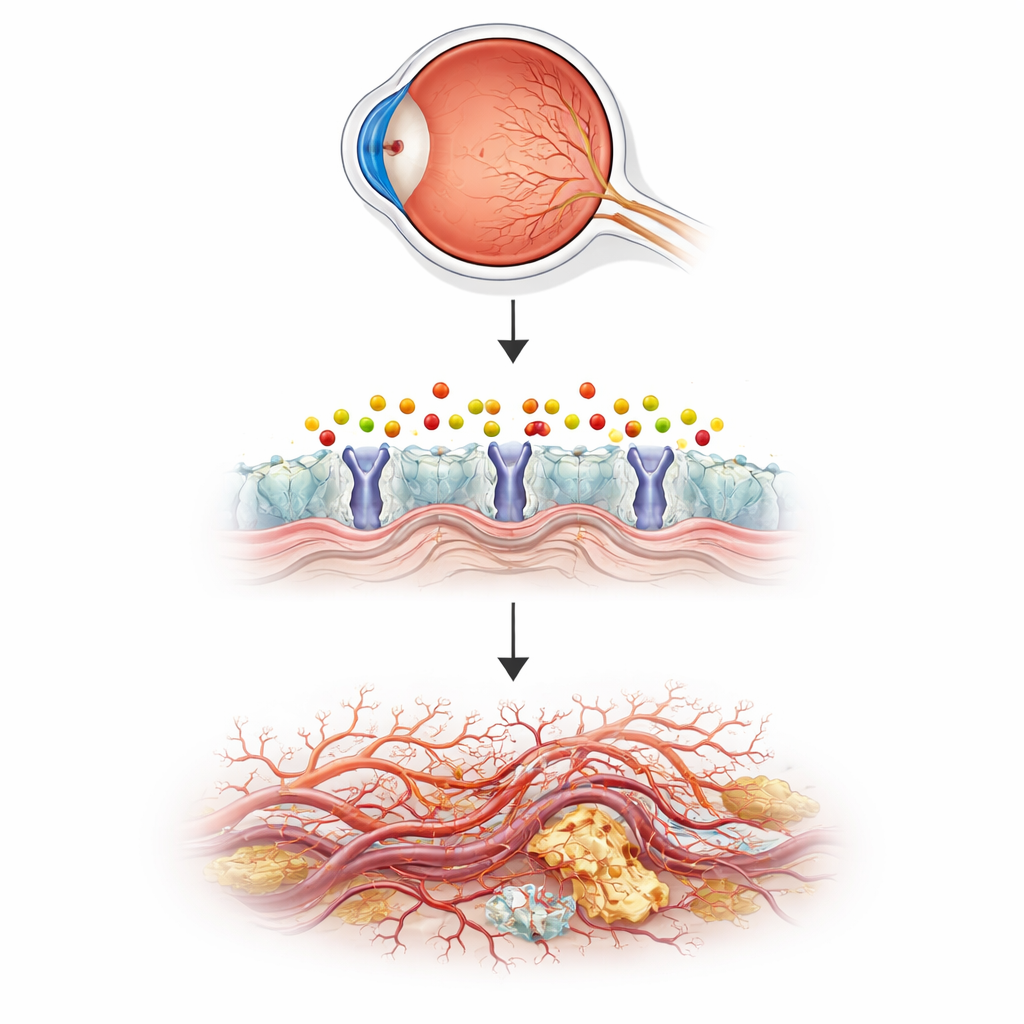
Usando peces diminutos para modelar ojos humanos enfermos
Para probar esta idea, el equipo recurrió al pez cebra, un pequeño pez de acuario cuyos embriones transparentes permiten a los científicos observar directamente la formación de vasos sanguíneos. Inactivaron un gen llamado aldh3b1, que codifica una enzima que desintoxica el 2‑hexadecenal, y siguieron el crecimiento de los vasos en el ojo. Los peces que carecían de esta enzima desarrollaron demasiados brotes finos y ramificaciones vasculares en la retina, en un patrón similar al de la enfermedad humana temprana, mientras que los vasos corporales mayores permanecieron normales. Cuando peces normales se bañaron simplemente en 2‑hexadecenal, sus vasos oculares también crecieron en exceso de la misma manera. Una molécula natural llamada carnosina, que puede capturar aldehídos reactivos, revirtió estos cambios, vinculando el crecimiento anómalo directamente con la acumulación de este único químico derivado de lípidos.
Desequilibrio de hierro y una forma inflamable de muerte celular
Los investigadores se preguntaron luego cómo esta molécula pequeña podía remodelar los vasos con tanta potencia. Al combinar perfiles de actividad génica y análisis químico detallado, encontraron que el exceso de 2‑hexadecenal alteraba la gestión del hierro en las células y las empujaba hacia la ferroptosis, una forma de muerte celular impulsada por el hierro recientemente reconocida y marcada por una oxidación masiva de lípidos. En los ojos de los peces aumentaron los marcadores de daño lipídico y sobrecarga de hierro, mientras que los sistemas protectores clave que normalmente impiden la ferroptosis, incluida una proteína llamada FSP1 y la enzima antioxidante GPX4, quedaron disminuidos. Bloquear la ferroptosis con un inhibidor especializado alivió el crecimiento vascular anómalo, mientras que bloquear directamente FSP1 imitó los cambios similares a la enfermedad, situando esta vía en el centro del daño.
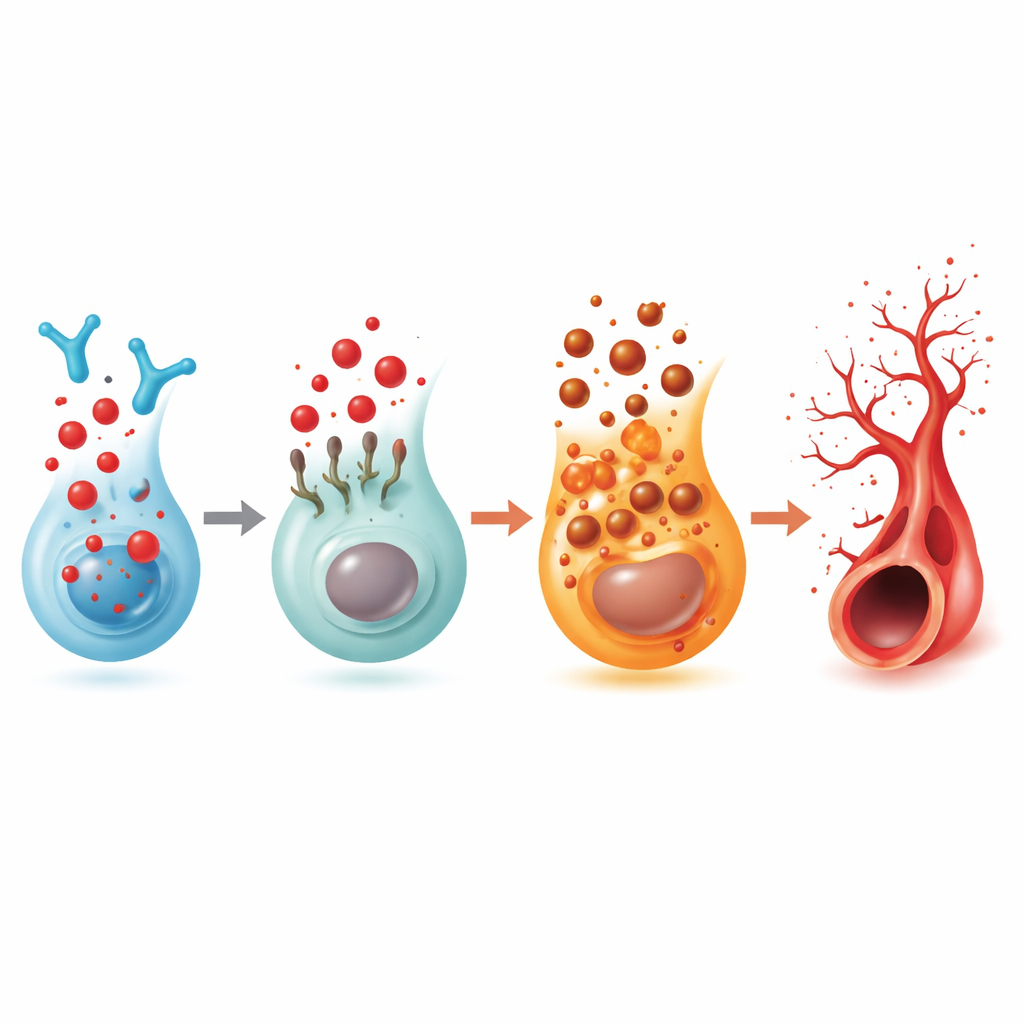
Un cambio de receptor que enlaza señales lipídicas, células inmunes y vasos
Dado que el 2‑hexadecenal procede del S1P, el equipo examinó los cinco receptores conocidos del S1P. Solo uno, llamado S1PR5, descendió de manera consistente en los ojos de los peces cuando se acumuló 2‑hexadecenal. La reducción de S1PR5 por sí sola provocó el mismo exceso de brotes y, al mismo tiempo, disminuyó FSP1, vinculando este receptor al freno de la ferroptosis. Un fármaco selectivo que activa S1PR5 restauró patrones vasculares más normales tanto en peces tratados con 2‑hexadecenal como en peces deficientes en la enzima. Trabajos biofísicos y de modelado por ordenador mostraron que el 2‑hexadecenal puede unirse directamente a S1PR5 y desencadenar su internalización en las células, debilitando su señal en la superficie. En datos humanos de retina a nivel de célula única, S1PR5 se encontró principalmente en células inmunitarias natural killer (NK), y en muestras de pacientes con retinopatía diabética avanzada, los niveles de S1PR5 eran marcadamente más altos mientras que las vías relacionadas con esfingolípidos, señalización inmune y ferroptosis estaban alteradas de forma consistente con los hallazgos en pez cebra.
Qué podría significar esto para personas con retinopatía diabética
En conjunto, el estudio dibuja una imagen sencilla pero poderosa: cuando la enzima ALDH3B1 no puede eliminar el aldehído derivado de S1P 2‑hexadecenal, este subproducto reactivo perturba la señal de S1PR5 en células inmunitarias, debilita un sistema de defensa interno contra el daño inducido por hierro y contribuye a desencadenar una forma de muerte celular «similar a la oxidación» que favorece que vasos enmarañados y frágiles invadan la retina. Dado que ya existen fármacos que actúan sobre receptores S1PR y algunos se administran por vía oral, este eje recién descrito 2‑hexadecenal–S1PR5–ferroptosis ofrece una ruta plausible hacia tratamientos futuros que podrían ralentizar o prevenir la pérdida de visión en la retinopatía diabética con menos inyecciones en el ojo.
Cita: Qian, X., Ge, R., Chu, Y. et al. Sphingosine-1-Phosphate-derived 2-Hexadecenal is a central mediator of ocular neovascularization by inhibiting Sphingosine-1-Phosphate receptor 5. Nat Commun 17, 3488 (2026). https://doi.org/10.1038/s41467-026-71792-3
Palabras clave: retinopatía diabética, vasos sanguíneos retinianos, señalización lipídica, ferroptosis, receptor de esfingosina‑1‑fosfato