Clear Sky Science · it
Il 2‑esadecenale derivato dalla sfingosina-1-fosfato è un mediatore centrale della neovascolarizzazione oculare inibendo il recettore della sfingosina-1-fosfato 5
Perché questo studio conta per la vista
La perdita della vista dovuta a malattie come la retinopatia diabetica spesso deriva dalla crescita di vasi sanguigni fragili e permeabili nella retina sul retro dell’occhio. I trattamenti attuali possono salvare la vista, ma sono costosi, invasivi e non funzionano per tutti. Questo studio individua un colpevole chimico finora nascosto e una nuova molecola bersaglio sulle cellule immunitarie che insieme guidano questa crescita vascolare dannosa, aprendo la strada a possibili terapie future più sicure e per via orale.
Un colpevole nascosto prodotto da un grasso utile
La storia inizia con un messaggero simile a un grasso chiamato sfingosina‑1‑fosfato (S1P). L’S1P normalmente aiuta a mantenere i vasi sanguigni stabili e non permeabili, e farmaci che agiscono sui suoi recettori sono già usati in malattie come la sclerosi multipla. Ma quando l’S1P viene degradato, può formare un sottoprodotto reattivo chiamato 2‑esadecenale, un piccolo aldeide instabile. Fino ad ora si sapeva poco su cosa faccia questo sottoprodotto nei vasi viventi, in particolare nell’occhio. Gli autori hanno ipotizzato che se il 2‑esadecenale non viene eliminato correttamente, potrebbe danneggiare le cellule e disturbare la fitta rete di vasi che nutre la retina sensibile alla luce.
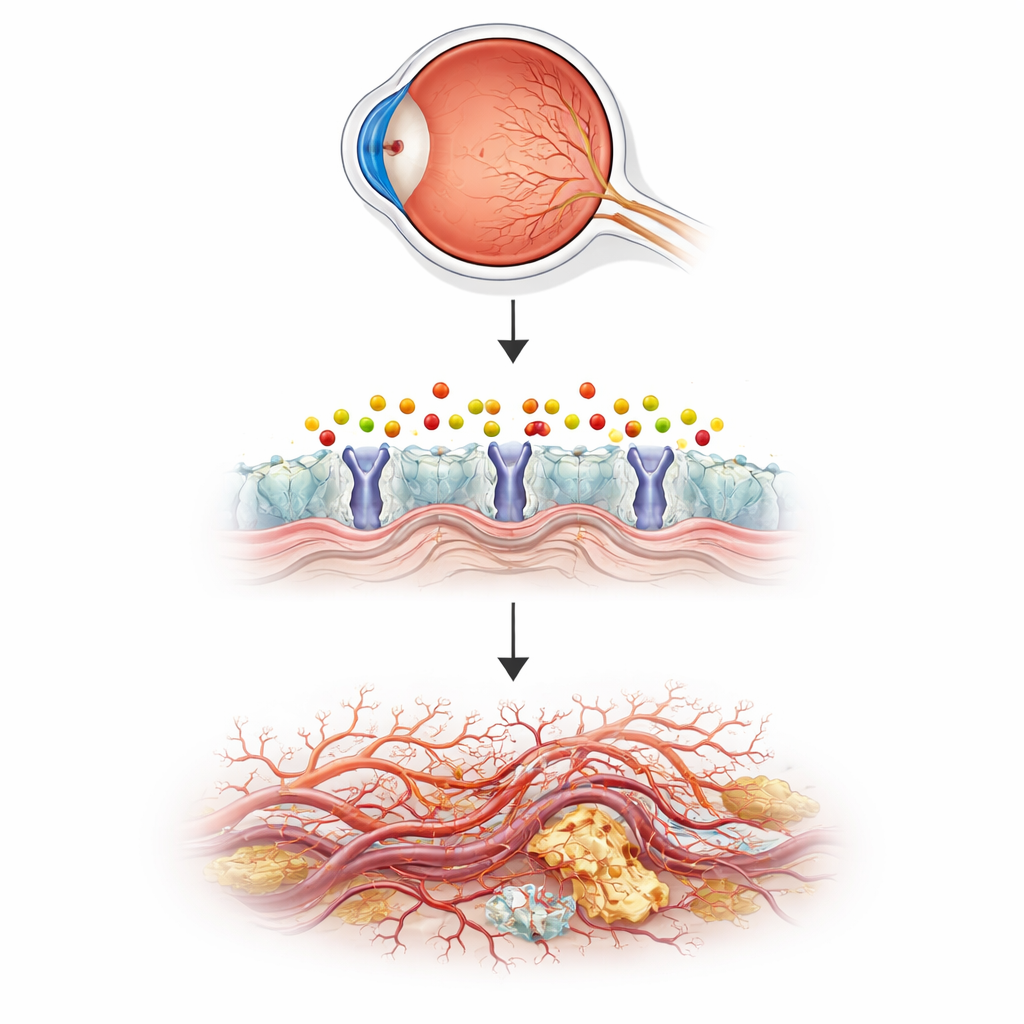
Usare piccoli pesci per modellare occhi umani malati
Per verificare questa idea, il gruppo si è rivolto al pesce zebra, un piccolo pesce d’acquario i cui embrioni trasparenti permettono agli scienziati di osservare direttamente la formazione dei vasi. Hanno disattivato un gene chiamato aldh3b1, che codifica un enzima che detossifica il 2‑esadecenale, e hanno seguito la crescita dei vasi nell’occhio. I pesci privi di questo enzima hanno sviluppato troppe sporgenze fini e ramificazioni nella retina, in uno schema simile a quello delle fasi precoci della malattia umana, mentre i vasi del corpo più grandi restavano normali. Quando pesci normali venivano semplicemente esposti al 2‑esadecenale, i loro vasi oculari crescevano eccessivamente nello stesso modo. Una molecola naturale chiamata carnosina, che può neutralizzare aldeidi reattive, ha invertito questi cambiamenti, collegando la crescita anomala all’accumulo di questa singola molecola derivata dai lipidi.
Squilibrio del ferro e una forma infuocata di morte cellulare
I ricercatori si sono poi chiesti come questa piccola molecola potesse rimodellare così potentemente i vasi. Combinando profili di attività genica e analisi chimiche dettagliate, hanno scoperto che l’eccesso di 2‑esadecenale interrompe il metabolismo del ferro nelle cellule e le spinge verso la ferroptosi, una forma di morte cellulare guidata dal ferro recentemente riconosciuta e caratterizzata da ossidazione lipidica incontrollata. Marcatori di danno lipidico e sovraccarico di ferro aumentavano negli occhi dei pesci, mentre sistemi protettivi chiave che normalmente bloccano la ferroptosi, inclusa una proteina chiamata FSP1 e l’enzima antiossidante GPX4, risultavano ridotti. Bloccare la ferroptosi con un inibitore specifico alleviava la crescita vascolare anomala, mentre bloccare direttamente FSP1 imitava i cambiamenti simili alla malattia, collocando questa via al centro del danno.
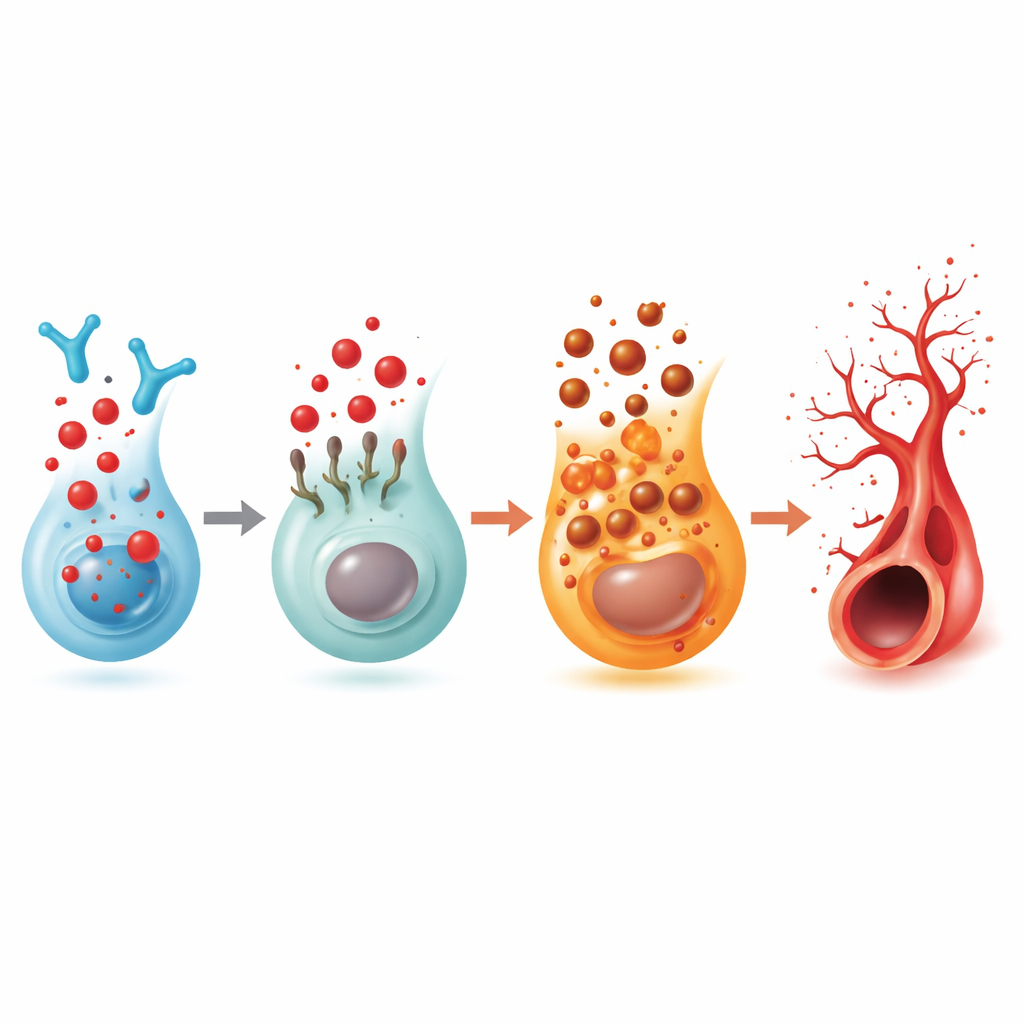
Un interruttore recettoriale che collega segnali lipidici, cellule immunitarie e vasi
Poiché il 2‑esadecenale deriva dall’S1P, il team ha esaminato i cinque recettori noti per l’S1P. Solo uno, chiamato S1PR5, diminuiva costantemente negli occhi dei pesci quando il 2‑esadecenale si accumulava. La riduzione di S1PR5 da sola causava lo stesso eccesso di sporgenze e contemporaneamente abbassava FSP1, collegando questo recettore al freno della ferroptosi. Un farmaco selettivo che attiva S1PR5 ha ristabilito modelli vascolari più normali sia nei pesci trattati con 2‑esadecenale sia in quelli carenti dell’enzima. Studi biofisici e di modellizzazione al computer hanno mostrato che il 2‑esadecenale può legarsi direttamente a S1PR5 e indurne l’internalizzazione nelle cellule, indebolendone il segnale di superficie. Nei dati umani di retina a cellula singola, S1PR5 è risultato principalmente presente sulle cellule immunitarie natural killer (NK), e in campioni di pazienti con retinopatia diabetica avanzata i livelli di S1PR5 erano marcatamente alterati mentre le vie correlate a sfingolipidi, segnalazione immunitaria e ferroptosi mostravano cambiamenti coerenti con i risultati nel pesce zebra.
Cosa potrebbe significare per le persone con retinopatia diabetica
Nel complesso, lo studio dipinge un quadro semplice ma potente: quando l’enzima ALDH3B1 non riesce a eliminare l’aldeide derivata dall’S1P, il 2‑esadecenale reattivo altera il segnale di S1PR5 sulle cellule immunitarie, indebolisce un sistema di difesa interno contro il danno guidato dal ferro e contribuisce a scatenare una forma di morte cellulare “simile alla ruggine” che favorisce l’invasione della retina da parte di vasi intricati e fragili. Poiché esistono già farmaci che modulano i recettori S1PR e alcuni sono disponibili per via orale, questo asse appena mappato 2‑esadecenale–S1PR5–ferroptosi offre una via plausibile per futuri trattamenti che potrebbero rallentare o prevenire la perdita della vista nella retinopatia diabetica con meno iniezioni intraoculari.
Citazione: Qian, X., Ge, R., Chu, Y. et al. Sphingosine-1-Phosphate-derived 2-Hexadecenal is a central mediator of ocular neovascularization by inhibiting Sphingosine-1-Phosphate receptor 5. Nat Commun 17, 3488 (2026). https://doi.org/10.1038/s41467-026-71792-3
Parole chiave: retinopatia diabetica, vasi sanguigni retinici, segnalazione lipidica, ferroptosi, recettore della sfingosina-1-fosfato