Clear Sky Science · ru
Производный сфингозин‑1‑фосфата 2‑гексадеценаль является центральным медиатором офтальмальной неоваскуляризации через ингибирование рецептора сфингозин‑1‑фосфата 5
Почему это исследование важно для зрения
Потеря зрения при таких заболеваниях, как диабетическая болезнь глаза, часто связана с ростом хрупких, проницаемых кровеносных сосудов в сетчатке. Существующие методы лечения могут сохранить зрение, но они дорогостоящи, инвазивны и не всегда эффективны. В этом исследовании обнаружен ранее не распознанный химический фактор и новая мишень на иммунных клетках, которые вместе стимулируют вредный рост сосудов — это открывает путь к более безопасным пероральным терапиям в будущем.
Скрытый «злодей», образующийся из полезного жира
История начинается с жирообразного посредника — сфингозин‑1‑фосфата (S1P). S1P обычно помогает поддерживать стабильность сосудов и их непроницаемость, и препараты, действующие на его рецепторы, уже применяются при таких заболеваниях, как рассеянный склероз. Но при разрушении S1P образуется реактивный побочный продукт — 2‑гексадеценаль, небольшой нестабильный альдегид. До сих пор почти ничего не было известно о том, как этот побочный продукт действует в живых сосудах, особенно в глазу. Авторы предположили, что если 2‑гексадеценаль не удаляется должным образом, он может повреждать клетки и нарушать тонкую сеть сосудов, питающих светочувствительную сетчатку.
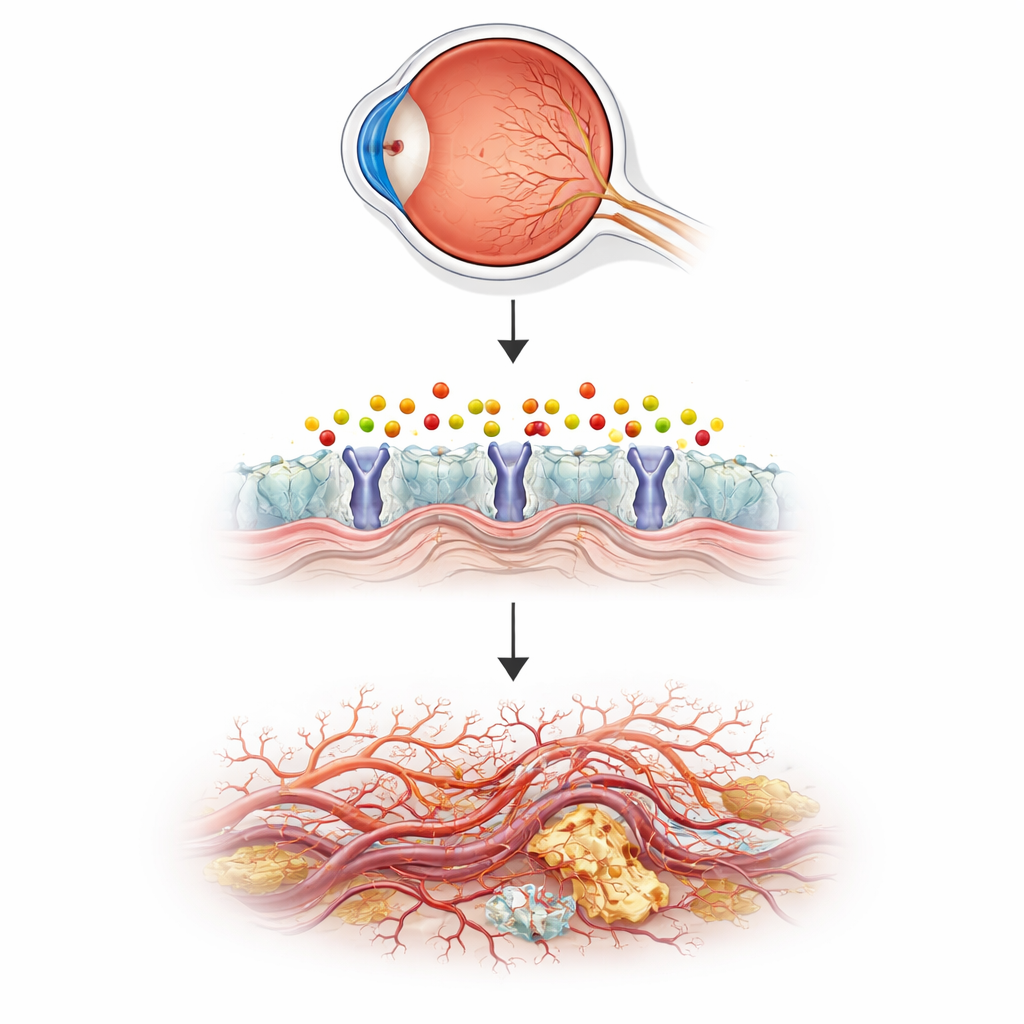
Использование мелких рыбок для моделирования больных человеческих глаз
Чтобы проверить эту гипотезу, команда обратилась к данио‑рерио (зебровой рыбке) — небольшой аквариумной рыбке с прозрачными эмбрионами, которые позволяют наблюдать за формированием сосудов в реальном времени. Они выключили ген aldh3b1, кодирующий фермент, детоксифицирующий 2‑гексадеценаль, и проследили рост сосудов в глазу. Рыбы без этого фермента развивали избыточные тонкие отростки и ветвление сосудов в сетчатке, в паттерне, схожем с ранней стадией заболевания у человека, тогда как крупные сосуды тела оставались нормальными. Когда нормальных рыб просто купали в растворе 2‑гексадеценаля, сосуды в их глазах также разрастались. Натуральная молекула карнозин, способная связывать реактивные альдегиды, обращала эти изменения, напрямую связывая аномальный рост с накоплением этого липид‑производного химического соединения.
Дисбаланс железа и «огненная» форма гибели клеток
Затем исследователи задали вопрос, как небольшая молекула может так сильно перестраивать сосудистую сеть. Комбинируя профилирование активности генов и детальный химический анализ, они обнаружили, что избыток 2‑гексадеценаля нарушает обмен железа в клетках и толкает их к ферроптозу — недавно описанной железозависимой форме клеточной смерти, характеризующейся неконтролируемой окислительной деградацией липидов. В сетчатках рыб возросли маркеры повреждения липидов и перегрузки железом, тогда как ключевые защитные механизмы, обычно препятствующие ферроптозу, включая белок FSP1 и антиоксидантный фермент GPX4, оказались подавлены. Блокирование ферроптоза специализированным ингибитором смягчало аномальный рост сосудов, тогда как прямая блокада FSP1 имитировала изменения, похожие на болезнь, что поместило этот путь в центр поражения.
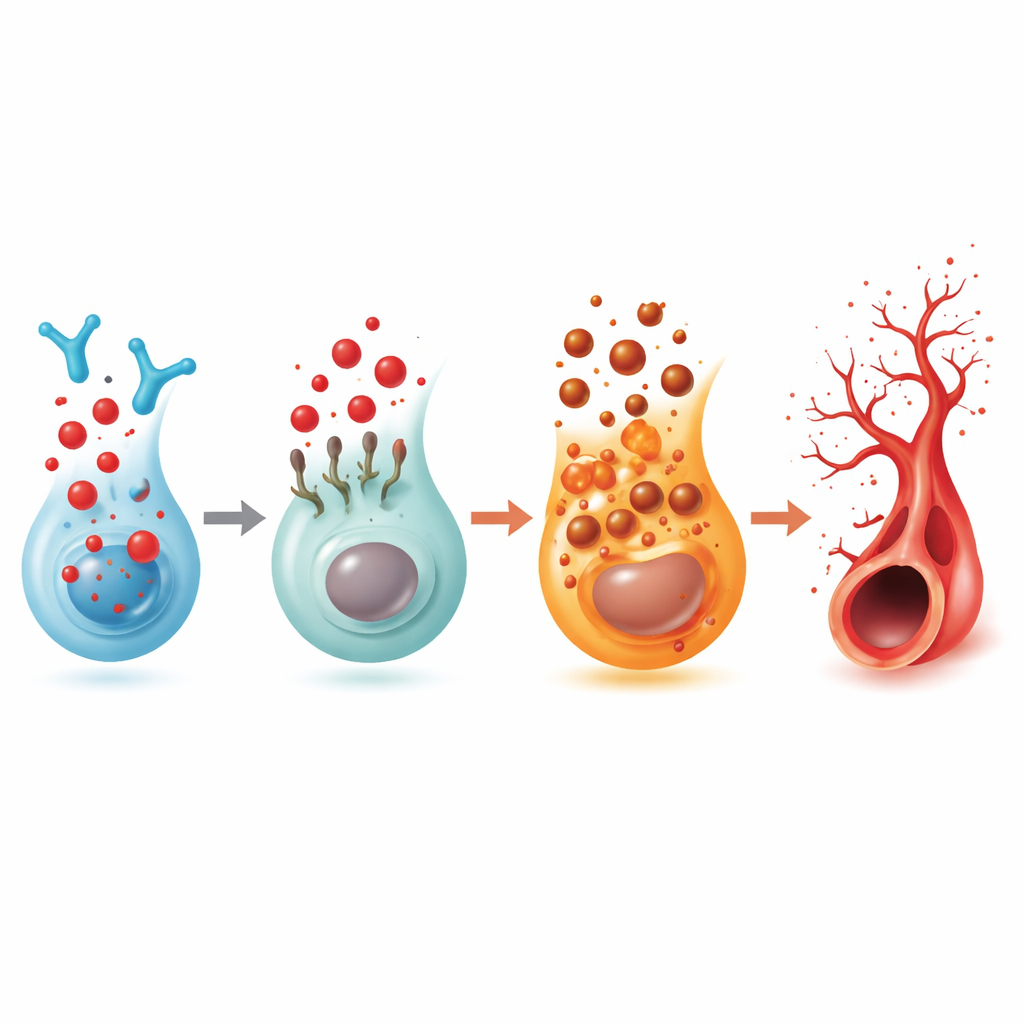
Переключатель рецептора, связывающий жировые сигналы, иммунные клетки и сосуды
Поскольку 2‑гексадеценаль образуется из S1P, команда изучила пять известных рецепторов S1P. Только один из них, S1PR5, последовательно снижался в глазах рыб при накоплении 2‑гексадеценаля. Понижение экспрессии S1PR5 само по себе вызывало тот же избыточный рост отростков и одновременно снижало уровень FSP1, связывая этот рецептор с «тормозом» ферроптоза. Селективный активатор S1PR5 восстанавливал более нормальный рисунок сосудов как у рыб, обработанных 2‑гексадеценалем, так и у животных с дефицитом фермента. Биофизические исследования и компьютерное моделирование показали, что 2‑гексадеценаль может напрямую связываться с S1PR5 и вызывать его внутреннее поглощение клеткой, ослабляя сигнал на поверхности. В данных по одно‑клеточной транскриптомике человеческой сетчатки S1PR5 обнаруживался преимущественно на натуральных киллерах (NK) — иммунных клетках, а в образцах пациентов с продвинутой диабетической ретинопатией уровни S1PR5 были заметно выше, в то время как связанные пути, включающие сфинголипиды, иммунную сигнализацию и ферроптоз, были изменены в согласии с наблюдениями у зебровых рыб.
Что это может означать для людей с диабетической болезнью глаза
В совокупности исследование рисует простую, но убедительную картину: когда фермент ALDH3B1 не способен удалять S1P‑производный альдегид 2‑гексадеценаль, этот реактивный побочный продукт нарушает сигнал S1PR5 на иммунных клетках, ослабляет внутреннюю систему защиты от железозависимого повреждения и способствует запуску формы «ржавеющей» клеточной гибели, которая стимулирует разрастание запутанных, хрупких сосудов в сетчатке. Поскольку препараты, нацеленные на рецепторы S1P, уже существуют и некоторые из них принимаются перорально, вновь описанная ось 2‑гексадеценаль–S1PR5–ферроптоз представляет собой правдоподобный путь для разработки будущих лечений, которые могли бы замедлить или предотвратить потерю зрения при диабетической ретинопатии с меньшим числом инъекций в глаз.
Цитирование: Qian, X., Ge, R., Chu, Y. et al. Sphingosine-1-Phosphate-derived 2-Hexadecenal is a central mediator of ocular neovascularization by inhibiting Sphingosine-1-Phosphate receptor 5. Nat Commun 17, 3488 (2026). https://doi.org/10.1038/s41467-026-71792-3
Ключевые слова: диабетическая ретинопатия, сосуды сетчатки, липидная сигнализация, ферроптоз, рецептор сфингозин‑1‑фосфата