Clear Sky Science · he
האלדהיד 2‑הקסאדצנאל המתקבל מספינגוזין‑1‑פוספט הוא מתווך מרכזי בנאויאנגיוגנזה עינית על‑ידי עיכוב קולטון ספינגוזין‑1‑פוספט 5
מדוע המחקר הזה חשוב לראייה
אובדן ראייה במחלות כמו מחלת העין הסוכרתית נובע לעתים קרובות מצמיחה של כלי דם שבירים ודולפים ברשתית שבאחורי העין. טיפולים קיימים יכולים להציל את הראייה, אך הם יקרים, פולשניים ולא יעילים לכל המטופלים. מחקר זה חושף גורם כימי מוסתר ומולקולת מטרה חדשה בתאי מערכת החיסון שהן יחד דוחפות צמיחה מזיקה של כלי דם, ומציעים נתיב אפשרי לטיפולים בטוחים יותר בצורת גלולה בעתיד.
בעייתן מוסתרת המתקבלת משומן מועיל
הסיפור מתחיל בשולח שומני בשם ספינגוזין‑1‑פוספט (S1P). בדרך כלל S1P מסייע לשמור על יציבות כלי הדם ולמנוע דליפות, ותכשירים הפועלים על קולטניו כבר בשימוש במחלות כמו טרשת נפוצה. אך כאשר S1P מתפרק, הוא יכול ליצור תוצר תגובתי בשם 2‑הקסאדצנאל, אלדהיד קטן ובלתי יציב. עד כה ידוע מעט מאוד על תפקידו של תוצר זה בכלי דם חיים, ובמיוחד בעין. המחברים שיערו שאם 2‑הקסאדצנאל אינו מוסר כראוי הוא עלול לפגוע בתאים ולהפר את רשת הכלים העדינה המזינה את הרשתית החשה לאור.
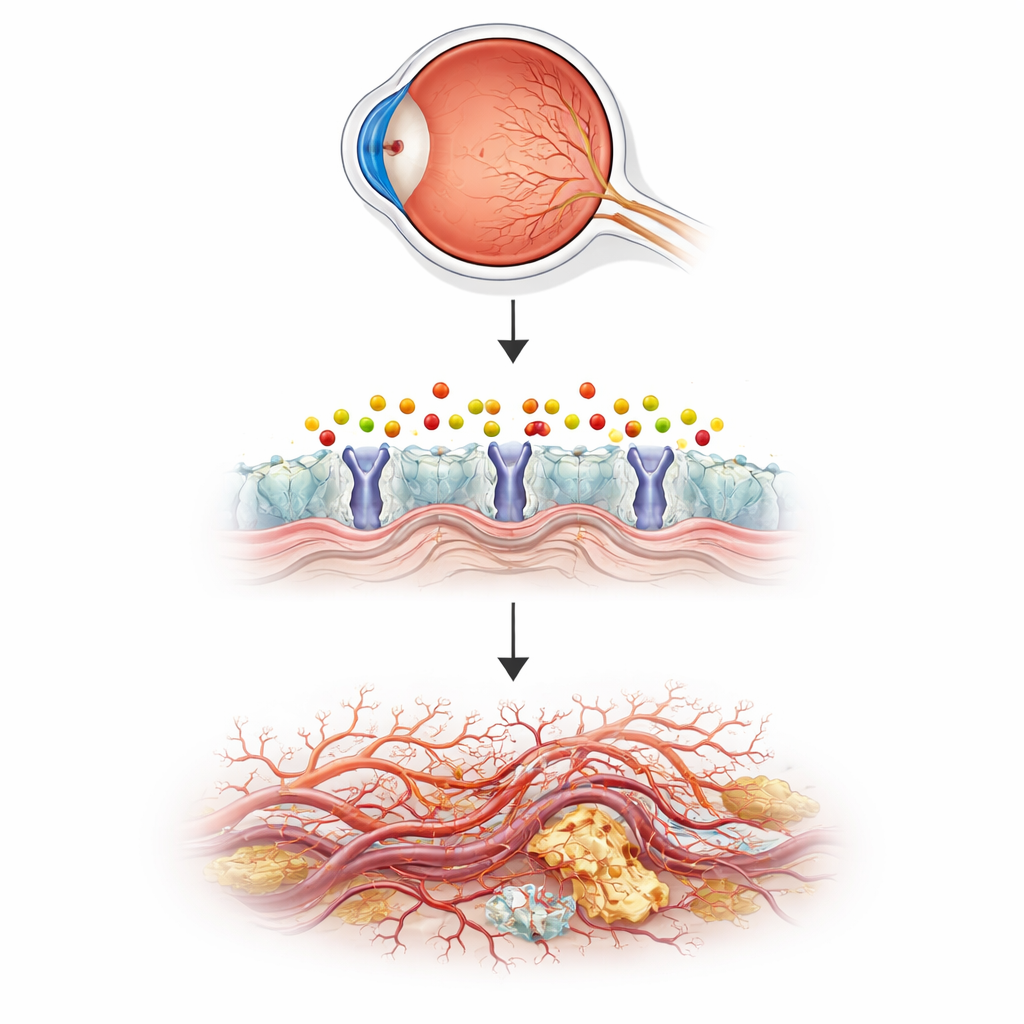
שימוש בדגים זעירים למדגם עיניים חולות של בני אדם
כדי לבחון רעיון זה פנו החוקרים לזברפים, דג קטן שאמבריוניו השקופים מאפשרים לצפות בכלי דם בזמן שהם נוצרים. הם נטרלו גן בשם aldh3b1, האחראי על ייצור אנזים שמנטרל את 2‑הקסאדצנאל, ועקבו אחר גידול כלי הדם בעין. דגים חסרי האנזים פיתחו ניצנים וסיעופים רבים מדי ברשתית, בדפוס הדומה למחלה אנושית מוקדמת, בעוד שכלי הדם הגדולים בגוף נותרו תקינים. כאשר דגי מבוגר נחשפו פשוט ל‑2‑הקסאדצנאל, כלי דמם בעיניהם גברו באותו אופן. מולקולה טבעית בשם קארנוזין, שיכולה לקשור אלדהידים תגובתיים, הפכה את השינויים האלו ובררה את הקשר הישיר בין הגידול הבלתי תקין להצטברות הכימיקל הליפידי הבודד הזה.
חוסר איזון ברזל וצורה דלקתית של מוות תאי
החוקרים שאלו אז כיצד מולקולה קטנה זו יכולה לעצב כלי דם בעוצמה כזו. בשילוב של פרופיל פעילות גנים וניתוח כימי מפורט, הם מצאו כי עודף 2‑הקסאדצנאל מפר את האופן שבו תאים מטפלים בברזל ודוחף אותם לעבר פרופטוזיס (ferroptosis), צורת מוות תאי שנוצרת על‑ידי ברזל ומתאפיינת בחמצון שומן פראי. סימנים לנזק ליפידי ולעומס ברזל עלו בעיני הדגים, בעוד שמערכות מיגון מרכזיות שברגיל מונעות פרופטוזיס — כולל החלבון FSP1 ואנזים הנוגד חמצון GPX4 — הוטלו מטה. עיכוב פרופטוזיס בעזרת מדכא ייעודי הקל על צמיחת כלי הדם הבלתי תקינה, בעוד שעיכוב ישיר של FSP1 חיקה את השינויים הדמויי‑מחלה, וממקם את הנתיב הזה במרכז הנזק.
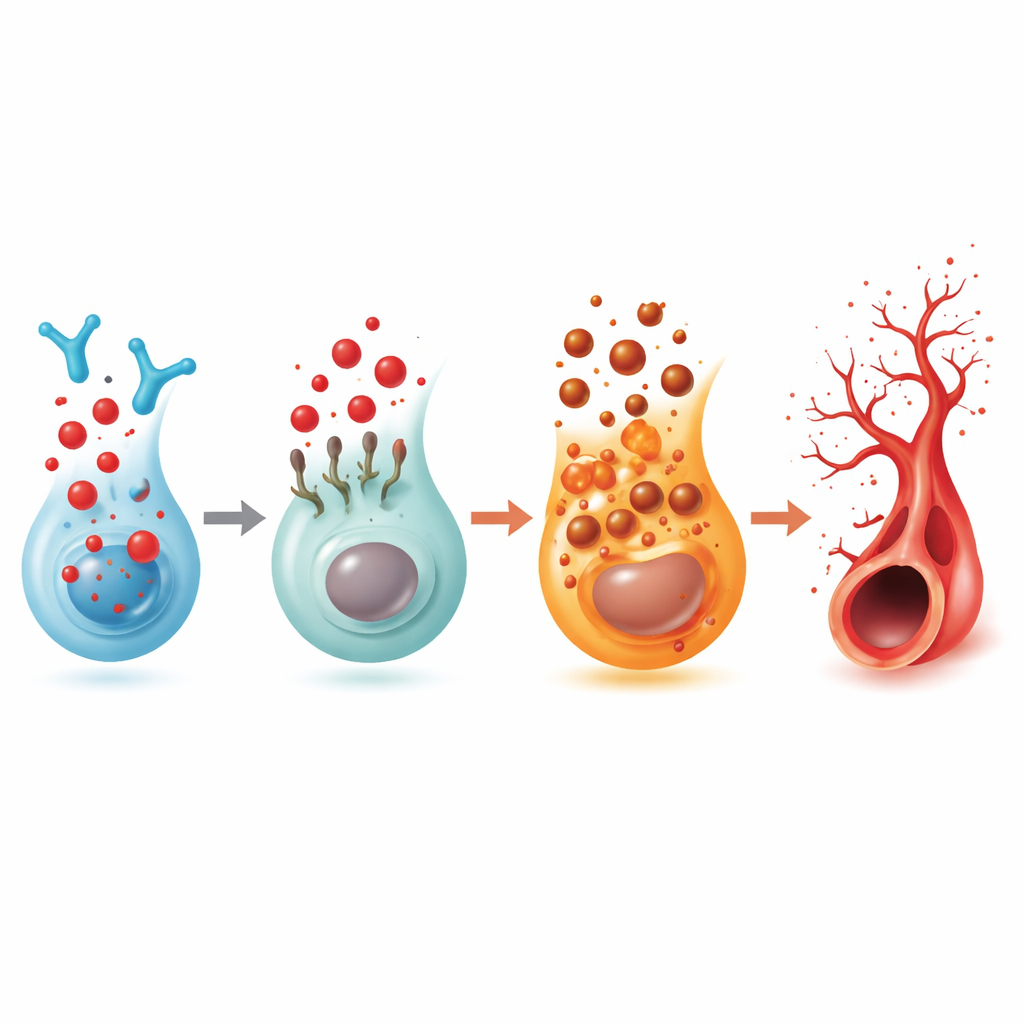
מתג קולטן שמקשר בין אותות שומניים, תאי חיסון וכלי דם
מכיוון ש‑2‑הקסאדצנאל נובע מ‑S1P, בדקו החוקרים את חמישה הקולטנים הידועים של S1P. רק אחד, שנקרא S1PR5, ירד בעקביות בעיני הדגים כשהצטבר 2‑הקסאדצנאל. הדחקה של S1PR5 לבדה גרמה לאותו ניצוח-יתר, ובאותו זמן הורידה את רמות FSP1, וקישרה את הקולטן הזה לבלם הפרופטוזיס. תרופה סלקטיבית שמפעילה את S1PR5 החזירה דפוסי כלי דם קרובים לנורמל גם בדגים שטופלו ב‑2‑הקסאדצנאל וגם בדגים חסרי האנזים. עבודות ביו‑פיזיקליות ומידול ממוחשב הראו ש‑2‑הקסאדצנאל יכול להיקשר ישירות ל‑S1PR5 ולהפעיל את פנייתו לתוך התא (internalization), מה שמחליש את האיתות שלו על המשטח. בנתוני רשתית חד‑תאיים אנושיים נמצא S1PR5 בעיקר על תאי חיסון טבעיים מסוג NK, ובמקטעים של מטופלים עם מחלת עין סוכרתית מתקדמת נמצאו רמות S1PR5 גבוהות משמעותית בעוד שדרכים קשורות בספינגוליפידים, אותות חיסוניים ופרופטוזיס השתנו באופן התואם לממצאי הזברף.
מה המשמעות עבור אנשים עם מחלת העין הסוכרתית
במבט כולל, המחקר מצייר תמונה פשוטה אך עוצמתית: כאשר האנזים ALDH3B1 אינו יכול לפנות את האלדהיד הנובע מ‑S1P, 2‑הקסאדצנאל התגובתי מופר את אות S1PR5 על תאי החיסון, מחליש מערכת הגנה פנימית מפני נזק מונע‑ברזל וגורם לצורת מוות תאי ״כמו חלודה״ שמעודדת התפשטות של כלי דם מסורבלים ושבירים לתוך הרשתית. מכיוון שכבר קיימים תכשירים הפונים אל קולטני S1P וחלקם ניתנים לנטילה, הציר החדש שצויר של 2‑הקסאדצנאל–S1PR5–פרופטוזיס מספק נתיב סביר לטיפולים עתידיים שעשויים להאט או למנוע אובדן ראייה ברטינופתיה סוכרתית עם פחות הזרקות לעין.
ציטוט: Qian, X., Ge, R., Chu, Y. et al. Sphingosine-1-Phosphate-derived 2-Hexadecenal is a central mediator of ocular neovascularization by inhibiting Sphingosine-1-Phosphate receptor 5. Nat Commun 17, 3488 (2026). https://doi.org/10.1038/s41467-026-71792-3
מילות מפתח: רטינופתיה סוכרתית, כלי דם רשתיתיים, אותות ליפידים, פרופטוזיס (ferroptosis), קולטן לספינגוזין‑1‑פוספט