Clear Sky Science · pt
2-Hexadecenal derivado da esfingosina-1-fosfato é um mediador central da neovascularização ocular ao inibir o receptor de esfingosina-1-fosfato 5
Por que este estudo importa para a visão
A perda de visão por doenças como a retinopatia diabética frequentemente decorre do crescimento de vasos sanguíneos frágeis e permeáveis na retina, na parte posterior do olho. Tratamentos atuais podem salvar a visão, mas são caros, invasivos e não funcionam para todos. Este estudo revela um agente químico antes oculto e uma nova molécula-alvo em células imunes que, em conjunto, promovem esse crescimento vascular prejudicial, abrindo um caminho possível para terapias orais mais seguras no futuro.
Um culpado oculto formado a partir de uma gordura benéfica
A história começa com um mensageiro semelhante a gordura chamado esfingosina‑1‑fosfato (S1P). Normalmente, S1P ajuda a manter os vasos sanguíneos estáveis e resistentes a vazamentos, e medicamentos que atuam em seus receptores já são usados em doenças como a esclerose múltipla. Mas quando o S1P é degradado, pode formar um subproduto reativo chamado 2‑hexadecenal, um aldeído pequeno e instável. Até agora, quase nada se sabia sobre o que esse subproduto faz em vasos sanguíneos vivos, especialmente no olho. Os autores suspeitaram que, se o 2‑hexadecenal não for eliminado corretamente, ele pode danificar células e perturbar a delicada rede de vasos que nutre a retina sensível à luz.
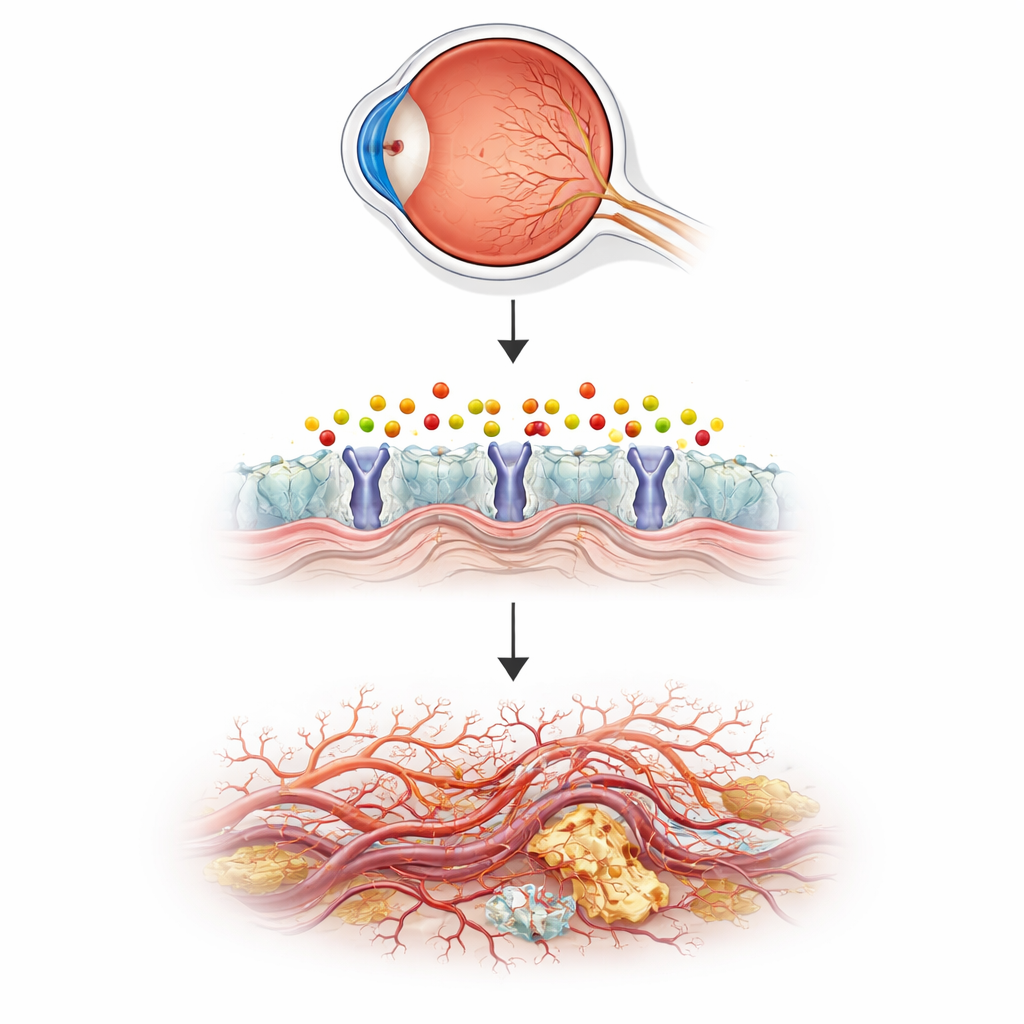
Usando peixinhos para modelar olhos humanos doentes
Para testar essa ideia, a equipe recorreu ao peixe-zebra, um pequeno peixe de aquário cujos embriões transparentes permitem observar diretamente os vasos enquanto se formam. Eles desativaram um gene chamado aldh3b1, que produz uma enzima que detoxifica o 2‑hexadecenal, e acompanharam o crescimento dos vasos no olho. Peixes que não tinham essa enzima desenvolveram brotos excessivos e ramificações finas na retina, em um padrão semelhante ao estágio inicial da doença humana, enquanto vasos maiores do corpo permaneceram normais. Quando peixes normais foram simplesmente expostos ao 2‑hexadecenal, os vasos oculares cresceram excessivamente da mesma maneira. Uma molécula natural chamada carnosina, que pode neutralizar aldeídos reativos, reverteu essas alterações, vinculando o crescimento anormal ao acúmulo desse único químico derivado de lipídio.
Desequilíbrio de ferro e uma forma inflamada de morte celular
Os pesquisadores então perguntaram como essa pequena molécula poderia remodelar os vasos de forma tão potente. Ao combinar perfis de atividade gênica e análise química detalhada, eles descobriram que o excesso de 2‑hexadecenal perturbou o manejo do ferro pelas células e as empurrou em direção à ferroptose, uma forma de morte celular dependente de ferro recentemente reconhecida, marcada por oxidação lipídica descontrolada. Marcadores de dano lipídico e sobrecarga de ferro aumentaram nos olhos dos peixes, enquanto sistemas protetores-chave que normalmente impedem a ferroptose, incluindo a proteína FSP1 e a enzima antioxidante GPX4, foram reduzidos. Bloquear a ferroptose com um inibidor especializado atenuou o crescimento vascular anômalo, enquanto bloquear diretamente a FSP1 imitou as alterações semelhantes à doença, colocando essa via no centro do dano.
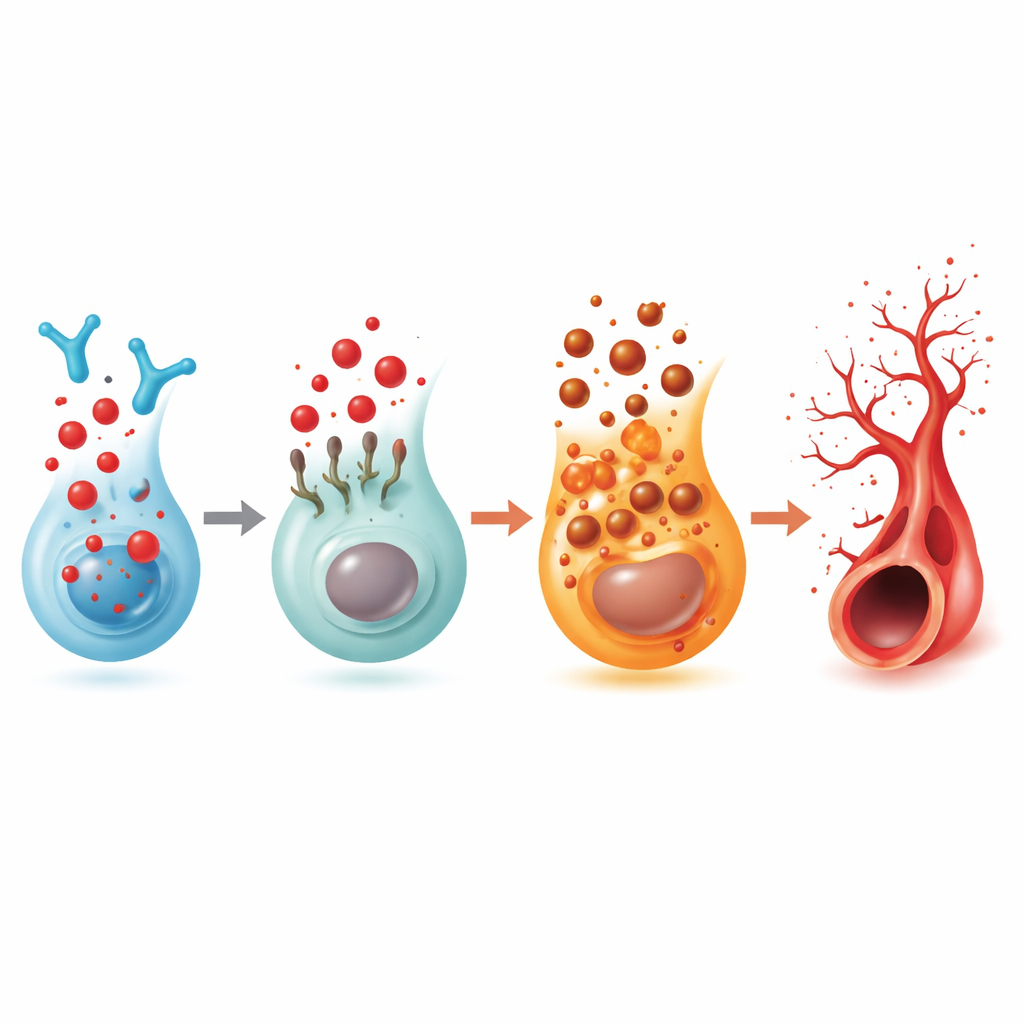
Uma troca de receptor que liga sinais lipídicos, células imunes e vasos
Como o 2‑hexadecenal deriva do S1P, a equipe examinou os cinco receptores conhecidos do S1P. Apenas um, chamado S1PR5, diminuiu consistentemente nos olhos dos peixes quando houve acúmulo de 2‑hexadecenal. Silenciar apenas o S1PR5 causou o mesmo crescimento excessivo de brotos e, ao mesmo tempo, reduziu a FSP1, ligando esse receptor ao freio da ferroptose. Um fármaco seletivo ativador do S1PR5 restaurou padrões vasculares mais normais tanto em peixes tratados com 2‑hexadecenal quanto naqueles deficientes na enzima. Trabalhos biofísicos e de modelagem computacional mostraram que o 2‑hexadecenal pode se ligar diretamente ao S1PR5 e desencadear sua internalização nas células, enfraquecendo seu sinal de superfície. Em dados humanos de retina em célula única, o S1PR5 foi encontrado principalmente em células imunes natural killer (NK), e em amostras de pacientes com retinopatia diabética avançada, os níveis de S1PR5 estavam marcadamente alterados enquanto vias relacionadas a esfingolipídios, sinalização imune e ferroptose mostraram modificações compatíveis com os achados no peixe-zebra.
O que isso pode significar para pessoas com retinopatia diabética
Em conjunto, o estudo descreve uma imagem simples, porém poderosa: quando a enzima ALDH3B1 não consegue eliminar o aldeído derivado do S1P, 2‑hexadecenal, esse subproduto reativo perturba o sinal do S1PR5 em células imunes, enfraquece um sistema de defesa interno contra danos induzidos por ferro e contribui para desencadear uma forma de morte celular “tipo ferrugem” que favorece a invasão da retina por vasos emaranhados e frágeis. Como já existem drogas que atuam em receptores S1PR e algumas são administradas por via oral, esse eixo recém-mapeado 2‑hexadecenal–S1PR5–ferroptose oferece uma rota plausível para tratamentos futuros que possam retardar ou prevenir a perda de visão na retinopatia diabética com menos injeções no olho.
Citação: Qian, X., Ge, R., Chu, Y. et al. Sphingosine-1-Phosphate-derived 2-Hexadecenal is a central mediator of ocular neovascularization by inhibiting Sphingosine-1-Phosphate receptor 5. Nat Commun 17, 3488 (2026). https://doi.org/10.1038/s41467-026-71792-3
Palavras-chave: retinopatia diabética, vasos sanguíneos da retina, sinalização lipídica, ferroptose, receptor de esfingosina-1-fosfato