Clear Sky Science · fr
Le 2‑hexadécénal dérivé du sphingosine‑1‑phosphate est un médiateur central de la néovascularisation oculaire en inhibant le récepteur Sphingosine‑1‑Phosphate 5
Pourquoi cette étude compte pour la vision
La perte de vision due à des maladies comme la rétinopathie diabétique résulte souvent de la formation de vaisseaux fragiles et perméables dans la rétine, à l’arrière de l’œil. Les traitements actuels peuvent préserver la vue, mais ils sont coûteux, invasifs et inefficaces chez certains patients. Cette étude met au jour un coupable chimique jusque‑là méconnu et une nouvelle cible moléculaire sur des cellules immunitaires qui, ensemble, favorisent cette croissance vasculaire nuisible, ouvrant la voie à d’éventuelles thérapies orales plus sûres à l’avenir.
Un fauteur de troubles caché issu d’un lipide utile
L’histoire commence par un messager lipide appelé sphingosine‑1‑phosphate (S1P). Le S1P aide normalement à maintenir les vaisseaux stables et peu perméables, et des médicaments ciblant ses récepteurs sont déjà utilisés dans des maladies comme la sclérose en plaques. Mais quand le S1P est dégradé, il peut former un sous‑produit réactif appelé 2‑hexadécénal, un petit aldéhyde instable. Jusqu’ici, on savait presque rien de ce que fait ce sous‑produit dans les vaisseaux vivants, et encore moins dans l’œil. Les auteurs ont émis l’hypothèse que, si le 2‑hexadécénal n’est pas correctement éliminé, il pourrait endommager les cellules et perturber le réseau délicat de vaisseaux qui nourrit la rétine photoréceptrice.
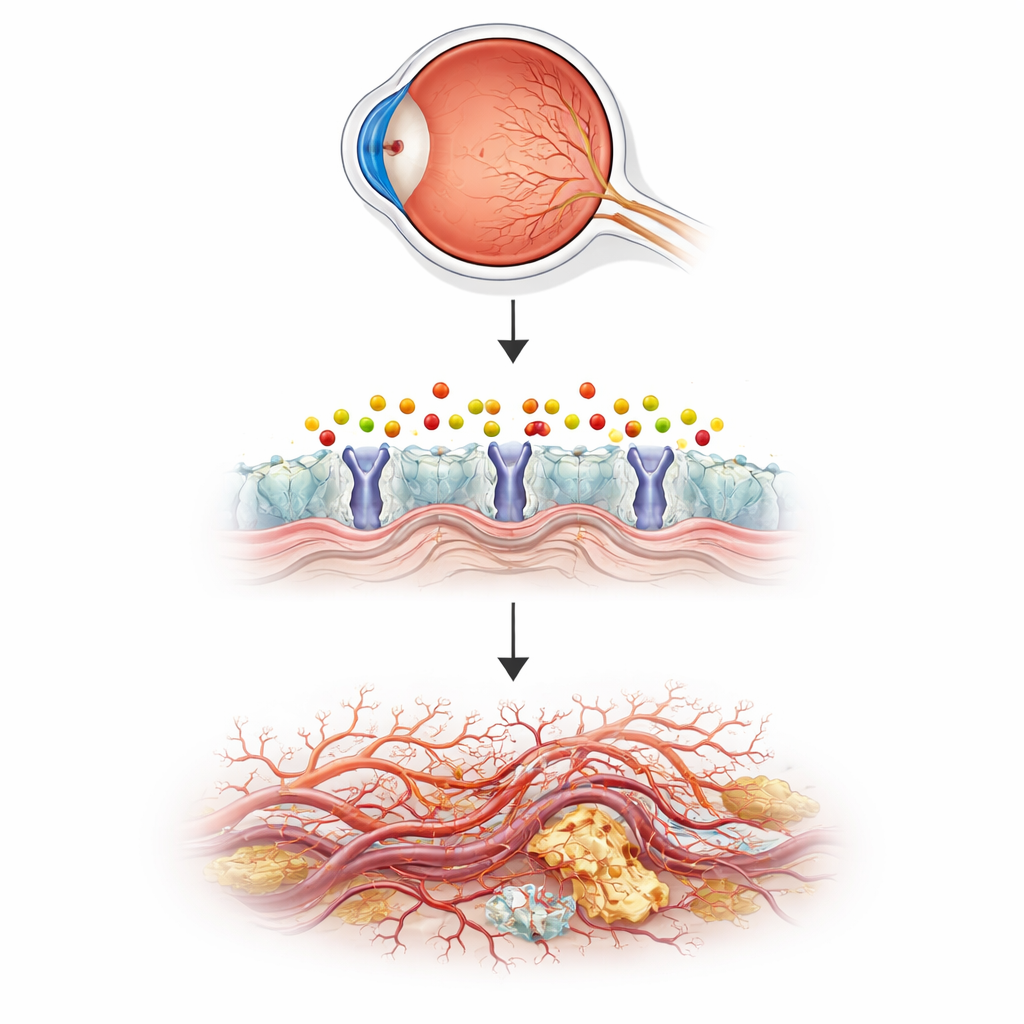
Utiliser de petits poissons pour modéliser des yeux malades humains
Pour tester cette idée, l’équipe a utilisé le poisson zèbre, un petit poisson d’aquarium dont les embryons transparents permettent d’observer directement la formation des vaisseaux. Ils ont inactivé un gène appelé aldh3b1, qui code pour une enzyme détoxifiant le 2‑hexadécénal, et suivi la croissance des vaisseaux oculaires. Les poissons privés de cette enzyme ont développé un excès de pousses fines et de ramifications dans la rétine, dans un schéma similaire aux stades précoces de la maladie humaine, tandis que les gros vaisseaux corporels restaient normaux. Lorsque des poissons normaux ont été simplement exposés au 2‑hexadécénal, leurs vaisseaux oculaires ont surcroît de la même façon. Une molécule naturelle, la carnosine, capable de piéger les aldéhydes réactifs, a inversé ces changements, reliant directement la croissance anormale à l’accumulation de cette unique molécule issue d’un lipide.
Déséquilibre du fer et une forme fulgurante de mort cellulaire
Les chercheurs se sont ensuite demandé comment cette petite molécule pouvait remodeler les vaisseaux de façon si puissante. En combinant des profils d’activité génique et une analyse chimique détaillée, ils ont constaté que l’excès de 2‑hexadécénal perturbait la gestion du fer par les cellules et les poussait vers la ferroptose, une forme de mort cellulaire dépendante du fer caractérisée par une oxydation lipidiques incontrôlée. Des marqueurs de dommages lipidiques et de surcharge en fer ont augmenté dans les yeux des poissons, tandis que des systèmes protecteurs clés qui empêchent normalement la ferroptose, notamment une protéine appelée FSP1 et l’enzyme antioxydante GPX4, étaient diminués. Bloquer la ferroptose avec un inhibiteur spécifique a atténué la croissance vasculaire anormale, tandis que l’inhibition directe de FSP1 reproduisait les changements ressemblant à la maladie, plaçant cette voie au cœur du processus délétère.
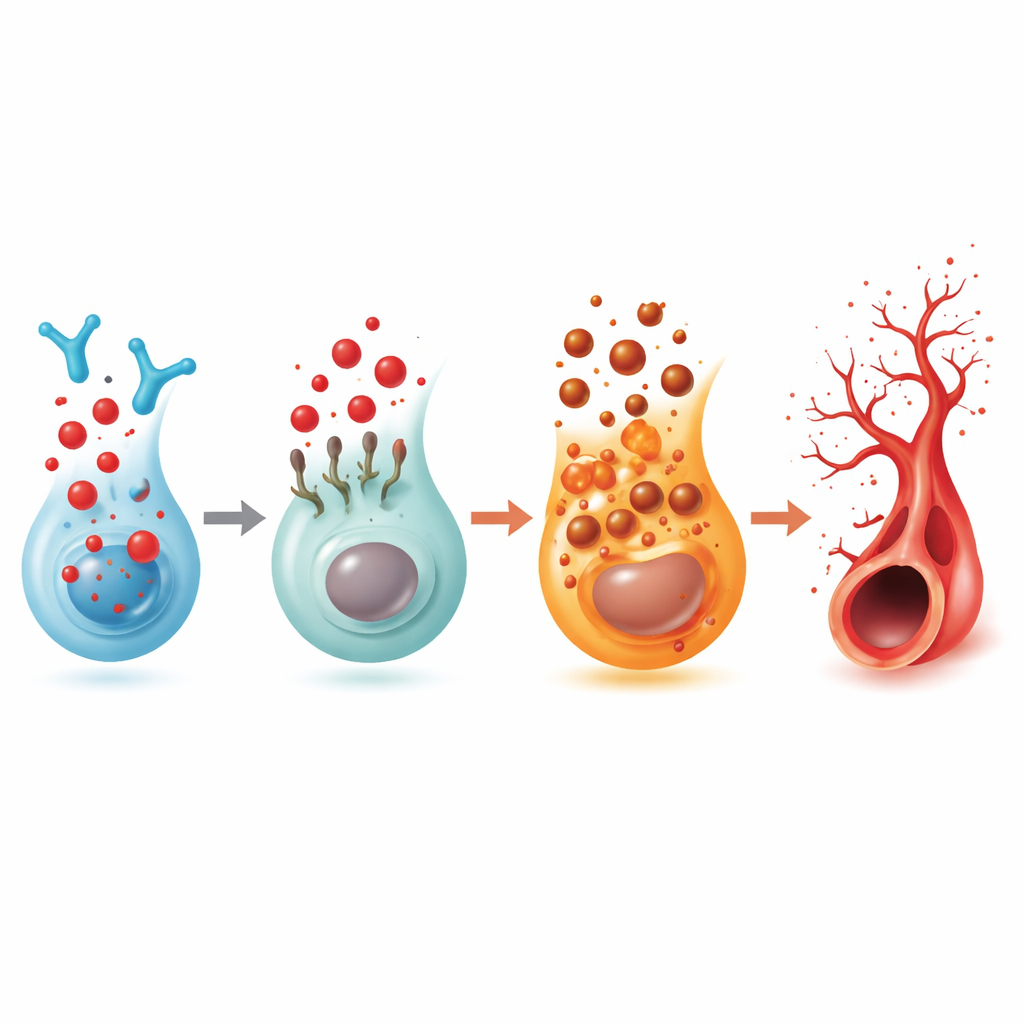
Un changement de récepteur reliant signaux lipidiques, cellules immunitaires et vaisseaux
Parce que le 2‑hexadécénal provient du S1P, l’équipe a examiné les cinq récepteurs connus du S1P. Un seul, nommé S1PR5, diminuait de façon constante dans les yeux des poissons lorsque le 2‑hexadécénal s’accumulait. L’inhibition isolée de S1PR5 provoquait la même pousse excessive et abaissait en même temps FSP1, liant ce récepteur au frein anti‑ferroptose. Un médicament sélectif activateur de S1PR5 a rétabli des motifs vasculaires plus normaux chez les poissons traités au 2‑hexadécénal et chez ceux déficients en enzyme. Des études biophysiques et de modélisation informatique ont montré que le 2‑hexadécénal peut se lier directement à S1PR5 et en déclencher l’internalisation, affaiblissant son signal de surface. Dans des données humaines de rétine en simple cellule, S1PR5 était principalement exprimé sur des cellules immunitaires de type natural killer (NK), et dans des échantillons de patients atteints de rétinopathie diabétique avancée, les niveaux de S1PR5 étaient notablement plus élevés tandis que des voies liées aux sphingolipides, à la signalisation immunitaire et à la ferroptose étaient altérées de façon cohérente avec les observations chez le poisson zèbre.
Ce que cela pourrait signifier pour les personnes atteintes de rétinopathie diabétique
Globalement, l’étude trace un scénario simple mais puissant : lorsque l’enzyme ALDH3B1 ne peut éliminer l’aldéhyde dérivé du S1P, le 2‑hexadécénal réactif perturbe le signal S1PR5 sur les cellules immunitaires, affaiblit les défenses internes contre les dommages induits par le fer et favorise une forme de mort cellulaire « rouilleuse » qui encourage l’invasion de la rétine par des vaisseaux tortueux et fragiles. Comme des médicaments ciblant les récepteurs S1PR existent déjà et que certains sont administrables par voie orale, cet axe nouvellement décrit 2‑hexadécénal–S1PR5–ferroptose offre une voie plausible vers des traitements futurs susceptibles de ralentir ou prévenir la perte de vision dans la rétinopathie diabétique, avec moins d’injections intraoculaires.
Citation: Qian, X., Ge, R., Chu, Y. et al. Sphingosine-1-Phosphate-derived 2-Hexadecenal is a central mediator of ocular neovascularization by inhibiting Sphingosine-1-Phosphate receptor 5. Nat Commun 17, 3488 (2026). https://doi.org/10.1038/s41467-026-71792-3
Mots-clés: rétinopathie diabétique, vaisseaux sanguins rétiniens, signalisation lipidique, ferroptose, récepteur du sphingosine‑1‑phosphate