Clear Sky Science · zh
复发性DNA断裂簇驱动复制应激诱导的拷贝数变异和基因组多样化
我们DNA蓝图中的隐性变化
我们体内的每个细胞在一生中要复制DNA数十亿次,大多数情况下这一过程近乎完美。但当复制机器承受压力时,DNA片段可能会丢失、重复或重排——这些变化统称为拷贝数变异。这类改变在脑部疾病和癌症中很常见,但它们最初如何产生长期以来一直是个谜。本研究揭示了一个核心罪魁:位于长神经基因中的特殊薄弱点,这些位置易发生DNA断裂,从而播下多种持久遗传改变的种子。
基因组易“裂开”的位置
研究人员关注“复发性DNA断裂簇”,即神经祖细胞中非常长的基因区域——这些细胞是分裂产生神经元的源头。此类长基因使用频繁且在细胞DNA复制计划的后期被复制,使其尤为脆弱。通过使用一种轻度抑制DNA聚合酶、诱导复制应激的药物,团队用深度全基因组测序观察基因组在哪些位置变薄。他们发现小尺度但一致的DNA丢失以及更明显的局部缺失强烈聚集在这些易碎的长神经基因区域,发生频率远高于随机预期。
从临时断裂到持久伤痕
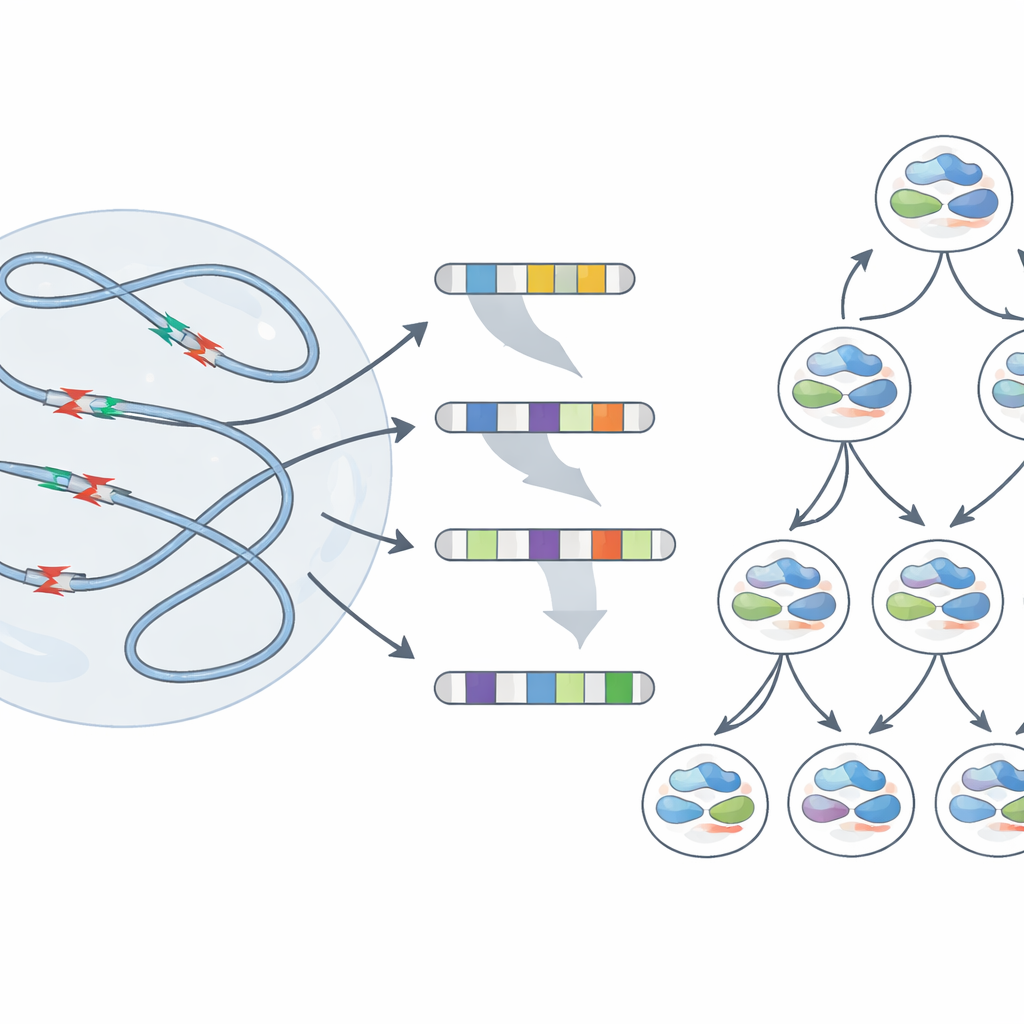
群体测序展示的是数百万细胞的平均行为,但无法揭示单个细胞内发生的情况。为了观察个体基因组在应激下的反应,团队采用了一种单细胞方法,追踪每个子代细胞继承的原始DNA链。复制应激后,许多细胞携带了跨越数百万个碱基的大缺失,甚至整条染色体臂的丢失。关键是,这些大范围改变的断点常常与先前识别的易碎区域重合。有时,来自同一个受压祖细胞的姊妹细胞最终出现截然不同的重排——这表明一次在这些热点处的损伤就能让子代细胞走上不同的遗传路径。
转录将脆弱点变成突变工厂
作者随后探究是什么使这些区域如此特殊。他们使用CRISPR工具关闭驱动两个已知存在断裂簇的大型脑基因的局部启动子和增强子(即转录开关)。当他们关闭转录时,典型的断裂簇消失了,相关的缺失在复制应激下也不再出现。值得注意的是,这些位点的DNA复制时序仍然很晚,甚至略有延迟,表明关键并非单纯复制发生的“时间”,而是活动使用与复制同时发生的组合。换言之,在复制过程中转录长基因会产生冲突区,断裂在这些区域形成,并成为拷贝数变异的起点。
修复选择决定结局
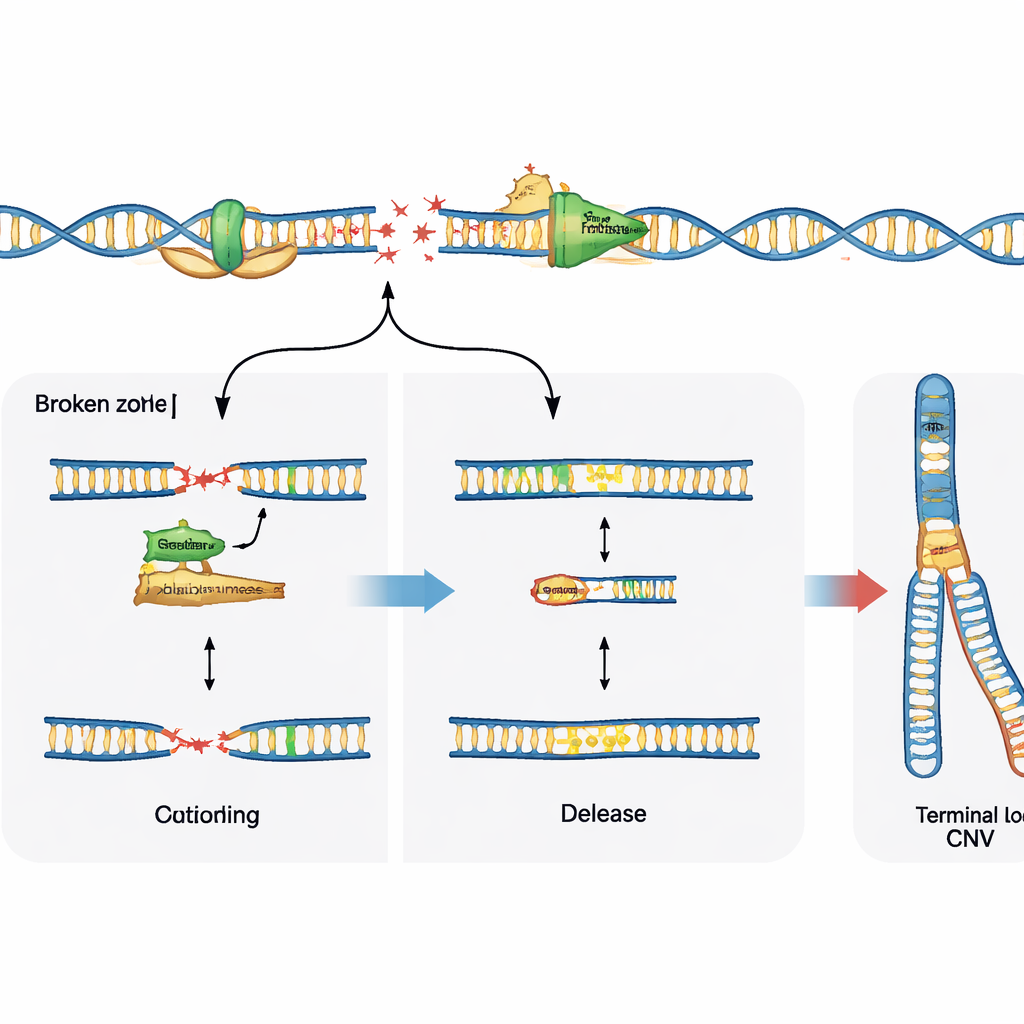
断裂只是故事的一半;细胞如何修复这些断裂决定了最终的变异模式。研究考察了一种专门酶——θ聚合酶(polymerase theta)的作用,该酶以拼接和连接破损DNA末端闻名。在缺失主要修复通路(称为非同源末端连接)的神经祖细胞中,阻断θ聚合酶显著减少了易碎位点处常见的复发性缺失,表明在这种背景下该酶积极促进拷贝数改变。相比之下,在具有完整修复系统的正常细胞中,抑制θ聚合酶并未防止这些缺失,反而暴露出更多易碎位点的原始DNA断裂。这提示θ聚合酶在其他修复选项缺失时可以推动基因组重塑,而在主修复机制存在时则可能帮助稳定复制叉并限制可见损伤。
这对脑健康和癌症意味着什么
总体而言,这项工作勾勒出一个清晰图景:在承受复制应激的神经祖细胞中,处于长且高转录活性的基因内的断裂簇充当中心枢纽,从这些枢纽既产生常见也产生罕见的拷贝数变异。这些结构性改变并非短暂;它们在子代细胞中被固定下来,有助于发育中大脑细胞基因组的多样化,并在不利条件下助长癌症的进化。通过将易碎基因区域、复制应激和特定修复通路联系起来,该研究为日常DNA复制错误与神经疾病及肿瘤中观测到的复杂结构变异模式之间搭建了一座机制性的桥梁。
引用: Corazzi, L., Ing, A., Benito, E. et al. Recurrent DNA break clusters drive replication-stress-induced copy number variants and genome diversification. Nat Commun 17, 3627 (2026). https://doi.org/10.1038/s41467-026-71790-5
关键词: 拷贝数变异, 复制应激, 神经祖细胞, DNA断裂簇, 基因组不稳定性