Clear Sky Science · ar
تجمعات متكررة لكسور الحمض النووي تقود متغيّرات عدد النسخ الناتجة عن إجهاد التضاعف وتنويع الجينوم
تغييرات خفيّة في مخطط الحمض النووي لدينا
كل خلية في أجسامنا تنسخ حمضها النووي مليارات المرّات خلال الحياة، وغالبًا ما يحدث ذلك بلا أخطاء. لكن عندما تتعرض آلية النسخ لضغط، قد تُفقد أو تُضاعف أو تُعاد ترتيب مقاطع من الحمض النووي — تغيّرات تُعرف باسم متغيّرات عدد النسخ. هذه التغيرات شائعة في اضطرابات الدماغ والسرطان، ومع ذلك ظلّ مصدرها لغزًا لفترة طويلة. تُبرز هذه الدراسة مسببًا مركزيًا: نقاط ضعف خاصة في جينات دماغية طويلة حيث تتراكم الكسور في الحمض النووي، ما يزرع مجموعة مدهشة من التغيرات الجينية الدائمة.
أين يميل الجينوم إلى التشقق
ركّز الباحثون على «تجمعات كسور الحمض النووي المتكررة»، وهي مقاطع داخل جينات طويلة جدًا في خلايا السلف العصبية — الخلايا المنقسمة التي تولّد الخلايا العصبية. تُستخدم هذه الجينات الطويلة بشكل كثيف وتُنسخ متأخرًا ضمن جدول تضاعف الحمض النووي في الخلية، مما يجعلها عرضة بشكل خاص. من خلال إبطاء بوليمرازات الحمض النووي بلطف بواسطة دواء يسبب إجهاد التضاعف، استخدم الفريق تسلسلًا عميقًا لكامل الجينوم لمراقبة أين يضعف الجينوم. وجدوا أن خسائر صغيرة ولكن متسقة في الحمض النووي، وحذفًا بؤريًا حادًا، تتركّز بقوة عند هذه المناطق المعرضة للكسور داخل الجينات العصبية الطويلة، أكثر بكثير مما يُتوقّع بالصدفة.
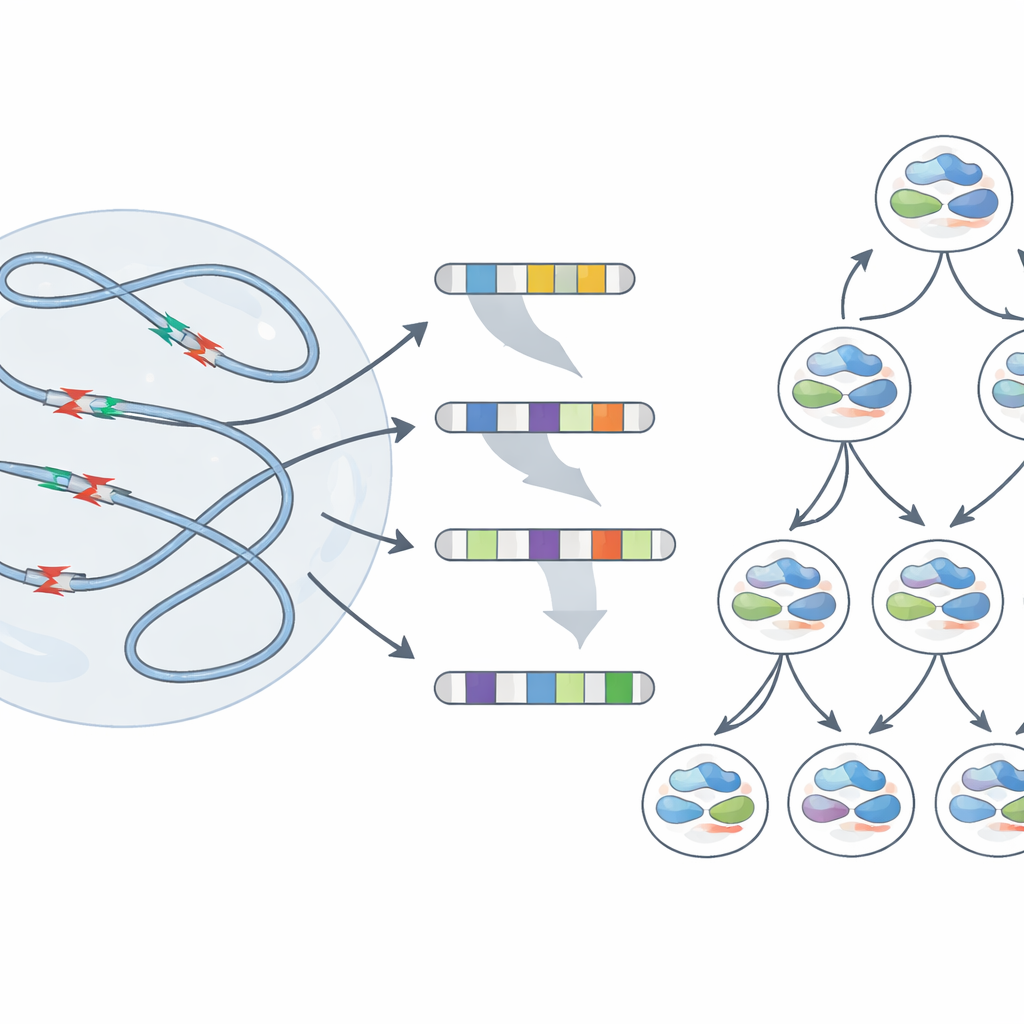
من كسور مؤقتة إلى ندوب دائمة
يُظهر التسلسل بالجملة السلوك المتوسط عبر ملايين الخلايا، لكنه لا يكشف ما يحدث في خلية مفردة. لرؤية كيف تستجيب الجينومات الفردية للإجهاد، استخدم الفريق طريقة خلوية مفردة تتتبّع أيّ سلاسل أصلية من الحمض النووي يرثها كل خلية ابنة. بعد إجهاد التضاعف، حملت العديد من الخلايا حذفًا كبيرًا يمتد على ملايين الحروف النووية وحتى خسائر لأذرع كروموسومية كاملة. والأهم أن نقاط الكسر لهذه التغيرات الكبيرة توافقت كثيرًا مع نفس المناطق الهشة المحددة سابقًا. أحيانًا، انتهت الخلايا الشقيقة الناشئة من سلف متعرض للضغط إلى إعادة ترتيبات مختلفة جدًا — دليل على أن جولة واحدة من الضرر عند هذه البؤر يمكن أن تفرّق الخلايا البنات على مسارات جينية متباينة.
النسخ يحوّل البقع الهشة إلى معامل طفرات
ثم سأل المؤلفون ما الذي يجعل هذه المناطق مميزة إلى هذا الحد. استخدموا أدوات كريسبر لإيقاف مفاتيح التشغيل المحلية (المروّجات والمعزّزات) التي تحرّك النسخ في اثنين من الجينات الدماغية العملاقة المعروفة باستضافة تجمعات الكسور. عندما أوقفوا النسخ، اختفت تجمعات الكسور المميزة، ولم تعد الحذوفات المرتبطة تظهر، حتى تحت إجهاد التضاعف. ومن الجدير بالذكر أن توقيت تضاعف الحمض النووي في تلك المواقع بقي متأخرًا أو أصبح متأخرًا قليلًا، مما يظهر أن المسألة ليست ببساطة «متى» تُنسخ هذه المناطق في دورة الخلية، بل مزيج الاستخدام النشط والنسخ. بعبارة أخرى، يؤدي نسخ جينات طويلة بينما تُنسخ أيضًا إلى خلق مناطق صراع حيث تتكوّن الكسور، وهذه الكسور هي بذور متغيّرات عدد النسخ.
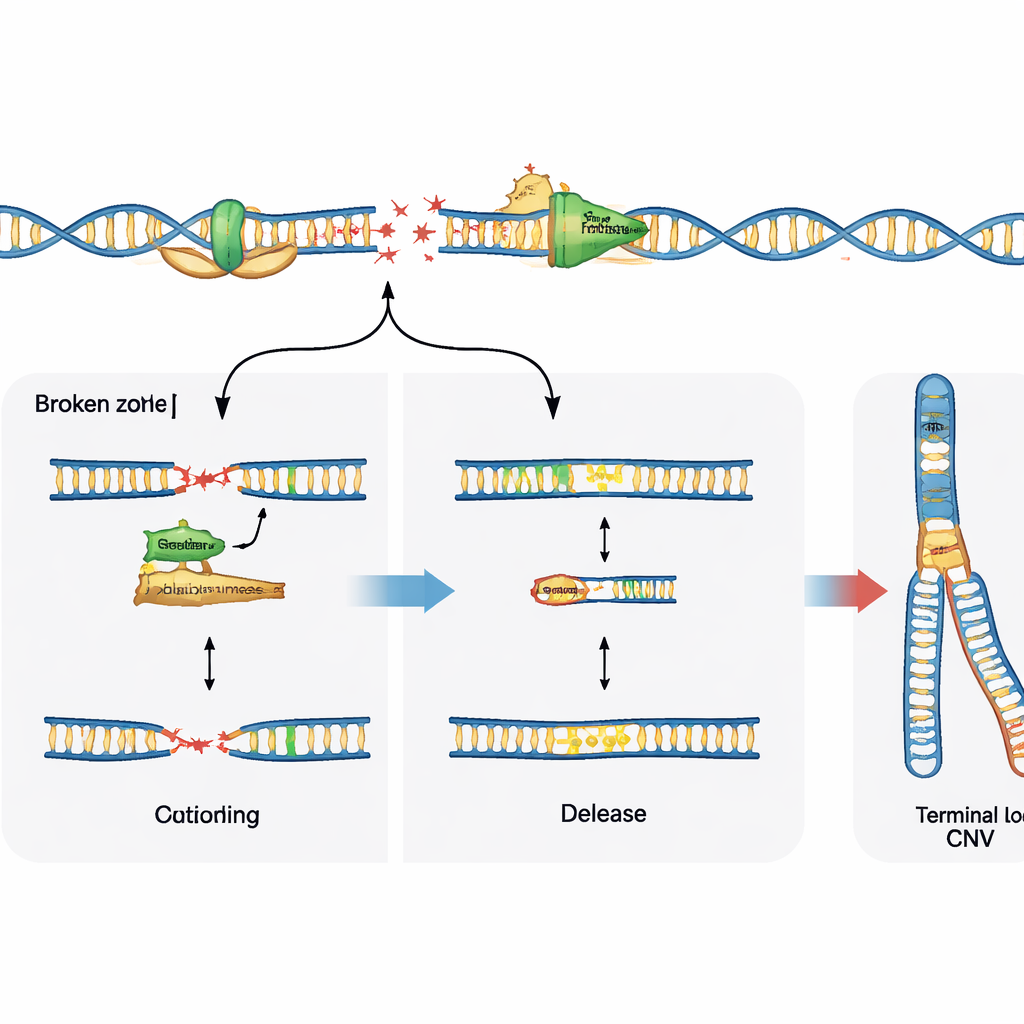
خيارات الإصلاح توجه النتيجة
كسر الحمض النووي هو نصف القصة فقط؛ كيفية إصلاح الخلية لتلك الكسور تشكّل نمط التباين النهائي. بحثت الدراسة دور إنزيم متخصص، بوليمراز ثيتا، المعروف بخياطته وربطه لنهايات الحمض النووي المكسورة. في خلايا السلف العصبية التي تفتقر إلى مسار إصلاح رئيسي يُسمى الربط غير المتجانس للنهايات، أدى حجب بوليمراز ثيتا إلى تقليل حاد للحذوفات المتكررة المعتادة عند المواقع الهشة، مما يُظهر أن الإنزيم في هذا السياق يروّج بنشاط لتغيرات عدد النسخ. في المقابل، في الخلايا الطبيعية ذات أنظمة الإصلاح السليمة، لم يمنع تثبيط بوليمراز ثيتا هذه الحذوفات بل كشف بدلًا من ذلك عن مزيد من الكسور الخام في المواقع الهشة. يشير ذلك إلى أن بوليمراز ثيتا يمكن أن يدفع إعادة تشكيل الجينوم عندما تكون الخيارات الإصلاحية الأخرى مفقودة، أو يساعد على استقرار شوكات النسخ والحدّ من الضرر المرئي عندما تكون آليات الإصلاح الرئيسية موجودة.
لماذا هذا مهم لصحة الدماغ والسرطان
مجتمعة، ترسم الدراسة صورة واضحة: في خلايا السلف العصبية تحت إجهاد التضاعف، تعمل الكسور المتجمعة في جينات طويلة ونشيطة كمحاور مركزية تنطلق منها متغيّرات عدد النسخ الشائعة والنادرة على حد سواء. هذه التغيرات الهيكلية ليست عابرة؛ إنها تثبت في الخلايا البنات، مما يساعد على تنويع جينومات الخلايا في الدماغ النامي وتحت ظروف خاطئة يغذي تطور السرطان. بربط المناطق الجينية الهشة وإجهاد التضاعف ومسارات الإصلاح المحددة، تقدم الدراسة جسرًا آليًا بين أخطاء نسخ الحمض النووي اليومية والأنماط المعقّدة للتباين البنيوي المرصودة في الأمراض العصبية والأورام.
الاستشهاد: Corazzi, L., Ing, A., Benito, E. et al. Recurrent DNA break clusters drive replication-stress-induced copy number variants and genome diversification. Nat Commun 17, 3627 (2026). https://doi.org/10.1038/s41467-026-71790-5
الكلمات المفتاحية: متغيّرات عدد النسخ, إجهاد التضاعف, خلايا السلف العصبية, تجمعات كسور الحمض النووي, عدم استقرار الجينوم