Clear Sky Science · sv
Återkommande DNA‑brytkluster driver replikationsstress‑inducerade kopiantalsvarianter och genomsbaserad diversifiering
Dolda förändringar i vår DNA‑ritning
Varje cell i vår kropp kopierar sitt DNA miljarder gånger under en livstid, och oftast sker detta felfritt. Men när kopieringsmaskineriet belastas kan DNA‑bitar gå förlorade, dupliceras eller omarrangeras — förändringar som kallas kopiantalsvarianter. Dessa förändringar är vanliga vid hjärnsjukdomar och cancer, men hur de uppstår har länge varit oklart. Denna studie identifierar en central bov: särskilda svaga punkter i långa hjärngen som tenderar att samla DNA‑brott, och som så fröar en förvånansvärd mångfald av permanenta genetiska förändringar.
Var genomet tenderar att spricka
Forskarna fokuserade på ”återkommande DNA‑brytkluster”, områden inom mycket långa gener i neuronala progenitorceller — de delande cellerna som ger upphov till nervceller. Dessa långa gener används intensivt och kopieras sent under cellens DNA‑replikationsschema, vilket gör dem särskilt utsatta. Genom att försiktigt bromsa DNA‑polymeraser med ett läkemedel som inducerar replikationsstress använde teamet djup helgenomsekvensering för att se var genomet tunnades ut. De fann att små men konsekventa förluster av DNA, och skarpare, fokala deletioner, var starkt koncentrerade till dessa brottkänsliga regioner inom långa neurala gener — betydligt oftare än vad som kan förväntas av en slump.
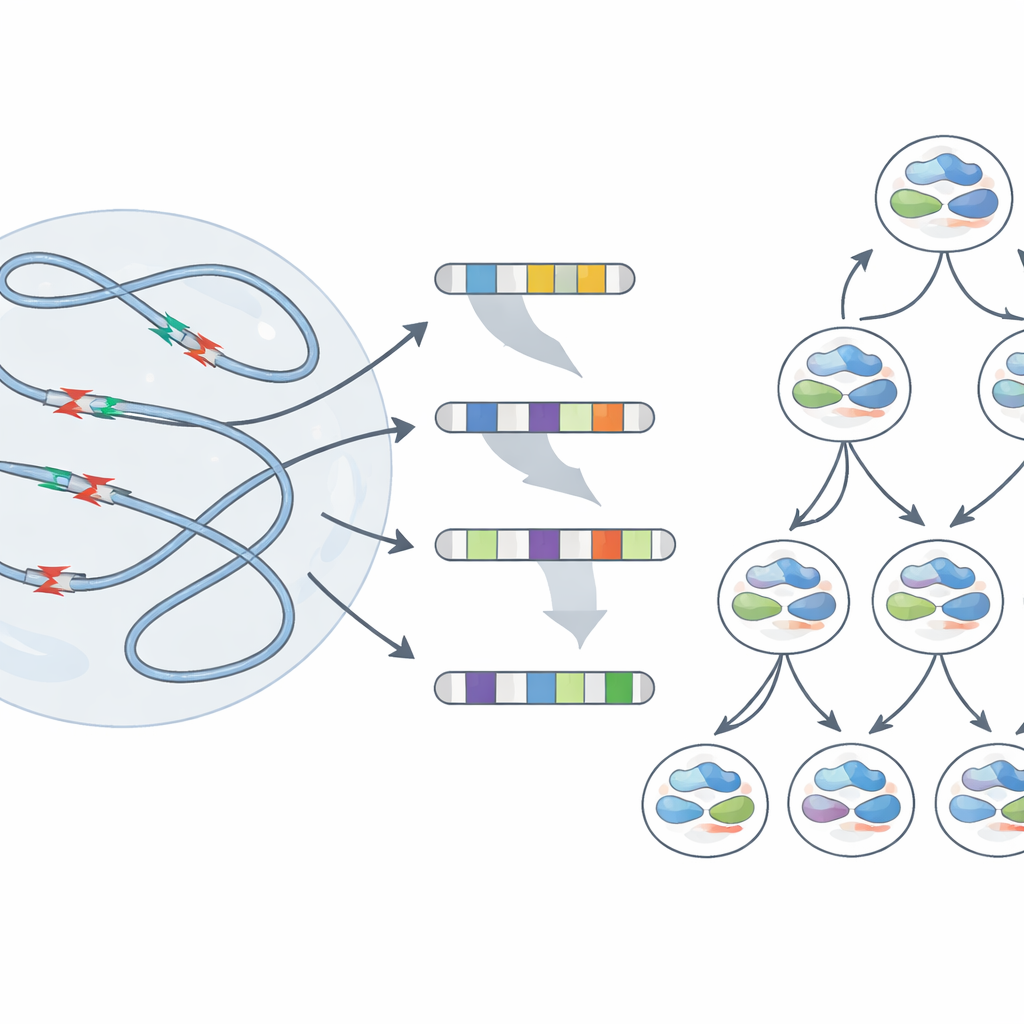
Från tillfälliga brott till bestående ärr
Populationsekvensering visar genomsnittligt beteende över miljontals celler, men avslöjar inte vad som händer i en enskild cell. För att se hur individuella genom reagerar på stress använde teamet en enkelcellsmetod som spårar vilka ursprungliga DNA‑strängar varje dottercell ärver. Efter replikationsstress bar många celler stora deletioner som sträckte sig över miljoner DNA‑bokstäver och till och med förluster av hela kromosomarmar. Viktigt var att brytpunkterna för dessa stora förändringar ofta låg i linje med samma sköra regioner som identifierats tidigare. Ibland fick systerceller som härstammade från en stressad förfader mycket olika omarrangemang — ett bevis på att en enda omgång skada vid dessa hotspot‑ställen kan sätta dotterceller på skilda genetiska banor.
Transkription förvandlar sköra platser till mutationsfabriker
Författarna frågade sedan vad som gör dessa regioner så speciella. De använde CRISPR‑verktyg för att stänga av lokala på‑switchar (promotorer och enhancers) som driver transkription av två jättelika hjärngener kända för att hysa brytkluster. När de stängde av transkriptionen försvann de karakteristiska brytklustren, och de associerade deletionerna uppträdde inte längre, inte ens under replikationsstress. Anmärkningsvärt var att tidpunkten för DNA‑replikation på dessa platser förblev sen eller blev något senare, vilket visar att det inte bara är ”när” i cellcykeln som dessa regioner kopieras som spelar roll, utan kombinationen av aktiv användning och kopiering. Med andra ord skapar samtidig transkription av långa gener och deras replikation konflikzones där brott bildas, och dessa brott är fröna till kopiantalsvarianter.
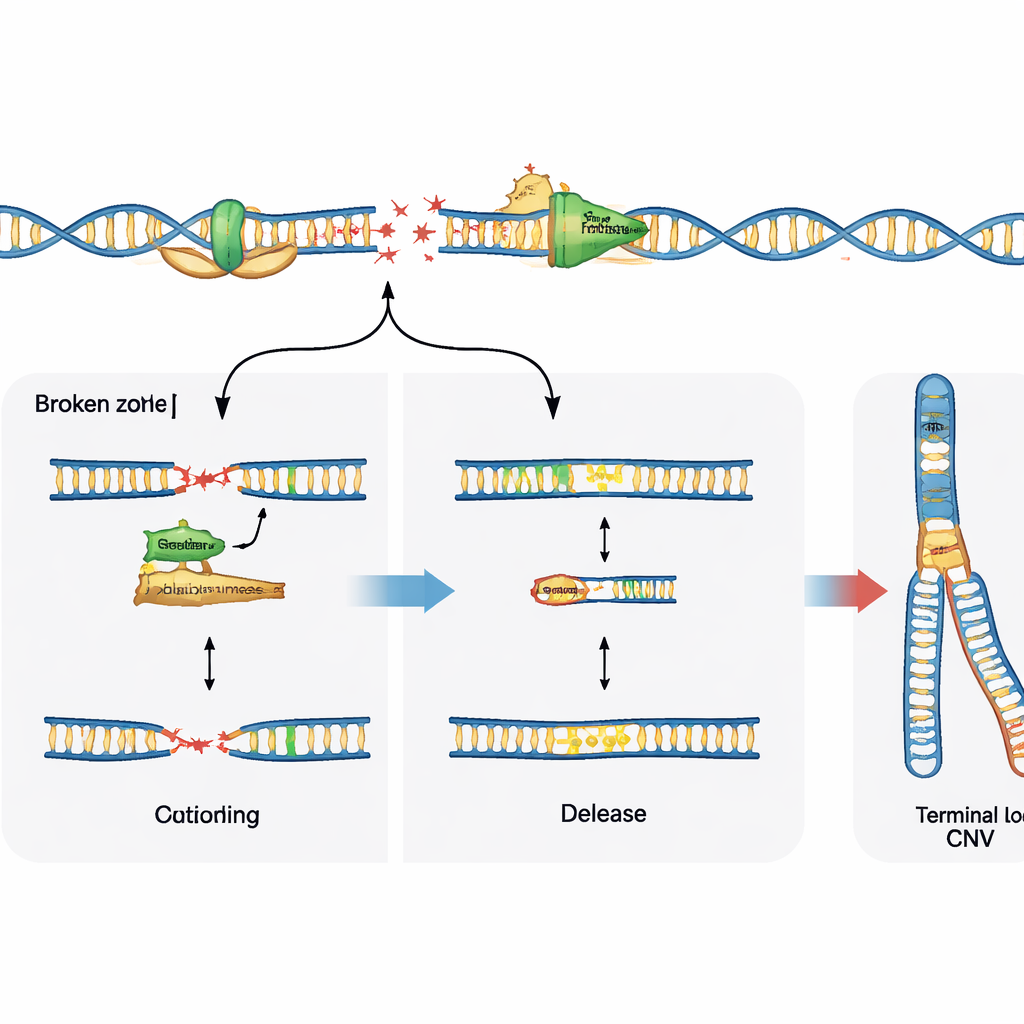
Reparationsval styr resultatet
Att DNA bryts är bara halva historien; hur cellen reparerar dessa brott formar det slutliga variationsmönstret. Studien undersökte rollen för ett specialiserat enzym, polymeras theta, som är känt för att lappa ihop och förena brutna DNA‑ändar. I neuronala progenitorceller som saknar en huvudväg för reparation kallad icke‑homolog ändläggning (non‑homologous end joining) minskade blockering av polymeras theta kraftigt de vanliga återkommande deletionerna vid de sköra platserna, vilket visar att enzymet i denna kontext aktivt främjar kopiantalsförändringar. I kontrast, i normala celler med intakta reparationssystem förhindrade inte inhibering av polymeras theta dessa deletioner utan blottlade istället fler råa DNA‑brott vid de sköra platserna. Detta tyder på att polymeras theta antingen kan driva omformning av genomet när andra reparationsalternativ saknas, eller hjälpa till att stabilisera gafflar och begränsa synlig skada när huvudreparationsmaskineriet är närvarande.
Varför detta är viktigt för hjärnhälsa och cancer
Tillsammans skildrar arbetet en tydlig bild: i neuronala progenitorceller under replikationsstress fungerar klustrade brott i långa, aktivt använda gener som centrala nav varifrån både vanliga och sällsynta kopiantalsvarianter uppstår. Dessa strukturella förändringar är inte flyktiga; de blir fixerade i dotterceller och bidrar till att diversifiera genomen hos celler i den utvecklande hjärnan och, under ogynnsamma förhållanden, att föda cancerutveckling. Genom att knyta samman sköra genregioner, replikationsstress och specifika reparationsvägar erbjuder studien en mekanistisk bro mellan vardagliga fel i DNA‑kopiering och de komplexa mönster av strukturell variation som ses vid neurologisk sjukdom och tumörer.
Citering: Corazzi, L., Ing, A., Benito, E. et al. Recurrent DNA break clusters drive replication-stress-induced copy number variants and genome diversification. Nat Commun 17, 3627 (2026). https://doi.org/10.1038/s41467-026-71790-5
Nyckelord: kopiantalsvarianter, replikationsstress, neuronala progenitorceller, DNA‑brytkluster, genomstabilitet