Clear Sky Science · de
Rekurrente DNA-Bruch‑Cluster treiben durch Replikationsstress ausgelöste Kopienzahlvarianten und Genomdiversifizierung voran
Verborgene Veränderungen in unserem DNA‑Bauplan
Jede Zelle unseres Körpers kopiert ihre DNA im Laufe des Lebens Milliarden von Malen, und meist geschieht dies fehlerfrei. Wenn die Kopiermaschine jedoch belastet ist, können DNA‑Stücke verloren gehen, dupliziert oder umgeordnet werden — Veränderungen, die als Kopienzahlvarianten bezeichnet werden. Solche Alterationen sind in Hirnerkrankungen und Krebs weit verbreitet, doch wie sie ursprünglich entstehen, war lange unklar. Diese Studie zeigt eine zentrale Ursache auf: besonders anfällige Stellen in sehr langen Hirngenen, an denen DNA‑Brüche gehäuft auftreten und die eine überraschende Vielfalt dauerhafter genetischer Veränderungen initiieren.
Wo das Genom zu reißen droht
Die Forschenden konzentrierten sich auf „rekurrente DNA‑Bruch‑Cluster“, Abschnitte innerhalb sehr langer Gene in neuralen Vorläuferzellen — den teilenden Zellen, aus denen Neurone entstehen. Diese langen Gene werden stark genutzt und spät im Zeitplan der DNA‑Replikation kopiert, wodurch sie besonders verwundbar sind. Durch eine leichte Verlangsamung der DNA‑Polymerasen mit einem Wirkstoff, der Replikationsstress erzeugt, nutzte das Team tiefgehende Ganzgenomsequenzierung, um zu beobachten, wo das Genom dünner wurde. Sie fanden, dass kleine, aber konsistente DNA‑Verluste und schärfere, fokale Deletionen stark an diesen bruchanfälligen Regionen innerhalb langer neuronaler Gene konzentriert waren — weitaus häufiger, als durch Zufall zu erwarten wäre.
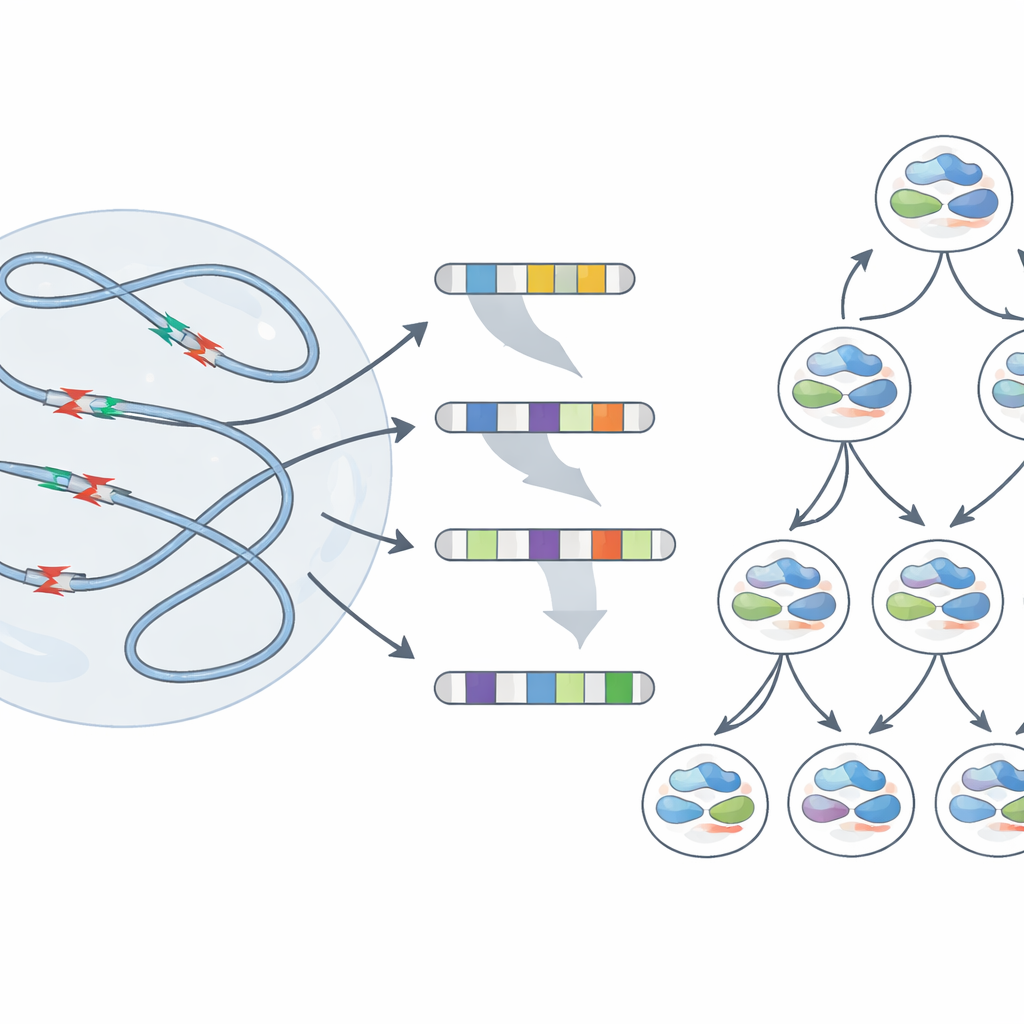
Von vorübergehenden Brüchen zu bleibenden Narben
Bulk‑Sequenzierung zeigt das durchschnittliche Verhalten von Millionen Zellen, offenbart aber nicht, was in einer einzelnen Zelle geschieht. Um zu sehen, wie einzelne Genome auf Stress reagieren, verwendete das Team eine Einzelzellmethode, die verfolgt, welche ursprünglichen DNA‑Stränge jede Tochterzelle erbt. Nach Replikationsstress trugen viele Zellen große Deletionen, die sich über Millionen von DNA‑Basen erstreckten, und sogar Verluste ganzer Chromosomenarme. Entscheidend war, dass die Bruchpunkte dieser großen Veränderungen häufig mit denselben fragilen Regionen übereinstimmten, die zuvor identifiziert worden waren. Manchmal erhielten Schwesterzellen, die von einem gestressten Vorfahren abstammen, sehr unterschiedliche Umordnungen — ein Beleg dafür, dass eine einzige Schadensrunde an diesen Hotspots Tochterzellen auf unterschiedliche genetische Wege bringen kann.
Transkription verwandelt fragile Stellen in Mutationsfabriken
Die Autoren fragten dann, was diese Regionen so besonders macht. Sie nutzten CRISPR‑Werkzeuge, um die lokalen Ein-/Ausschalter (Promotoren und Enhancer) auszuschalten, die die Transkription von zwei riesigen Hirngenen steuern, die als Wirte für Bruch‑Cluster bekannt sind. Als sie die Transkription ausschalteten, verschwanden die charakteristischen Bruch‑Cluster und die damit verbundenen Deletionen traten nicht mehr auf — selbst unter Replikationsstress. Bemerkenswerterweise blieb das Replikationszeitfenster an diesen Stellen spät oder wurde sogar geringfügig später, was zeigt, dass nicht allein das „Wann“ im Zellzyklus entscheidend ist, sondern die Kombination aus aktiver Nutzung und Kopieren. Anders ausgedrückt: Die gleichzeitige Transkription langer Gene während ihrer Replikation schafft Konfliktzonen, in denen Brüche entstehen, und diese Brüche sind die Keimzellen von Kopienzahlvarianten.
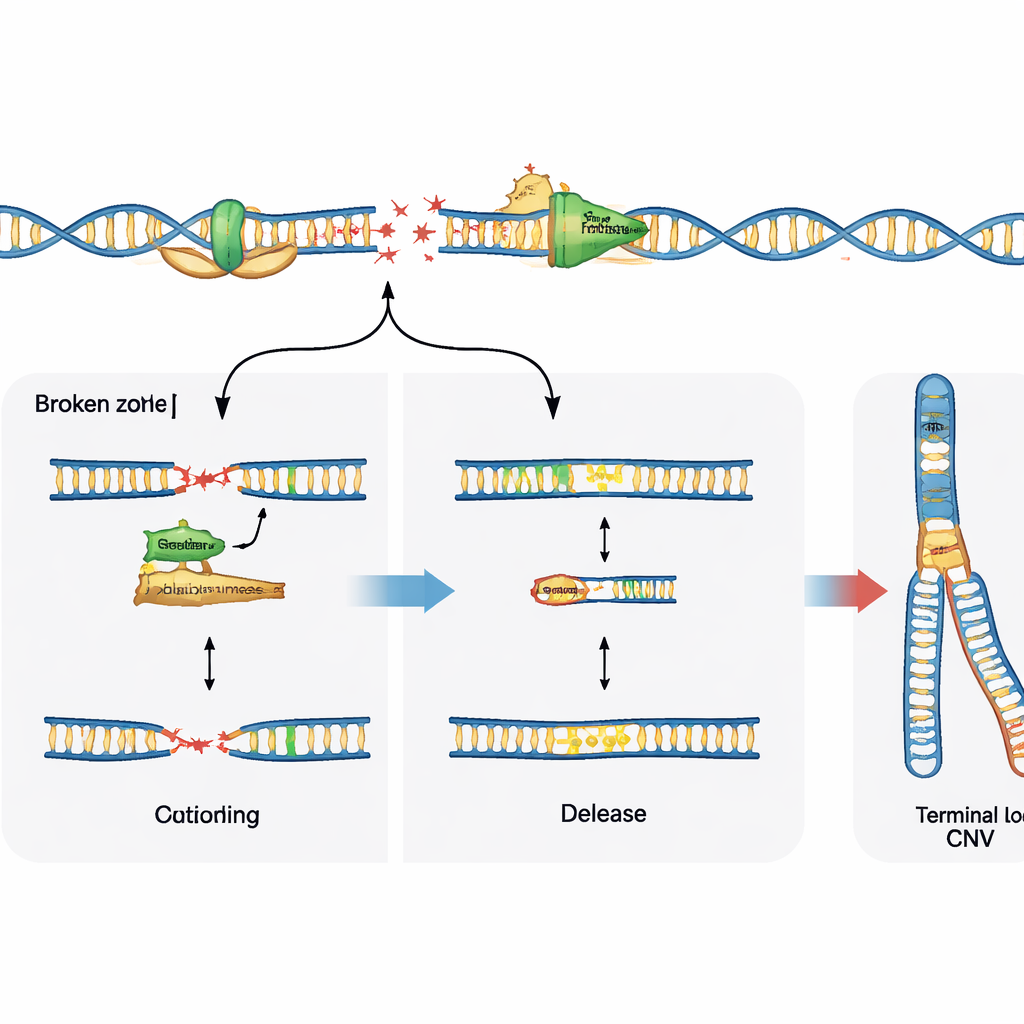
Reparaturentscheidungen bestimmen das Ergebnis
DNA‑Brüche sind nur die halbe Geschichte; wie die Zelle diese Brüche repariert, prägt das endgültige Muster der Variation. Die Studie untersuchte die Rolle eines spezialisierten Enzyms, der Polymerase theta, das dafür bekannt ist, gebrochene DNA‑Enden zu flicken und zusammenzufügen. In neuralen Vorläuferzellen, denen ein wichtiger Reparaturweg namens nicht‑homologe End‑Verknüpfung fehlt, reduzierte die Blockade der Polymerase theta die üblichen rekurrenten Deletionen an fragilen Stellen deutlich, was zeigt, dass das Enzym in diesem Kontext aktiv Kopienzahlveränderungen fördert. Im Gegensatz dazu verhinderte die Hemmung der Polymerase theta in normalen Zellen mit intaktem Reparatursystem diese Deletionen nicht, sondern legte stattdessen mehr rohe DNA‑Brüche an fragilen Stellen offen. Das deutet darauf hin, dass Polymerase theta entweder die Umgestaltung des Genoms antreiben kann, wenn andere Reparaturoptionen fehlen, oder dazu beiträgt, Replikationsgabeln zu stabilisieren und sichtbaren Schaden zu begrenzen, wenn die Hauptreparaturmaschinerie vorhanden ist.
Warum das für Gehirngesundheit und Krebs wichtig ist
In der Summe zeichnen die Ergebnisse ein klares Bild: In neuralen Vorläuferzellen unter Replikationsstress wirken gebündelte Brüche in langen, aktiv genutzten Genen als zentrale Knotenpunkte, von denen sowohl häufige als auch seltene Kopienzahlvarianten ausgehen. Diese strukturellen Veränderungen sind nicht flüchtig; sie werden in Tochterzellen fixiert, tragen zur Diversifizierung der Genome von Zellen im sich entwickelnden Gehirn bei und können unter ungünstigen Bedingungen die Krebsentwicklung fördern. Indem fragile Genregionen, Replikationsstress und spezifische Reparaturwege miteinander verknüpft werden, bietet die Studie eine mechanistische Brücke zwischen alltäglichen Kopierfehlern der DNA und den komplexen Mustern struktureller Variation, wie sie bei neurologischen Erkrankungen und Tumoren beobachtet werden.
Zitation: Corazzi, L., Ing, A., Benito, E. et al. Recurrent DNA break clusters drive replication-stress-induced copy number variants and genome diversification. Nat Commun 17, 3627 (2026). https://doi.org/10.1038/s41467-026-71790-5
Schlüsselwörter: Kopienzahlvarianten, Replikationsstress, neurale Vorläuferzellen, DNA‑Bruch‑Cluster, Genominstabilität