Clear Sky Science · es
Los cúmulos recurrentes de roturas de ADN impulsan variantes en el número de copias inducidas por el estrés de replicación y la diversificación genómica
Cambios ocultos en nuestro plano genético
Cada célula de nuestro cuerpo copia su ADN miles de millones de veces a lo largo de la vida, y la mayoría de las veces esto ocurre sin errores. Pero cuando la maquinaria de copiado se ve sometida a tensión, fragmentos de ADN pueden perderse, duplicarse o reordenarse: cambios conocidos como variantes en el número de copias. Estas alteraciones son frecuentes en trastornos cerebrales y cánceres, pero cómo se originan ha sido durante mucho tiempo un misterio. Este estudio identifica a un culpable central: puntos débiles especiales en genes largos del cerebro donde las roturas de ADN tienden a acumularse, sembrando una sorprendente variedad de cambios genéticos permanentes.
Dónde tiende a fracturarse el genoma
Los investigadores se centraron en los “cúmulos recurrentes de roturas de ADN”, tramos dentro de genes muy largos en células progenitoras neuronales, las células en división que dan lugar a las neuronas. Estos genes largos se utilizan intensamente y se replican tarde durante el programa de replicación del ADN de la célula, lo que los hace especialmente vulnerables. Al ralentizar suavemente las ADN polimerasas con un fármaco que induce estrés de replicación, el equipo empleó secuenciación genómica profunda para observar dónde se adelgazaba el genoma. Encontraron que pequeñas pero consistentes pérdidas de ADN, y deleciones focales más marcadas, se concentraban fuertemente en estas regiones propensas a roturas dentro de genes neuronales largos, mucho más a menudo de lo que cabría esperar por azar.
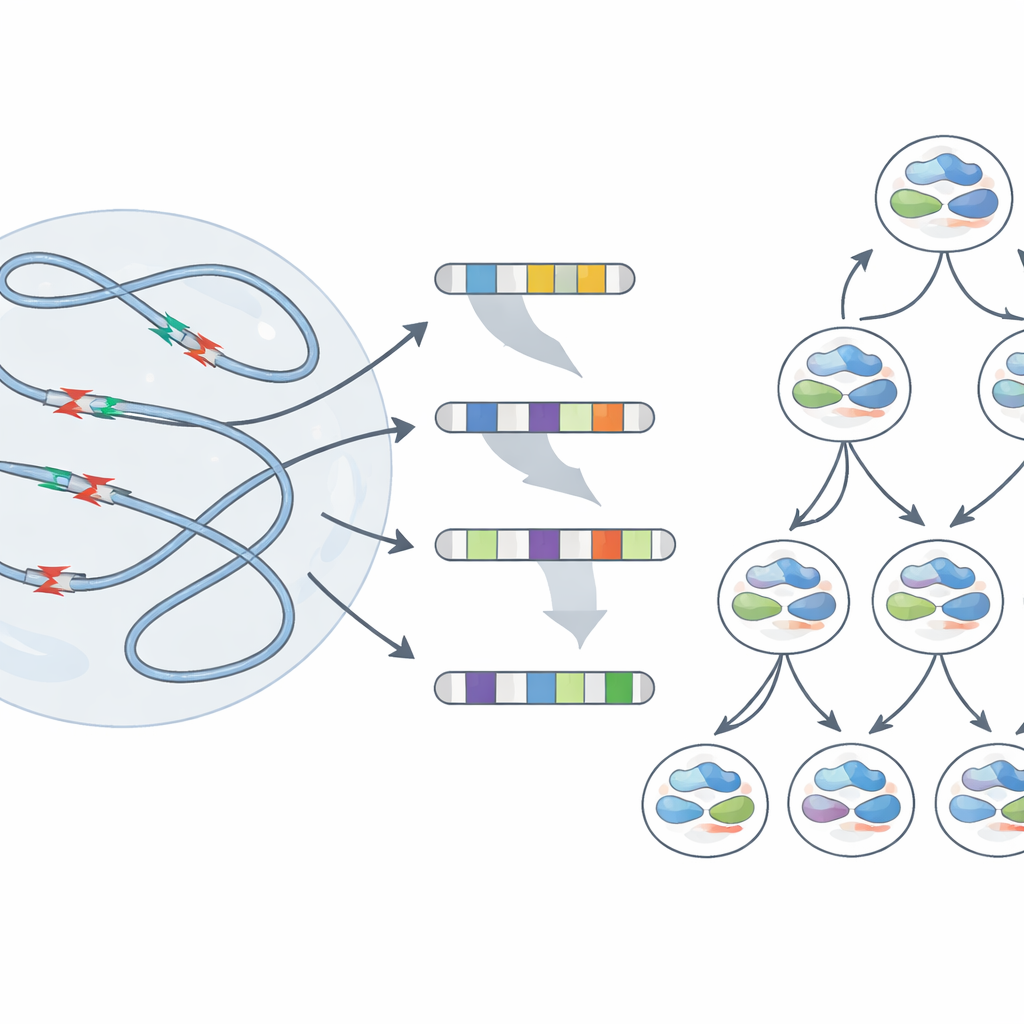
De roturas temporales a cicatrices duraderas
La secuenciación masiva muestra el comportamiento promedio a través de millones de células, pero no revela lo que ocurre en cada célula individual. Para ver cómo responden genomas individuales al estrés, el equipo utilizó un método de una sola célula que rastrea qué hebras originales de ADN hereda cada célula hija. Tras el estrés de replicación, muchas células presentaron deleciones grandes que se extendían por millones de letras de ADN e incluso pérdidas de brazos cromosómicos enteros. De forma crucial, los puntos de ruptura de estos cambios grandes con frecuencia coincidían con las mismas regiones frágiles identificadas antes. A veces, células hermanas descendientes de un ancestro estresado acababan con reordenamientos muy distintos: evidencia de que una sola ronda de daño en estos puntos calientes puede empujar a las células hijas por senderos genéticos divergentes.
La transcripción convierte puntos frágiles en fábricas de mutaciones
Los autores preguntaron entonces qué hace que estas regiones sean tan especiales. Usaron herramientas CRISPR para apagar los interruptores locales (promotores y potenciadores) que impulsan la transcripción de dos genes cerebrales gigantes conocidos por albergar cúmulos de roturas. Cuando desactivaron la transcripción, los cúmulos característicos de roturas desaparecieron y las deleciones asociadas dejaron de aparecer, incluso bajo estrés de replicación. Es notable que el momento de la replicación del ADN en esos sitios siguió siendo tardío o incluso se volvió algo más tardío, lo que demuestra que no es simplemente «cuándo» en el ciclo celular se copian estas regiones lo que importa, sino la combinación de uso activo y copiado. En otras palabras, la transcripción de genes largos mientras se replican crea zonas de conflicto donde se forman roturas, y esas roturas son la semilla de las variantes en el número de copias.
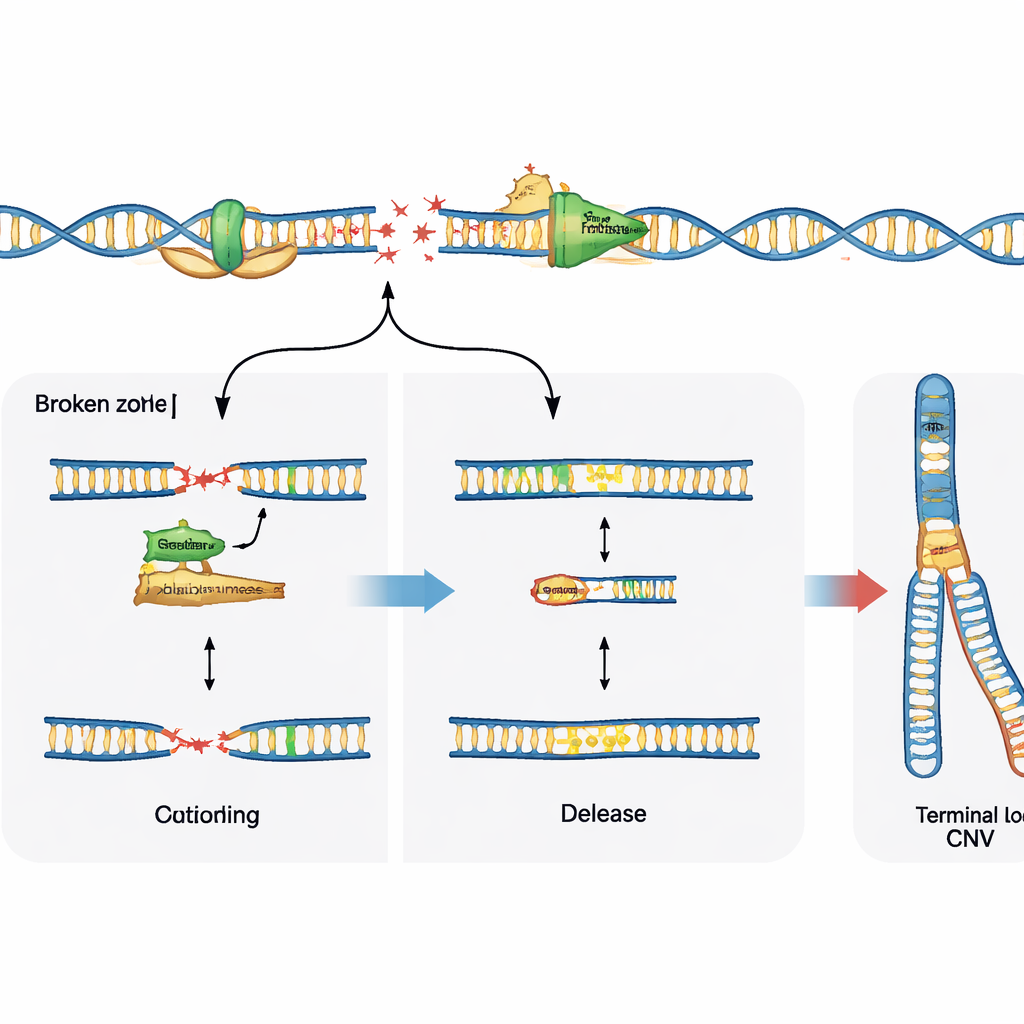
Las elecciones de reparación orientan el resultado
Romper el ADN es solo la mitad de la historia; cómo la célula repara esas roturas moldea el patrón final de variación. El estudio investigó el papel de una enzima especializada, la polimerasa theta, que se sabe parchea y une extremos rotos de ADN. En células progenitoras neuronales faltas de una vía de reparación principal llamada unión de extremos no homóloga, bloquear la polimerasa theta redujo drásticamente las deleciones recurrentes habituales en los sitios frágiles, mostrando que en este contexto la enzima promueve activamente los cambios en el número de copias. En contraste, en células normales con sistemas de reparación intactos, inhibir la polimerasa theta no evitó estas deleciones, sino que reveló más roturas de ADN sin procesar en los sitios frágiles. Esto sugiere que la polimerasa theta puede o bien impulsar la remodelación del genoma cuando faltan otras opciones de reparación, o ayudar a estabilizar las horquillas y limitar el daño visible cuando la maquinaria principal de reparación está presente.
Por qué esto importa para la salud cerebral y el cáncer
En conjunto, el trabajo dibuja un panorama claro: en células progenitoras neuronales bajo estrés de replicación, los cúmulos de roturas en genes largos y activamente utilizados actúan como centros desde los que emergen tanto variantes comunes como raras en el número de copias. Estos cambios estructurales no son efímeros; se fijan en las células hijas, contribuyendo a diversificar los genomas de las células en desarrollo del cerebro y, en condiciones desfavorables, a alimentar la evolución del cáncer. Al vincular regiones de genes frágiles, estrés de replicación y vías de reparación específicas, el estudio ofrece un puente mecanístico entre los errores cotidianos de copiado del ADN y los complejos patrones de variación estructural observados en enfermedades neurológicas y tumores.
Cita: Corazzi, L., Ing, A., Benito, E. et al. Recurrent DNA break clusters drive replication-stress-induced copy number variants and genome diversification. Nat Commun 17, 3627 (2026). https://doi.org/10.1038/s41467-026-71790-5
Palabras clave: variantes en el número de copias, estrés de replicación, células progenitoras neuronales, cúmulos de roturas de ADN, inestabilidad genómica