Clear Sky Science · nl
Terugkerende DNA-breukclusters veroorzaken kopieaantalvarianten en genoomdiversificatie door replicatiestress
Verborgen veranderingen in ons DNA-blauwdruk
Elke cel in ons lichaam kopieert zijn DNA miljarden keren tijdens een leven, en meestal verloopt dat foutloos. Maar wanneer het kopieermechanisme onder druk staat, kunnen stukken DNA verloren gaan, verdubbeld of herschikt worden—veranderingen die bekendstaan als kopieaantalvarianten. Deze aanpassingen komen veel voor bij hersenaandoeningen en kanker, maar hoe ze in de eerste plaats ontstaan is lange tijd onduidelijk geweest. Deze studie onthult een centrale boosdoener: bijzondere zwakke plekken in lange hersengenes waar DNA-breuken de neiging hebben zich op te stapelen en zo een verrassende verscheidenheid aan blijvende genetische veranderingen zaaien.
Waar het genoom de neiging heeft te scheuren
De onderzoekers richtten zich op “recidiverende DNA-breukclusters”, stroken binnen zeer lange genen in neurale voorlopercellen—de delende cellen die neuronen voortbrengen. Deze lange genen worden intensief gebruikt en laat in het DNA-replicatieschema van de cel gekopieerd, waardoor ze extra kwetsbaar zijn. Door DNA-polymerasen mild te vertragen met een geneesmiddel dat replicatiestress veroorzaakt, gebruikte het team diepe whole-genome sequencing om te volgen waar het genoom dunner werd. Ze vonden dat kleine maar consistente DNA-verliezen en scherp afgebakende deleties sterk geconcentreerd waren op deze breukgevoelige gebieden binnen lange neuronale genen, veel vaker dan bij toeval verwacht zou worden.
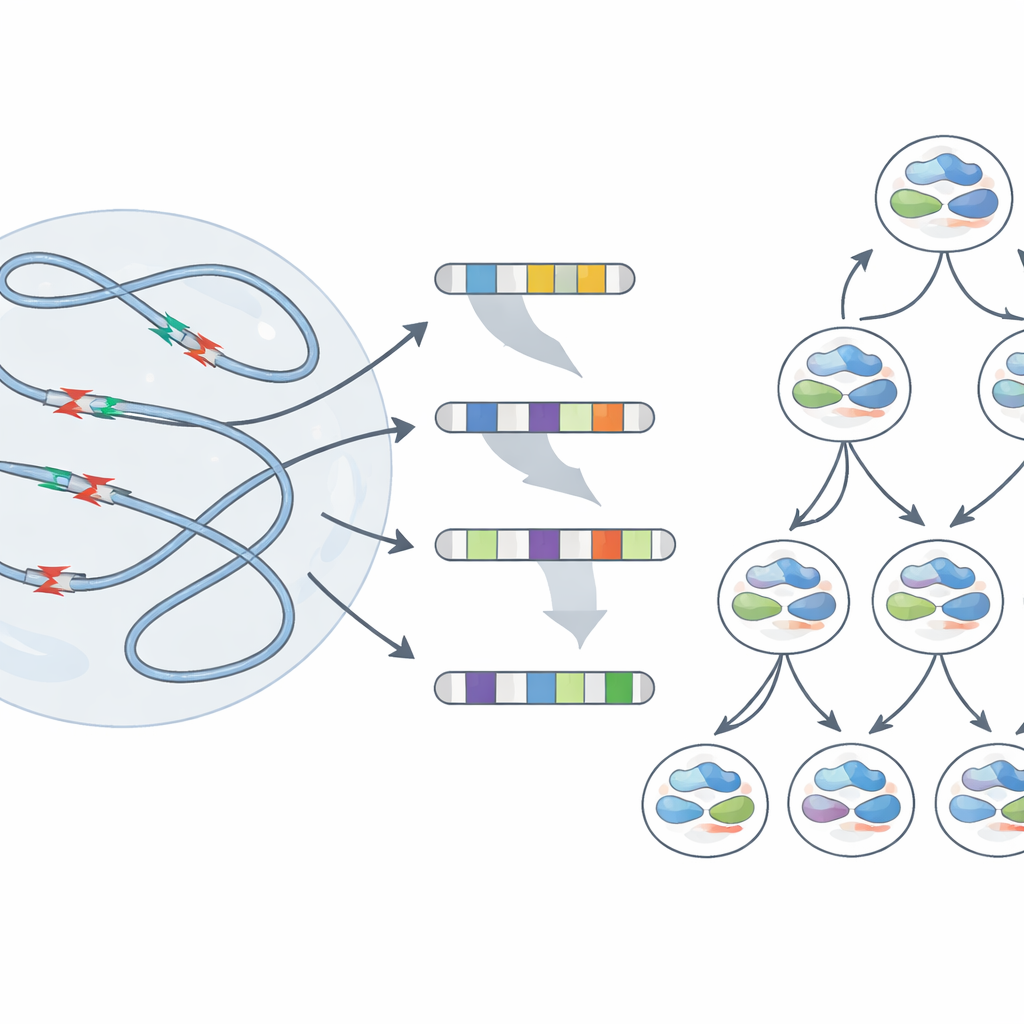
Van tijdelijke breuken naar blijvende littekens
Bulksequencing laat het gemiddelde gedrag van miljoenen cellen zien, maar onthult niet wat er in een enkele cel gebeurt. Om te zien hoe individuele genomen op stress reageren, gebruikte het team een single-cell methode die bijhoudt welke oorspronkelijke DNA-strengen elke dochtercel erft. Na replicatiestress droegen veel cellen grote deleties die zich uitstrekten over miljoenen DNA-letters en zelfs verliezen van gehele chromosoomarmen. Cruciaal is dat de breukpunten van deze grote veranderingen vaak samenvielen met dezelfde fragiele regio’s die eerder waren geïdentificeerd. Soms eindigden zustercellen die afstamden van één gestresste voorouder met zeer verschillende herschikkingen—bewijs dat een enkele ronde schade op deze hotspots dochtercellen op uiteenlopende genetische paden kan zetten.
Transcriptie verandert fragiele plekken in mutatiefabrieken
De auteurs onderzochten vervolgens wat deze regio’s zo bijzonder maakt. Ze gebruikten CRISPR-gereedschap om de lokale aan-knoppen (promoters en enhancers) uit te schakelen die de transcriptie van twee gigantische hersengenen aansturen die bekendstaan als gastheer van breukclusters. Toen ze de transcriptie uitschakelden, verdwenen de karakteristieke breukclusters en traden de bijbehorende deleties niet meer op, zelfs niet onder replicatiestress. Opvallend bleef de replicatietiming van het DNA op die locaties laat of werd zelfs iets later, wat laat zien dat het niet eenvoudigweg het tijdstip in de celcyclus is waarop deze regio’s gekopieerd worden dat telt, maar de combinatie van actieve benutting en kopiëren. Met andere woorden: het transcriberen van lange genen terwijl ze worden gerepliceerd creëert conflictzones waar breuken ontstaan, en die breuken vormen de zaden van kopieaantalvarianten.
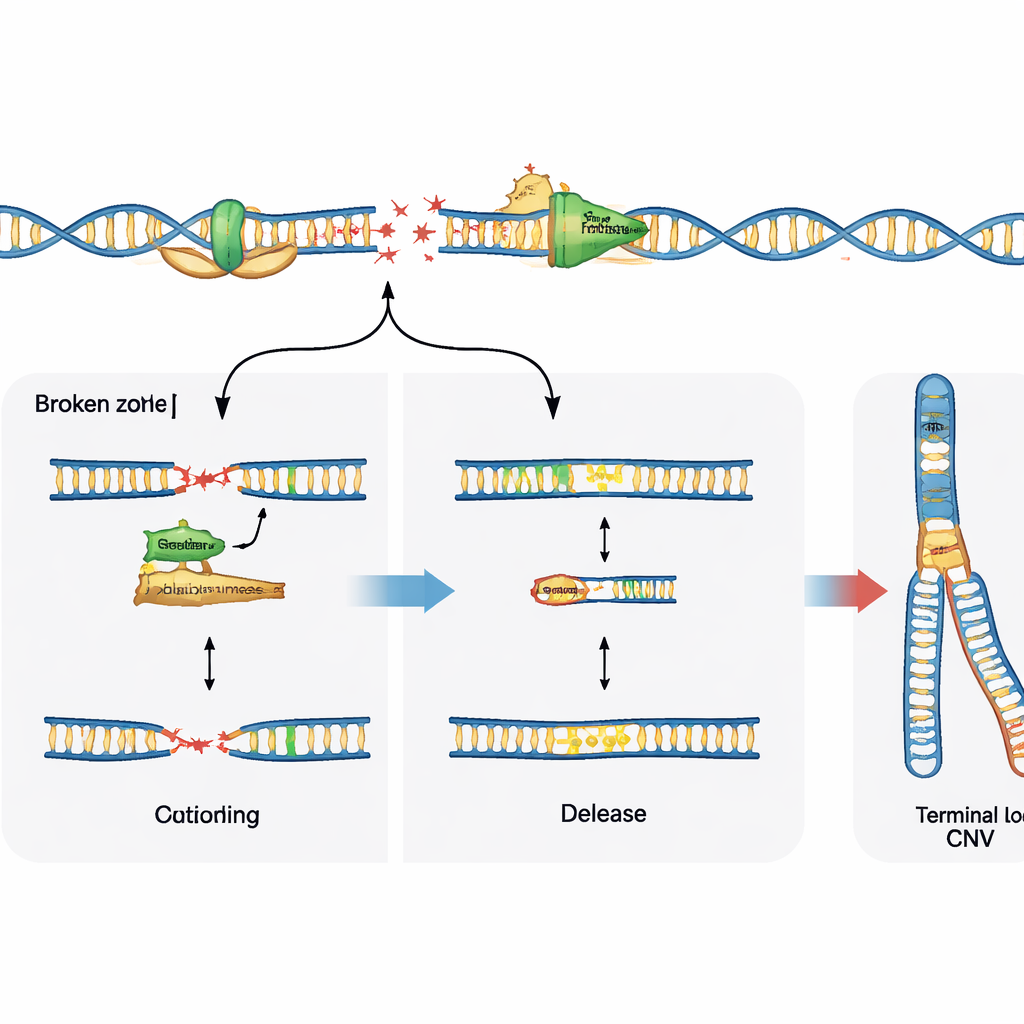
Herstelkeuzes bepalen het resultaat
DNA-breuken vormen slechts de helft van het verhaal; hoe de cel die breuken repareert, bepaalt het uiteindelijke patroon van variatie. De studie onderzocht de rol van een gespecialiseerd enzym, polymerase theta, dat bekendstaat om gebroken DNA-einden te plakken en te verbinden. In neurale voorlopercellen zonder een belangrijke herstelroute die non-homologous end joining heet, verminderde het blokkeren van polymerase theta de gebruikelijke recidiverende deleties op fragiele sites sterk, wat toont dat het enzym in deze situatie actief bijdraagt aan kopieaantalveranderingen. In normale cellen met intacte herstelmechanismen voorkwam het remmen van polymerase theta deze deleties echter niet, maar toonde het juist meer ruwe DNA-breuken op fragiele plaatsen. Dit suggereert dat polymerase theta ofwel de genoomherschikking kan stimuleren wanneer andere herstelopties ontbreken, ofwel replisomstabilisatie kan ondersteunen en zichtbaar schade kan beperken wanneer het hoofdherstelmechanisme aanwezig is.
Waarom dit belangrijk is voor hersengezondheid en kanker
Samen geven de resultaten een helder beeld: in neurale voorlopercellen onder replicatiestress fungeren gebundelde breuken in lange, actief gebruikte genen als centrale knooppunten van waaruit zowel veelvoorkomende als zeldzame kopieaantalvarianten ontstaan. Deze structurele veranderingen zijn niet vluchtig; ze worden gefixeerd in dochtercellen, dragen bij aan de diversificatie van genomen in ontwikkelende hersencellen en, onder ongunstige omstandigheden, aan de evolutie van kanker. Door fragiele genregio’s, replicatiestress en specifieke herstelroutes met elkaar te verbinden, biedt de studie een mechanistische brug tussen alledaagse kopieerfouten van DNA en de complexe patronen van structurele variatie die worden gezien bij neurologische aandoeningen en tumoren.
Bronvermelding: Corazzi, L., Ing, A., Benito, E. et al. Recurrent DNA break clusters drive replication-stress-induced copy number variants and genome diversification. Nat Commun 17, 3627 (2026). https://doi.org/10.1038/s41467-026-71790-5
Trefwoorden: kopieaantalvarianten, replicatiestress, neurale voorlopercellen, DNA-breukclusters, genoominstabiliteit