Clear Sky Science · it
I cluster ricorrenti di rotture del DNA guidano le varianti di numero di copia indotte dallo stress di replicazione e la diversificazione del genoma
Cambiamenti nascosti nel nostro progetto del DNA
Ogni cellula del nostro corpo copia il proprio DNA miliardi di volte nel corso della vita, e nella maggior parte dei casi questo avviene in modo impeccabile. Ma quando la macchina di copiatura è sotto sforzo, porzioni di DNA possono andare perse, essere duplicate o riorganizzate—alterazioni note come varianti di numero di copia. Questi cambiamenti sono comuni nei disturbi cerebrali e nei tumori, eppure il modo in cui si originano è stato a lungo un mistero. Questo studio individua un colpevole centrale: punti deboli speciali in geni cerebrali molto lunghi dove le rotture del DNA tendono ad accumularsi, seminando una sorprendente varietà di modifiche genetiche permanenti.
Dove il genoma tende a incrinarsi
I ricercatori si sono concentrati sui “cluster ricorrenti di rotture del DNA”, tratti all’interno di geni molto lunghi nelle cellule progenitrici neurali—le cellule in divisione che danno origine ai neuroni. Questi geni lunghi sono intensamente utilizzati e vengono copiati in fase tardiva del programma di replicazione del DNA della cellula, rendendoli particolarmente vulnerabili. Rallentando leggermente le DNA polimerasi con un farmaco che induce stress di replicazione, il gruppo ha utilizzato sequenziamento dell’intero genoma ad alta profondità per osservare dove il genoma si assottigliava. Hanno trovato che piccole ma coerenti perdite di DNA, e delezioni più nette e focali, si concentravano in modo marcato in queste regioni predisposte alle rotture all’interno dei lunghi geni neuronali, molto più spesso di quanto ci si attenderebbe per caso.
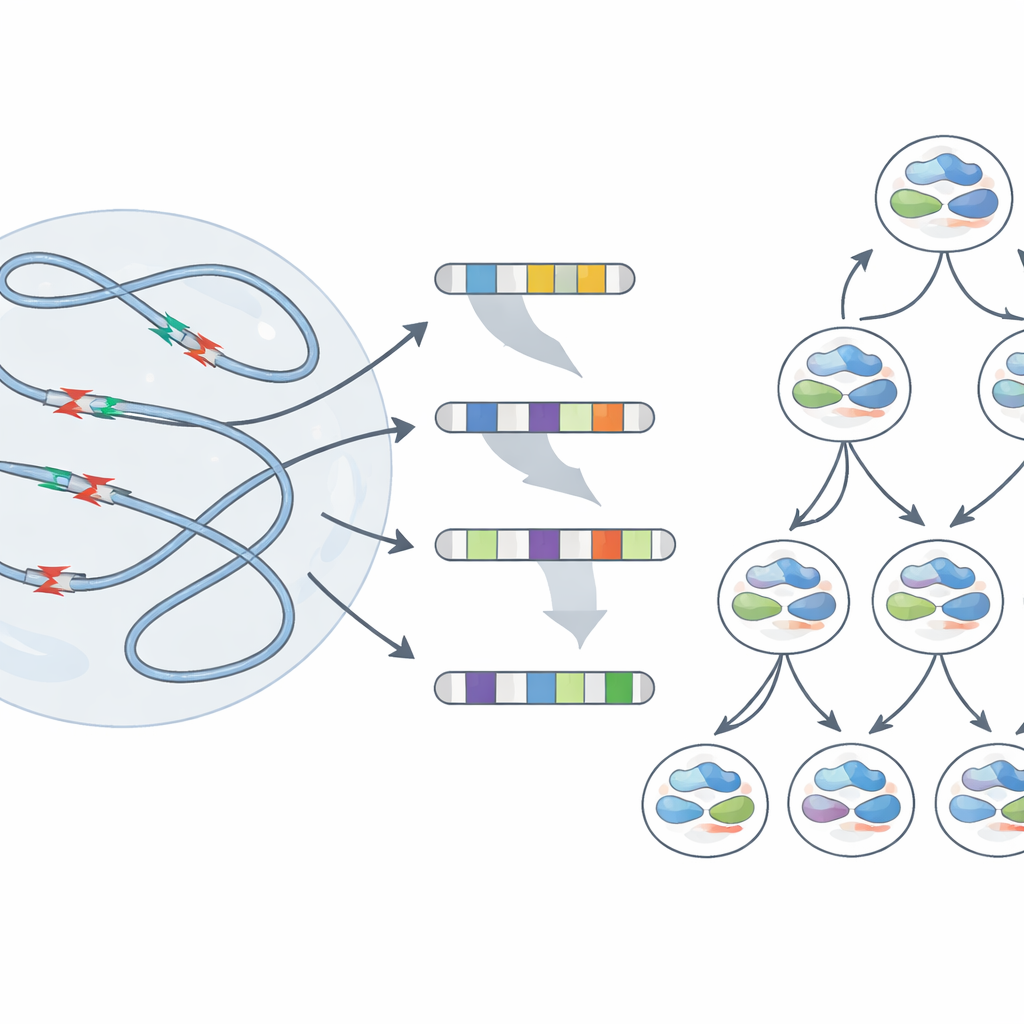
Dalle rotture temporanee alle cicatrici durature
Il sequenziamento in massa mostra il comportamento medio su milioni di cellule, ma non rivela cosa accade in una singola cellula. Per vedere come singoli genomi rispondono allo stress, il gruppo ha impiegato un metodo a singola cellula che traccia quali filamenti di DNA originali ciascuna cellula figlia eredita. Dopo lo stress di replicazione, molte cellule presentavano grandi delezioni che si estendevano su milioni di basi e perfino perdite di interi bracci cromosomici. Crucialmente, i punti di rottura di questi grandi cambiamenti spesso coincidevano con le stesse regioni fragili identificate in precedenza. Talvolta, cellule sorelle discendenti da un unico antenato stressato finivano con riorganizzazioni molto diverse—evidenza che un singolo evento di danno in questi punti caldi può indirizzare le cellule figlie su percorsi genetici divergenti.
La trascrizione trasforma i punti fragili in «fabbriche» di mutazioni
Gli autori si sono poi chiesti cosa renda queste regioni così speciali. Hanno usato strumenti CRISPR per disattivare gli interruttori locali (promotori ed enhancer) che guidano la trascrizione di due giganteschi geni cerebrali noti per ospitare cluster di rotture. Quando hanno spento la trascrizione, i tipici cluster di rotture sono scomparsi e le delezioni associate non si sono più verificate, neppure sotto stress di replicazione. È notevole che il timing della replicazione del DNA in quei siti sia rimasto tardivo o sia addirittura diventato leggermente più tardivo, dimostrando che non è semplicemente il “quando” del ciclo cellulare che conta, ma la combinazione di uso attivo e copiatura. In altre parole, trascrivere geni lunghi mentre vengono replicati crea zone di conflitto dove si formano rotture, e quelle rotture sono il seme delle varianti di numero di copia.
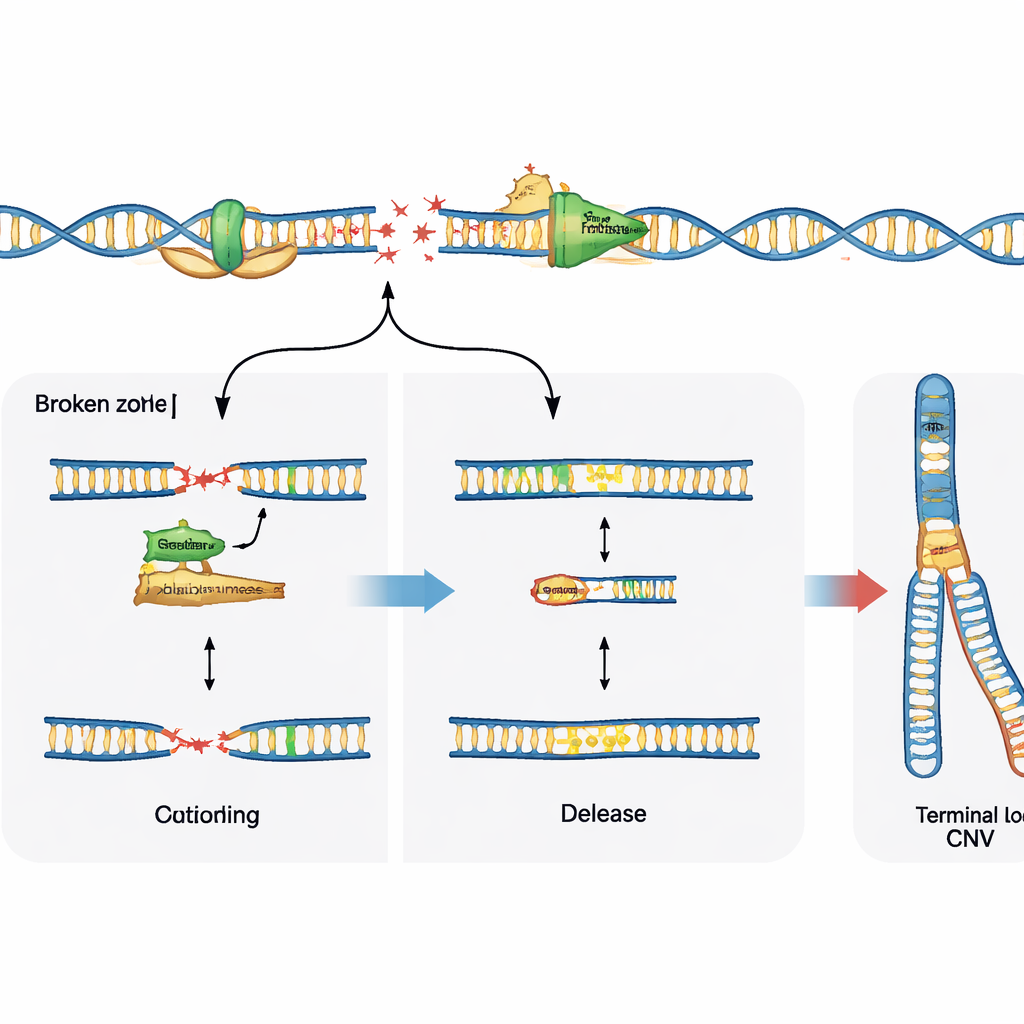
Le scelte di riparazione orientano l’esito
Rompere il DNA è solo metà della storia; il modo in cui la cellula ripara quelle rotture determina il modello finale di variazione. Lo studio ha esplorato il ruolo di un enzima specializzato, la polimerasi theta, nota per rattoppare e unire estremità del DNA spezzate. Nelle cellule progenitrici neurali prive di una via di riparazione principale chiamata giunzione non omologa delle estremità, bloccare la polimerasi theta ha ridotto drasticamente le delezioni ricorrenti abituali nei siti fragili, mostrando che in questo contesto l’enzima promuove attivamente i cambiamenti del numero di copie. Al contrario, nelle cellule normali con sistemi di riparazione integri, l’inibizione della polimerasi theta non ha impedito queste delezioni ma ha invece rivelato più rotture di DNA grezze nei siti fragili. Questo suggerisce che la polimerasi theta può o guidare il rimodellamento del genoma quando altre opzioni di riparazione mancano, o contribuire a stabilizzare le forcelle di replicazione e limitare il danno visibile quando la principale macchina di riparazione è presente.
Perché questo conta per la salute cerebrale e il cancro
Nel complesso, il lavoro dipinge un quadro chiaro: nelle cellule progenitrici neurali sotto stress di replicazione, cluster di rotture in geni lunghi e attivamente utilizzati agiscono come hub centrali da cui emergono sia varianti di numero di copia comuni sia rare. Questi cambiamenti strutturali non sono fugaci; si fissano nelle cellule figlie, contribuendo a diversificare i genomi delle cellule nel cervello in sviluppo e, nelle condizioni sbagliate, a nutrire l’evoluzione tumorale. Collegando regioni geniche fragili, stress di replicazione e specifiche vie di riparazione, lo studio offre un ponte meccanicistico tra gli errori quotidiani di copiatura del DNA e i complessi modelli di variazione strutturale osservati nelle malattie neurologiche e nei tumori.
Citazione: Corazzi, L., Ing, A., Benito, E. et al. Recurrent DNA break clusters drive replication-stress-induced copy number variants and genome diversification. Nat Commun 17, 3627 (2026). https://doi.org/10.1038/s41467-026-71790-5
Parole chiave: varianti di numero di copia, stress di replicazione, cellule progenitrici neurali, cluster di rotture del DNA, instabilità del genoma