Clear Sky Science · pt
Clusters recorrentes de quebras de DNA impulsionam variantes de número de cópia induzidas por estresse de replicação e diversificação do genoma
Mudanças ocultas no nosso projeto de DNA
Cada célula do nosso corpo copia seu DNA bilhões de vezes ao longo da vida, e na maior parte das vezes isso ocorre sem erros. Mas quando a maquinaria de cópia fica sobrecarregada, fragmentos de DNA podem ser perdidos, duplicados ou rearranjados — alterações conhecidas como variantes de número de cópia. Essas alterações são comuns em distúrbios cerebrais e em cânceres, entretanto como elas surgem inicialmente tem sido um mistério de longa data. Este estudo revela um culpado central: pontos fracos especiais em genes longos do cérebro onde quebras de DNA tendem a se acumular, semeando uma variedade surpreendente de mudanças genéticas permanentes.
Onde o genoma tende a rachar
Os pesquisadores concentraram-se em “clusters recorrentes de quebras de DNA”, trechos dentro de genes muito longos em células progenitoras neurais — as células em divisão que dão origem aos neurônios. Esses genes longos são muito transcritos e replicados tardiamente no cronograma de replicação do DNA da célula, tornando-os especialmente vulneráveis. Ao desacelerar suavemente as DNA polimerases com um fármaco que induz estresse de replicação, a equipe usou sequenciamento profundo do genoma inteiro para observar onde o genoma se afinava. Eles constataram que pequenas, porém consistentes, perdas de DNA e deleções focais mais acentuadas concentravam-se fortemente nessas regiões propensas a quebras dentro de genes neuronais longos, muito mais frequentemente do que seria esperado ao acaso.
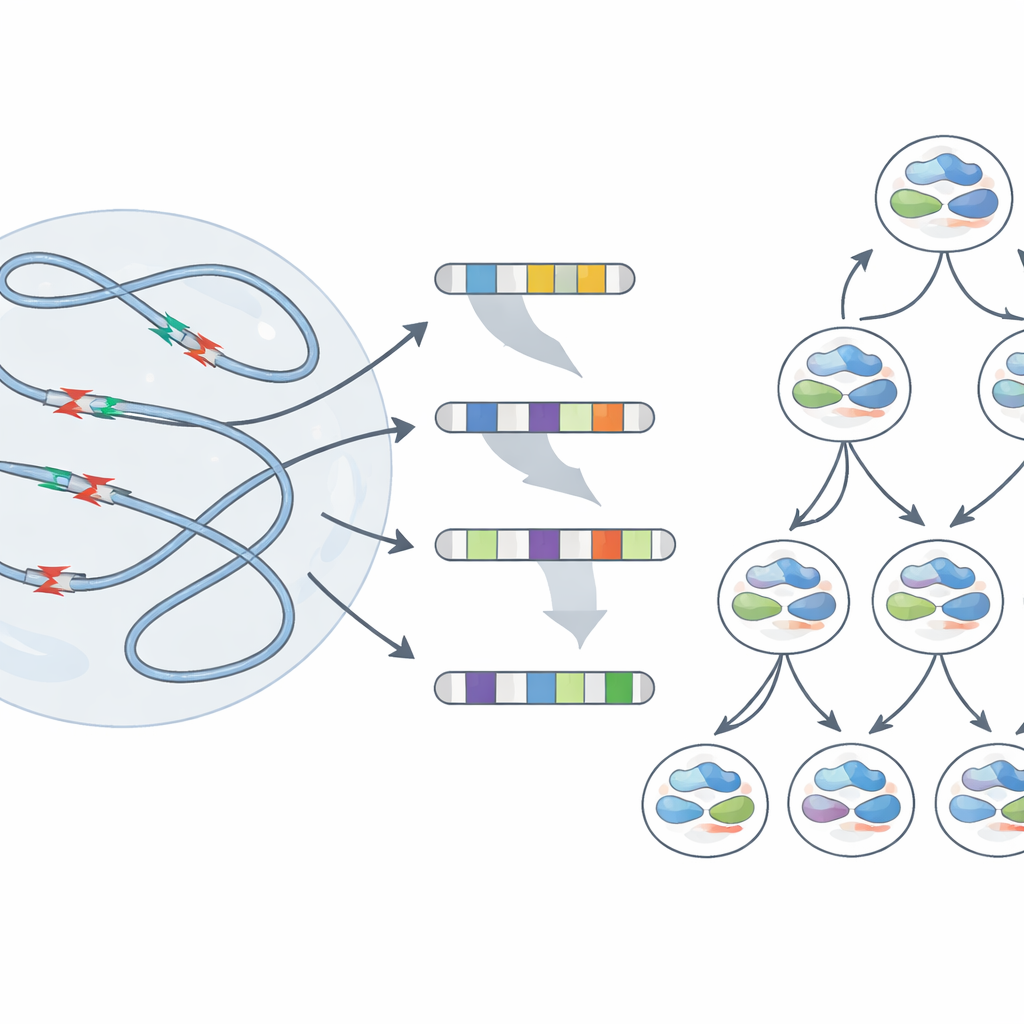
De quebras temporárias a cicatrizes permanentes
O sequenciamento em massa mostra o comportamento médio de milhões de células, mas não revela o que acontece em cada célula individual. Para ver como genomas individuais respondem ao estresse, a equipe usou um método de célula única que rastreia quais fitas originais de DNA cada célula filha herda. Após o estresse de replicação, muitas células apresentaram grandes deleções abrangendo milhões de letras de DNA e até perdas de braços cromossômicos inteiros. Crucialmente, os pontos de quebra dessas grandes alterações frequentemente se alinhavam com as mesmas regiões frágeis identificadas anteriormente. Às vezes, células irmãs descendentes de um mesmo ancestral estressado apresentaram rearranjos muito diferentes — evidência de que uma única rodada de dano nesses pontos quentes pode desviar as células filhas para caminhos genéticos divergentes.
A transcrição transforma pontos frágeis em fábricas de mutação
Os autores então investigaram o que torna essas regiões tão especiais. Eles usaram ferramentas CRISPR para desligar os interruptores locais (promotores e enhancers) que impulsionam a transcrição de dois genes gigantes do cérebro conhecidos por abrigar clusters de quebras. Quando desligaram a transcrição, os clusters característicos de quebras desapareceram, e as deleções associadas deixaram de aparecer, mesmo sob estresse de replicação. Notavelmente, o momento da replicação do DNA nesses locais permaneceu tardio ou até se tornou ligeiramente mais tardio, mostrando que não é simplesmente “quando” no ciclo celular essas regiões são copiadas que importa, mas a combinação de uso ativo e cópia. Em outras palavras, transcrever genes longos enquanto são replicados cria zonas de conflito onde ocorrem quebras, e essas quebras são as sementes das variantes de número de cópia.
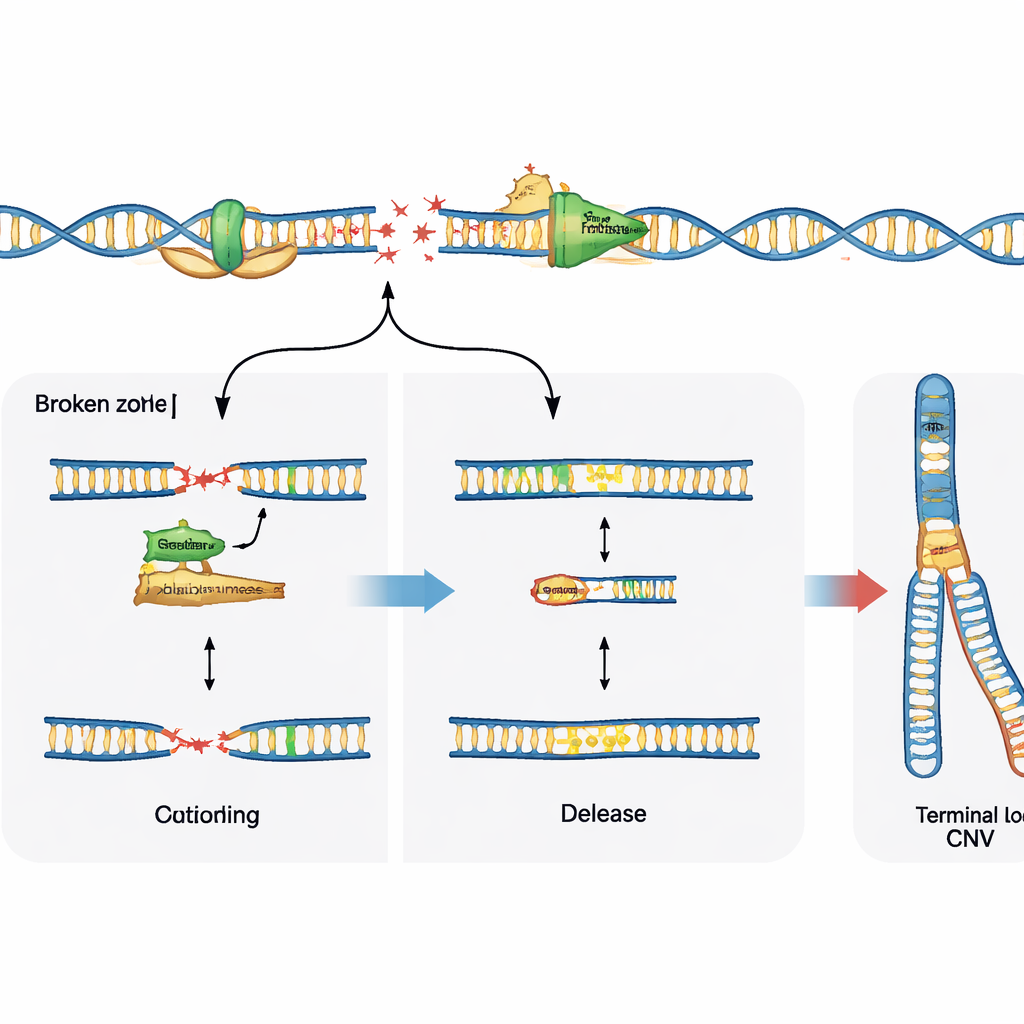
Escolhas de reparo direcionam o resultado
Quebrar o DNA é apenas metade da história; como a célula repara essas quebras molda o padrão final de variação. O estudo investigou o papel de uma enzima especializada, a polimerase theta, conhecida por selar e juntar extremidades de DNA quebrado. Em células progenitoras neurais sem uma via de reparo principal chamada junção de extremidades sem homologia, bloquear a polimerase theta reduziu fortemente as deleções recorrentes usuais em sítios frágeis, mostrando que, nesse contexto, a enzima promove ativamente as mudanças no número de cópia. Em contraste, em células normais com sistemas de reparo intactos, inibir a polimerase theta não impediu essas deleções, mas em vez disso revelou mais quebras brutas de DNA nos sítios frágeis. Isso sugere que a polimerase theta pode ou impulsionar a remodelação do genoma quando outras opções de reparo estão ausentes, ou ajudar a estabilizar forquilhas de replicação e limitar o dano visível quando a maquinaria principal de reparo está presente.
Por que isso importa para a saúde cerebral e o câncer
Em conjunto, o trabalho pinta um quadro claro: em células progenitoras neurais sob estresse de replicação, quebras agrupadas em genes longos e ativamente usados atuam como centros a partir dos quais emergem tanto variantes de número de cópia comuns quanto raras. Essas alterações estruturais não são passageiras; elas se tornam fixas nas células filhas, ajudando a diversificar os genomas das células no cérebro em desenvolvimento e, em condições inadequadas, a alimentar a evolução do câncer. Ao ligar regiões gênicas frágeis, estresse de replicação e vias específicas de reparo, o estudo oferece uma ponte mecanicista entre erros cotidianos na cópia do DNA e os padrões complexos de variação estrutural observados em doenças neurológicas e tumores.
Citação: Corazzi, L., Ing, A., Benito, E. et al. Recurrent DNA break clusters drive replication-stress-induced copy number variants and genome diversification. Nat Commun 17, 3627 (2026). https://doi.org/10.1038/s41467-026-71790-5
Palavras-chave: variantes de número de cópia, estresse de replicação, células progenitoras neurais, clusters de quebras de DNA, instabilidade genômica