Clear Sky Science · pl
Klastrowe uszkodzenia DNA wielokrotnie występujące prowadzą do wariantów liczby kopii wywołanych stresem replikacyjnym i dywersyfikacji genomu
Ukryte zmiany w naszej instrukcji DNA
Każda komórka w naszym ciele kopiuje swoje DNA miliardy razy w ciągu życia i zazwyczaj odbywa się to bezbłędnie. Jednak gdy mechanizm kopiowania jest przeciążony, fragmenty DNA mogą zostać utracone, zduplikowane albo przestawione — zmiany znane jako warianty liczby kopii. Te modyfikacje są powszechne w zaburzeniach mózgu i nowotworach, a ich powstawanie od dawna stanowiło zagadkę. W tym badaniu wykryto głównego winowajcę: szczególne słabe punkty w długich genach mózgowych, w których gromadzą się pęknięcia DNA i które dają początek zaskakującej różnorodności trwałych zmian genetycznych.
Gdzie genom ma tendencję do pękania
Naukowcy skoncentrowali się na „wielokrotnie występujących klastrach pęknięć DNA” — odcinkach bardzo długich genów w komórkach progenitorowych nerwowych, czyli dzielących się komórkach będących źródłem neuronów. Te długie geny są intensywnie eksploatowane i kopiowane późno w harmonogramie replikacji DNA komórki, co czyni je szczególnie podatnymi. Poprzez delikatne spowolnienie polimeraz DNA lekiem wywołującym stres replikacyjny, zespół użył głębokiego sekwencjonowania całego genomu, by zobaczyć, gdzie genom się przerzedza. Stwierdzili, że niewielkie, ale spójne utraty DNA oraz wyraźne, ogniskowe delecje koncentrowały się w tych podatnych na pęknięcia regionach długich genów neuronalnych znacznie częściej niż można by oczekiwać przypadkowo.
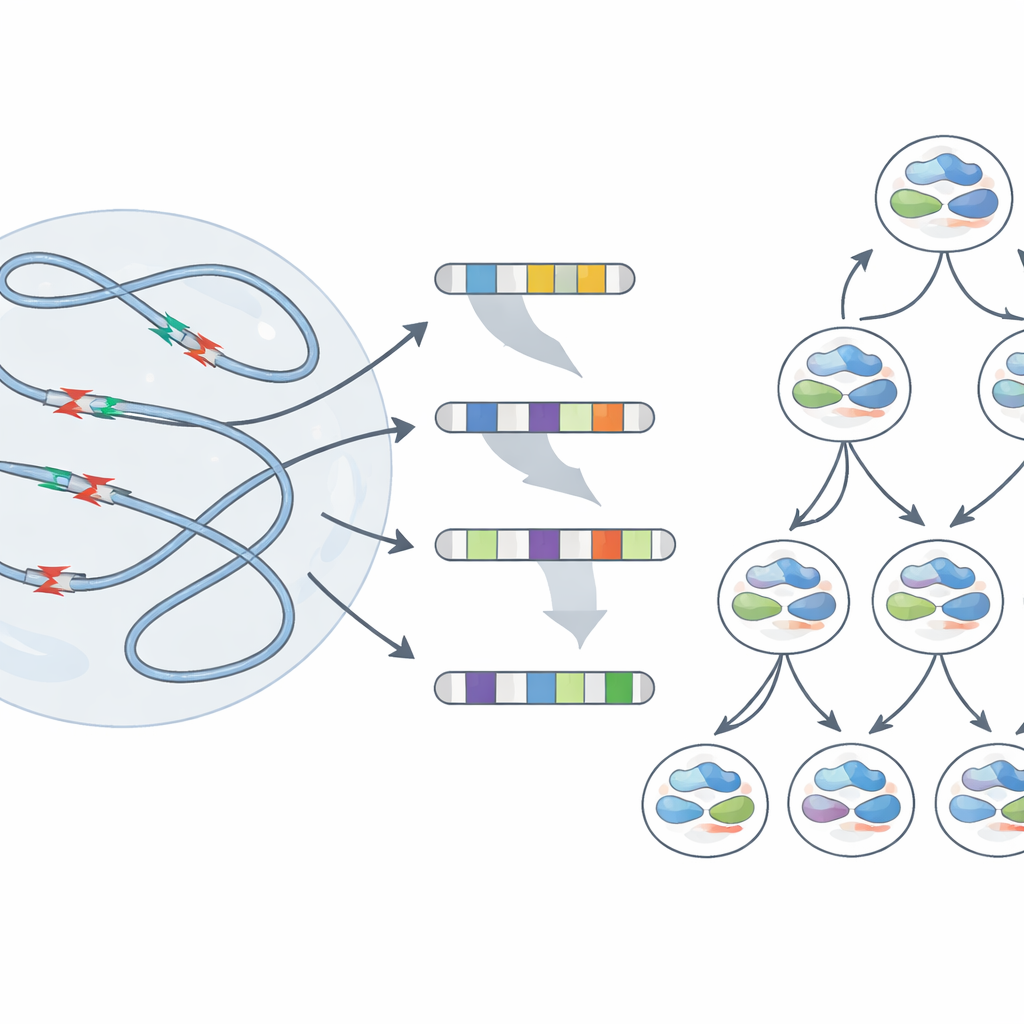
Z tymczasowych pęknięć w trwałe blizny
Analiza masowa pokazuje średnie zachowanie w milionach komórek, ale nie ujawnia, co dzieje się w pojedynczej komórce. Aby zobaczyć, jak indywidualne genomy reagują na stres, zespół zastosował metodę jednowkomórkową, śledzącą, które oryginalne nici DNA każda komórka‑córka odziedziczyła. Po stresie replikacyjnym wiele komórek nosiło duże delecje obejmujące miliony nukleotydów, a nawet utraty całych ramion chromosomów. Co istotne, punkty złamania tych dużych zmian często pokrywały się z tymi samymi kruchemi regionami zidentyfikowanymi wcześniej. Czasem komórki‑siostry pochodzące od jednego zestresowanego przodka kończyły z bardzo różnymi przebudowaniami — dowód, że jedna runda uszkodzeń w tych punktach może skierować komórki‑córki na odmienne genetyczne ścieżki.
Transkrypcja zamienia kruche miejsca w fabryki mutacji
Autorzy zastanawiali się następnie, co czyni te regiony tak wyjątkowymi. Użyli narzędzi CRISPR do wyłączenia lokalnych włączników (promotorów i enhancerów), które napędzają transkrypcję dwóch olbrzymich genów mózgowych znanych z występowania klastrów pęknięć. Po wyciszeniu transkrypcji charakterystyczne klastry pęknięć zniknęły, a związane z nimi delecje przestały się pojawiać, nawet pod stresem replikacyjnym. Warto zauważyć, że czas replikacji DNA w tych miejscach pozostał późny, a czasami stał się nieco jeszcze późniejszy, co pokazuje, że kluczowe nie jest wyłącznie „kiedy” w cyklu komórkowym te regiony są kopiowane, lecz połączenie ich aktywnego użytkowania i kopiowania. Innymi słowy, transkrypcja długich genów podczas ich replikacji tworzy strefy konfliktu, w których powstają pęknięcia, a te pęknięcia są zalążkiem wariantów liczby kopii.
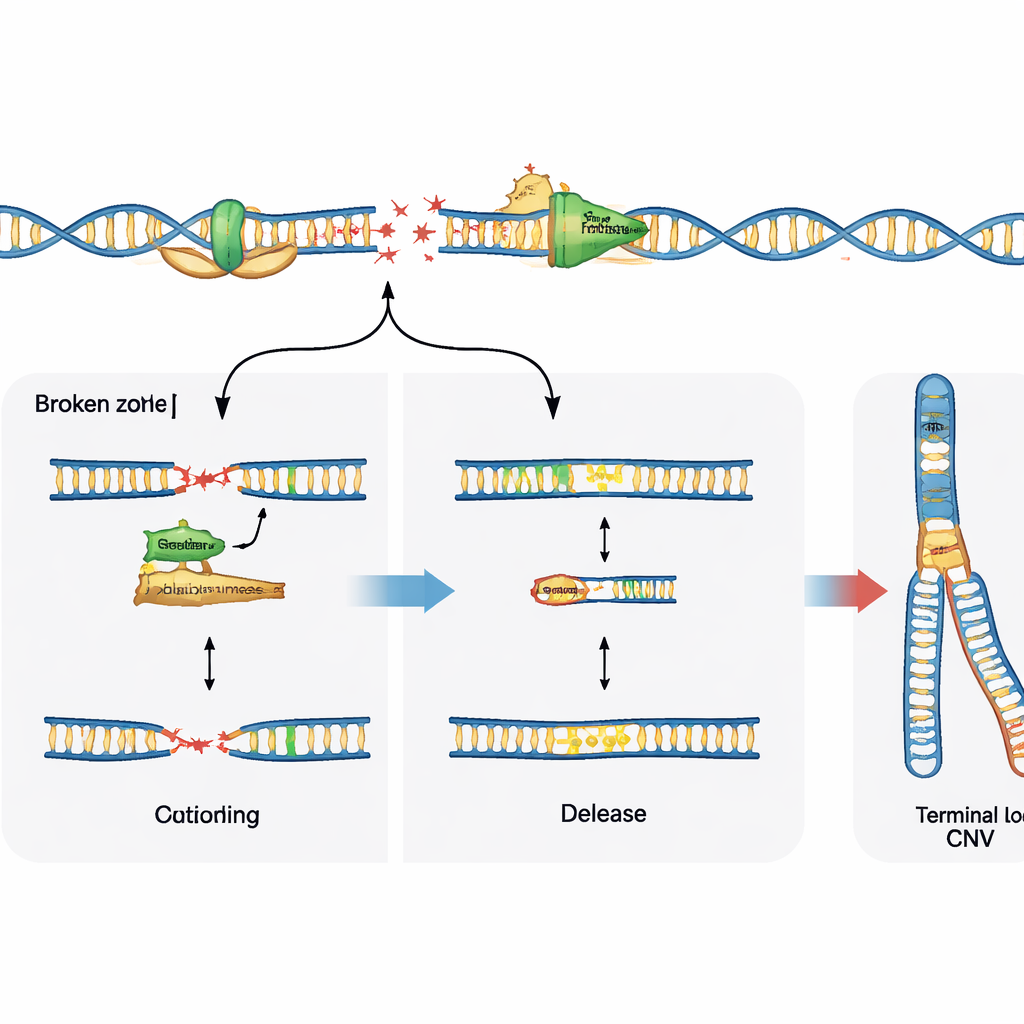
Wybory naprawy kierują końcowym wynikiem
Pękanie DNA to tylko połowa opowieści; to, jak komórka naprawia te złamania, kształtuje ostateczny wzorzec zmienności. Badanie sprawdziło rolę wyspecjalizowanej enzymu, polimerazy theta, która jest znana z łatania i łączenia przerwanych końców DNA. W komórkach progenitorowych nerwowych pozbawionych głównej ścieżki naprawczej zwanej łączeniem bez homologii, blokada polimerazy theta wyraźnie zmniejszyła typowe wielokrotne delecje w miejscach podatnych, co pokazuje, że w tym kontekście enzym aktywnie promuje zmiany liczby kopii. W przeciwieństwie do tego, w normalnych komórkach z nienaruszonymi systemami naprawczymi, hamowanie polimerazy theta nie zapobiegło tym delecjom, lecz ujawniło więcej surowych złamań DNA w miejscach kruchych. Sugeruje to, że polimeraza theta może albo napędzać przebudowę genomu, gdy brakuje innych opcji naprawy, albo pomagać stabilizować widełki i ograniczać widoczne uszkodzenia, gdy główne mechanizmy naprawcze są obecne.
Dlaczego to ma znaczenie dla zdrowia mózgu i nowotworów
Podsumowując, praca kreśli jasny obraz: w komórkach progenitorowych nerwowych pod stresem replikacyjnym skumulowane pęknięcia w długich, aktywnie używanych genach działają jako centralne węzły, z których powstają zarówno powszechne, jak i rzadkie warianty liczby kopii. Te zmiany strukturalne nie są przemijające; utrwalają się w komórkach‑córkach, przyczyniając się do dywersyfikacji genomów komórek w rozwijającym się mózgu i, w niekorzystnych warunkach, napędzając ewolucję nowotworów. Łącząc kruche regiony genów, stres replikacyjny i specyficzne szlaki naprawcze, badanie oferuje mechanistyczne ogniwo między codziennymi błędami kopiowania DNA a złożonymi wzorcami wariacji strukturalnej obserwowanymi w chorobach neurologicznych i guzach.
Cytowanie: Corazzi, L., Ing, A., Benito, E. et al. Recurrent DNA break clusters drive replication-stress-induced copy number variants and genome diversification. Nat Commun 17, 3627 (2026). https://doi.org/10.1038/s41467-026-71790-5
Słowa kluczowe: warianty liczby kopii, stres replikacyjny, komórki progenitorowe nerwowe, klastry pęknięć DNA, niestabilność genomu