Clear Sky Science · fr
Des grappes récurrentes de cassures d’ADN provoquent des variants de nombre de copies induits par le stress de réplication et la diversification du génome
Changements cachés dans notre plan d’ADN
Chaque cellule de notre corps copie son ADN des milliards de fois au cours d’une vie, et la plupart du temps cela se passe sans erreur. Mais lorsque la machinerie de copie est mise à rude épreuve, des segments d’ADN peuvent être perdus, dupliqués ou réarrangés — des modifications appelées variants de nombre de copies. Ces altérations sont fréquentes dans les troubles cérébraux et les cancers, pourtant leur origine restait longtemps mystérieuse. Cette étude met en évidence un coupable central : des points faibles particuliers dans de longs gènes cérébraux où les cassures d’ADN ont tendance à s’accumuler, semant une variété surprenante de changements génétiques permanents.
Où le génome a tendance à se fissurer
Les chercheurs se sont concentrés sur les « grappes récurrentes de cassures d’ADN », des étendues situées au sein de très longs gènes dans les cellules progénitrices neuronales — les cellules en division qui donnent naissance aux neurones. Ces longs gènes sont fortement transcrits et copiés tard dans le programme de réplication de la cellule, ce qui les rend particulièrement vulnérables. En ralentissant délicatement les ADN polymérases avec un médicament induisant le stress de réplication, l’équipe a utilisé un séquençage profond du génome complet pour observer où le génome s’affaiblissait. Ils ont constaté que de petites pertes d’ADN constantes, ainsi que des délétions plus nettes et focales, se concentraient fortement à ces régions fragiles au sein des longs gènes neuronaux, bien plus souvent que ce qui serait attendu par hasard.
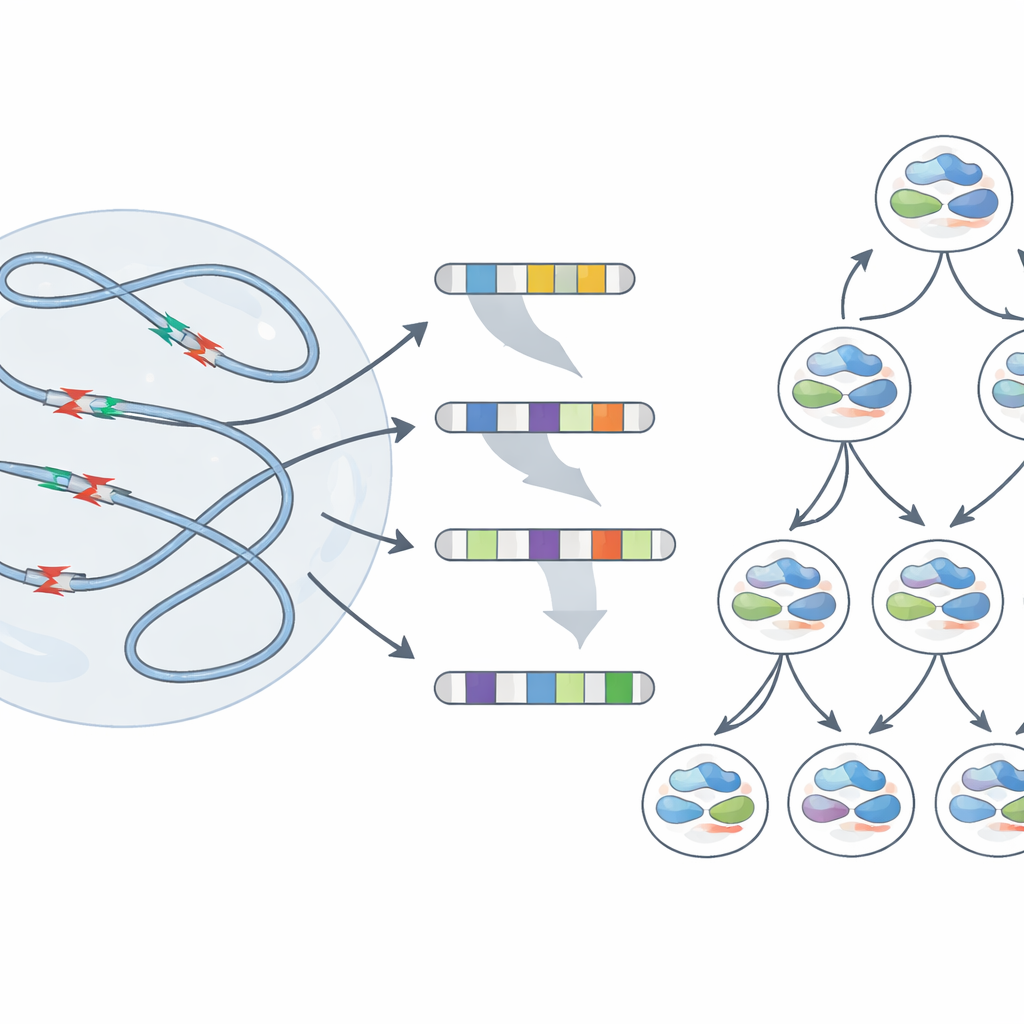
De cassures temporaires à cicatrices durables
Le séquençage en masse montre le comportement moyen de millions de cellules, mais ne révèle pas ce qui arrive dans une cellule individuelle. Pour voir comment des génomes individuels répondent au stress, l’équipe a utilisé une méthode unicellulaire qui suit quelles brins d’ADN originaux chaque cellule fille hérite. Après le stress de réplication, de nombreuses cellules présentaient de larges délétions s’étendant sur des millions de bases et même des pertes de bras chromosomiques entiers. De manière cruciale, les points de cassure de ces grandes modifications coïncidaient fréquemment avec les mêmes régions fragiles identifiées précédemment. Parfois, des cellules sœurs issues d’un même ancêtre stressé présentaient des réarrangements très différents — preuve qu’un seul épisode de dommages à ces points chauds peut lancer les cellules filles sur des trajectoires génétiques divergentes.
La transcription transforme les zones fragiles en usines à mutations
Les auteurs se sont ensuite demandé ce qui rend ces régions si particulières. Ils ont utilisé des outils CRISPR pour couper les commutateurs locaux (promoteurs et enhancers) qui pilotent la transcription de deux énormes gènes cérébraux connus pour héberger des grappes de cassures. Lorsqu’ils ont arrêté la transcription, les grappes caractéristiques de cassures ont disparu et les délétions associées n’apparaissaient plus, même en présence de stress de réplication. Notamment, la chronologie de la réplication de l’ADN à ces sites est restée tardive ou est même devenue légèrement plus tardive, démontrant que ce n’est pas simplement « quand » dans le cycle cellulaire ces régions sont copiées qui importe, mais la combinaison d’une utilisation active et de la réplication. Autrement dit, transcrire de longs gènes pendant qu’ils sont répliqués crée des zones de conflit où se forment des cassures, et ces cassures sont les graines des variants de nombre de copies.
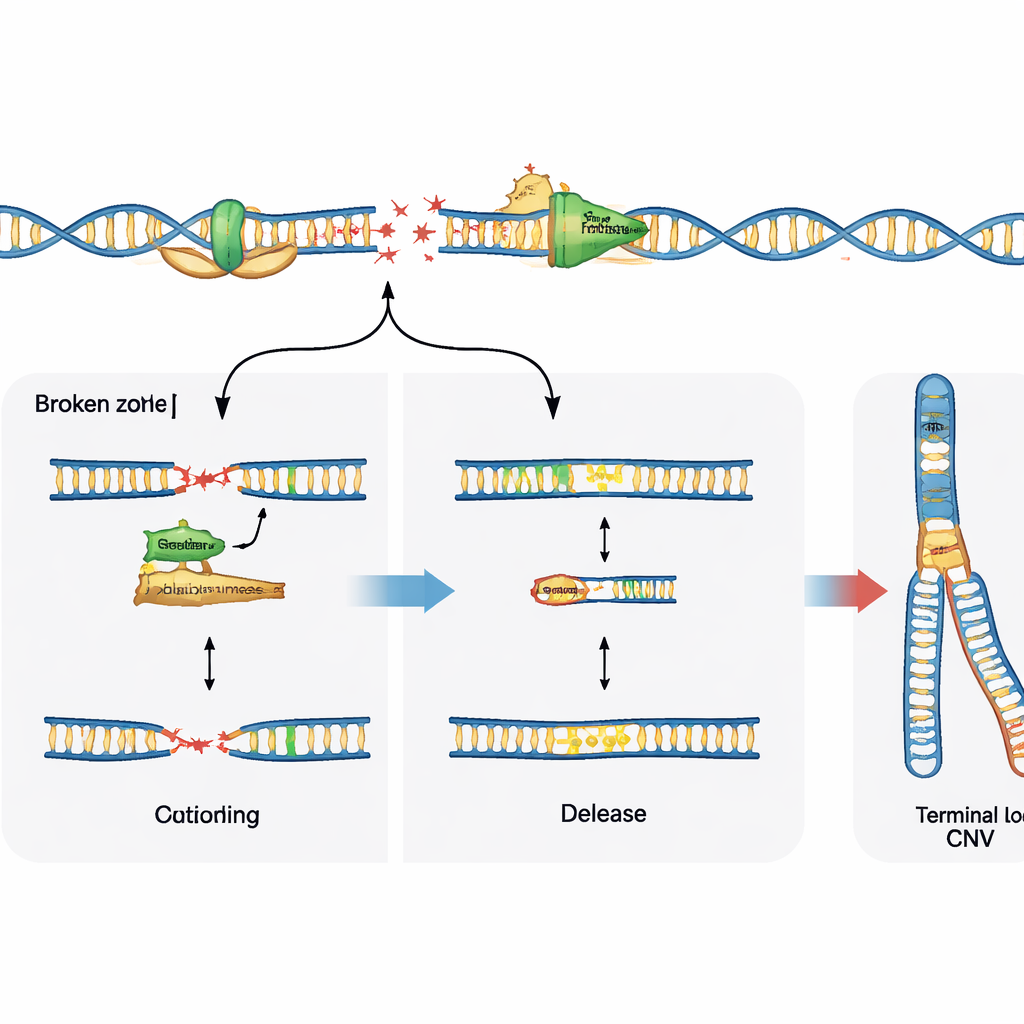
Les choix de réparation orientent le résultat
La cassure de l’ADN n’est que la moitié de l’histoire ; la manière dont la cellule répare ces cassures façonne le motif final de variation. L’étude a exploré le rôle d’une enzyme spécialisée, la polymérase thêta, connue pour raccommoder et joindre des extrémités d’ADN brisées. Dans les cellules progénitrices neuronales dépourvues d’une voie de réparation majeure appelée jonction d’extrémités non homologues, le blocage de la polymérase thêta a fortement réduit les délétions récurrentes usuelles aux sites fragiles, montrant que dans ce contexte l’enzyme favorise activement les changements de nombre de copies. En revanche, dans des cellules normales avec des systèmes de réparation intacts, l’inhibition de la polymérase thêta n’empêchait pas ces délétions mais révélait davantage de cassures d’ADN brutes aux sites fragiles. Cela suggère que la polymérase thêta peut soit entraîner le remodelage du génome lorsque d’autres options de réparation font défaut, soit aider à stabiliser les fourches de réplication et limiter les dommages visibles lorsque la machinerie principale de réparation est présente.
Pourquoi cela compte pour la santé cérébrale et le cancer
Dans l’ensemble, le travail dresse un tableau clair : dans les cellules progénitrices neuronales soumises au stress de réplication, des cassures groupées dans de longs gènes activement utilisés agissent comme des foyers centraux d’où émergent à la fois des variants de nombre de copies communs et rares. Ces modifications structurelles ne sont pas éphémères ; elles se fixent dans les cellules filles, contribuant à diversifier les génomes des cellules du cerveau en développement et, dans de mauvaises conditions, à alimenter l’évolution tumorale. En reliant régions géniques fragiles, stress de réplication et voies de réparation spécifiques, l’étude offre un pont mécanistique entre les erreurs quotidiennes de copie de l’ADN et les schémas complexes de variation structurelle observés dans les maladies neurologiques et les tumeurs.
Citation: Corazzi, L., Ing, A., Benito, E. et al. Recurrent DNA break clusters drive replication-stress-induced copy number variants and genome diversification. Nat Commun 17, 3627 (2026). https://doi.org/10.1038/s41467-026-71790-5
Mots-clés: variants de nombre de copies, stress de réplication, cellules progénitrices neuronales, grappes de cassures d’ADN, instabilité du génome