Clear Sky Science · ru
Повторяющиеся кластеры разрывов ДНК вызывают варианты числа копий и разнообразие генома при репликационном стрессе
Скрытые изменения в нашей ДНК‑схеме
Каждая клетка нашего тела копирует свою ДНК миллиарды раз за жизнь, и чаще всего это происходит без ошибок. Но когда механизм копирования испытывает перегрузку, фрагменты ДНК могут теряться, дублироваться или перестраиваться — такие изменения называют вариантами числа копий. Эти перестройки часто встречаются при заболеваниях мозга и раке, однако происхождение их долго оставалось загадкой. В этом исследовании выявлен ключевой виновник: особые уязвимые участки в очень длинных генах мозга, где склонность к разрывам ДНК создает почву для разнообразных постоянных генетических изменений.
Где геном склонен «трещать»
Исследователи сосредоточились на «повторяющихся кластерах разрывов ДНК» — участках внутри очень длинных генов в предшественниках нейронов — делящихся клетках, из которых образуются нейроны. Эти длинные гены активно транскрибируются и реплицируются поздно в расписании копирования ДНК клетки, что делает их особенно уязвимыми. Ослабив работу ДНК‑полимераз с помощью препарата, индуцирующего репликационный стресс, команда с помощью глубокого секвенирования всего генома проследила, где геном истончается. Они обнаружили, что небольшие, но повторяющиеся потери ДНК и более резкие фокальные делеции сильно концентрируются в этих склонных к разрывам участках внутри длинных нейронных генов — значительно чаще, чем можно было бы ожидать случайно.
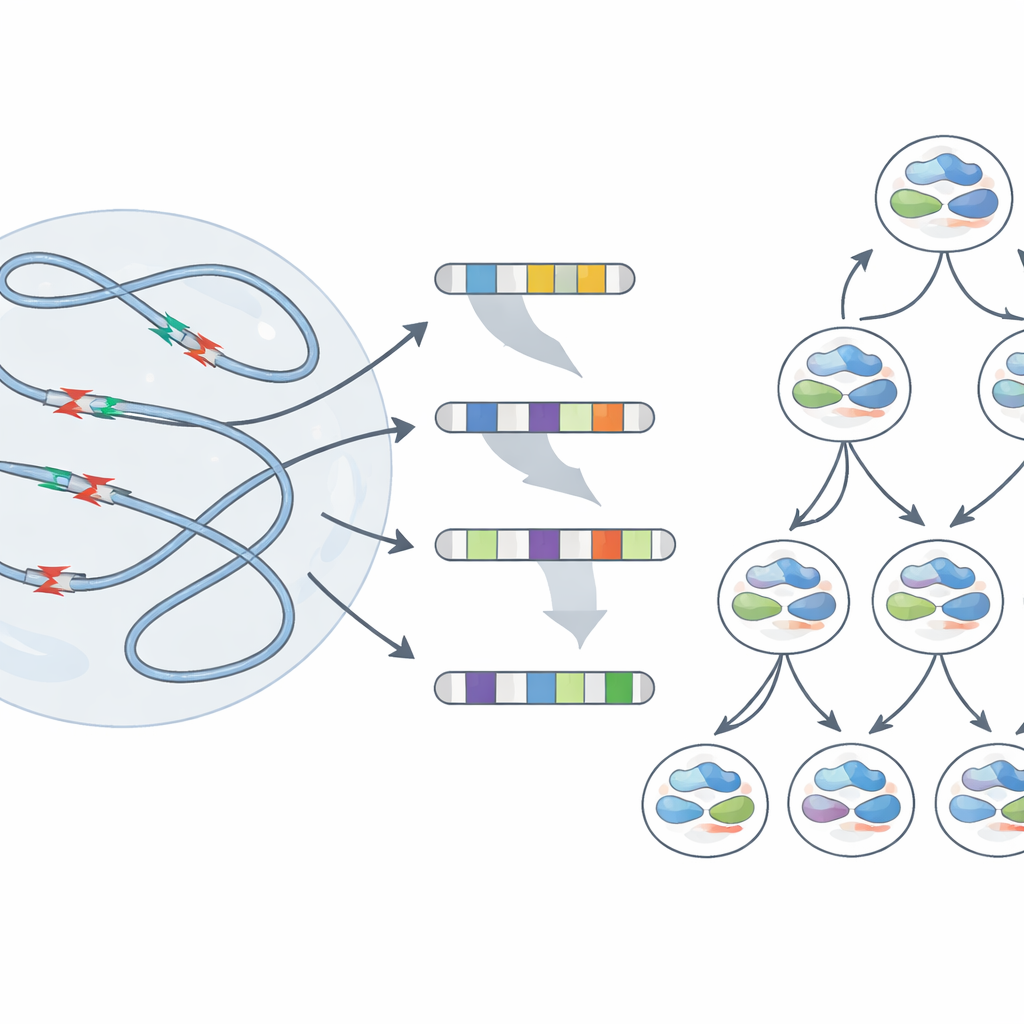
От временных разрывов к постоянным шрамам
Массовое секвенирование показывает усредненное поведение миллионов клеток, но не раскрывает, что происходит в каждой отдельной клетке. Чтобы увидеть, как отдельные геномы реагируют на стресс, команда использовала метод одиночной клетки, отслеживающий, какие исходные нитки ДНК наследует каждая дочерняя клетка. После репликационного стресса многие клетки несли большие делеции, простирающиеся на миллионы пар оснований, и даже утраты целых плеч хромосом. Важно, что точки разрыва этих крупных изменений часто совпадали с теми же хрупкими регионами, выявленными ранее. Иногда сестринские клетки, происходящие от одного повреждённого предка, получали очень разные перестройки — свидетельство того, что один раунд повреждений в этих горячих точках может запустить дочерние клетки по разным генетическим путям.
Транскрипция превращает уязвимые сайты в фабрики мутаций
Авторы затем спросили, что делает эти регионы такими особенными. Они использовали инструменты CRISPR, чтобы выключить локальные включатели (промоторы и энхансеры), которые запускают транскрипцию двух гигантских мозговых генов, известных как носители кластеров разрывов. Когда транскрипция была подавлена, характерные кластеры разрывов исчезли, и связанные с ними делеции больше не появлялись, даже при репликационном стрессе. Примечательно, что время репликации в этих участках оставалось поздним или даже сдвинулось ещё позже, что показывает: важен не только момент в клеточном цикле, когда эти регионы копируются, но сочетание их активного использования и копирования. Иначе говоря, транскрибирование длинных генов одновременно с их репликацией создаёт зоны конфликтов, где образуются разрывы, а эти разрывы становятся семенами вариантов числа копий.
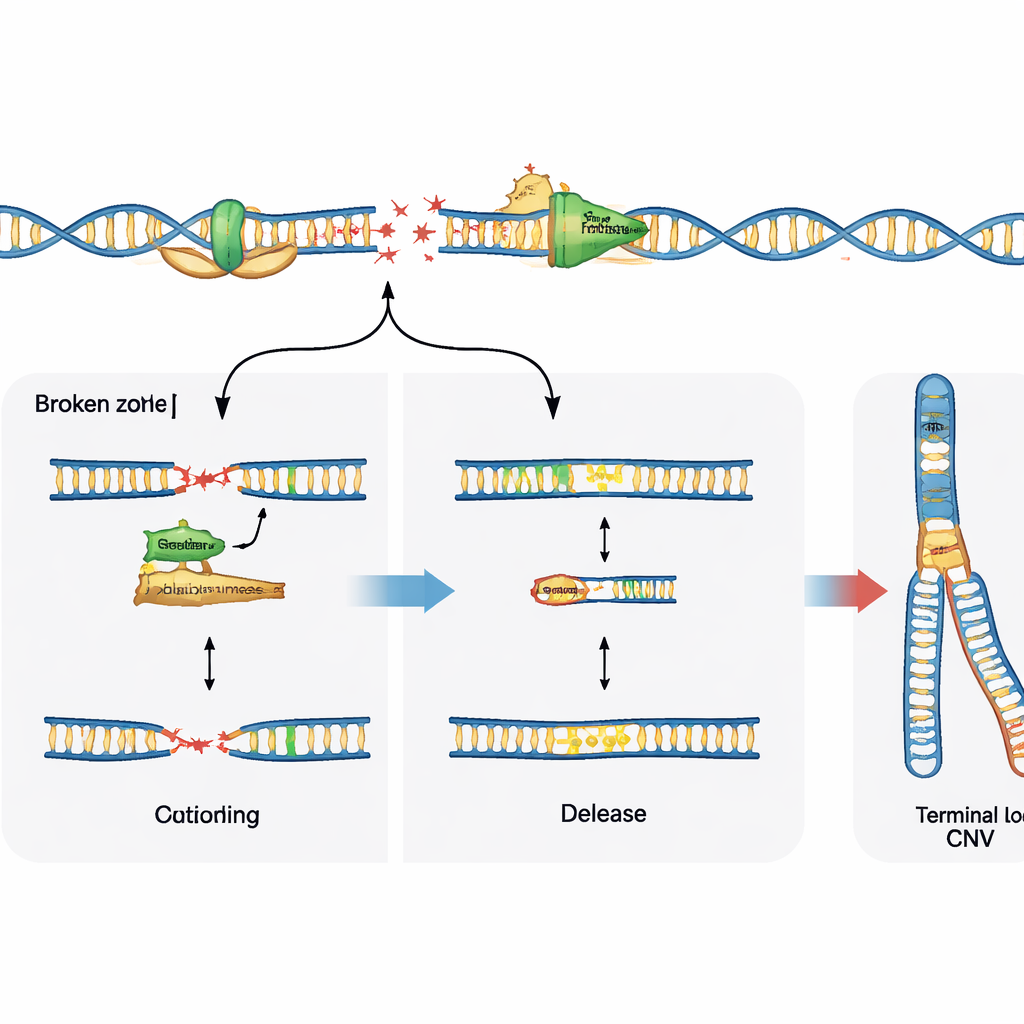
Выбор способа ремонта определяет исход
Разрыв ДНК — это только половина истории; то, как клетка восстанавливает эти разрывы, формирует итоговый узор вариаций. В работе изучали роль специализированного фермента, полимеразы тэта (theta), который известен тем, что заполняет и соединяет разорванные концы ДНК. В предшественниках нейронов, лишённых одного из основных путей ремонта — негомологичного сшивания концов, блокирование полимеразы тэта резко уменьшало типичные повторяющиеся делеции в хрупких участках, показывая, что в такой обстановке фермент активно способствует изменениям числа копий. Напротив, в нормальных клетках с интактными системами ремонта ингибирование полимеразы тэта не предотвращало эти делеции, но выявляло больше явных разрывов ДНК в хрупких зонах. Это указывает на то, что полимераза тэта может либо стимулировать перестройку генома, когда другие пути ремонта недоступны, либо помогать стабилизировать вилка репликации и ограничивать видимые повреждения, когда основной ремонт функционирует.
Почему это важно для здоровья мозга и рака
В сумме работа рисует ясную картину: в предшественниках нейронов при репликационном стрессе сгруппированные разрывы в длинных, активно используемых генах выступают центральными узлами, от которых возникают как распространённые, так и редкие варианты числа копий. Эти структурные изменения не мимолётны — они фиксируются в дочерних клетках, способствуя диверсификации геномов клеток развивающегося мозга и, при неблагоприятных условиях, питая эволюцию опухолей. Связав хрупкие генные регионы, репликационный стресс и конкретные пути ремонта, исследование предлагает механистический мост между повседневными ошибками копирования ДНК и сложными паттернами структурной вариабельности, наблюдаемыми при неврологических заболеваниях и опухолях.
Цитирование: Corazzi, L., Ing, A., Benito, E. et al. Recurrent DNA break clusters drive replication-stress-induced copy number variants and genome diversification. Nat Commun 17, 3627 (2026). https://doi.org/10.1038/s41467-026-71790-5
Ключевые слова: варианты числа копий, репликационный стресс, предшественники нейронов, кластеры разрывов ДНК, нестабильность генома