Clear Sky Science · tr
Tekrarlayan DNA kırık kümeleri, replikasyon stresi kaynaklı kopya sayı varyantlarını ve genom çeşitlenmesini tetikler
DNA planımızdaki gizli değişiklikler
Vücudumuzdaki her hücre yaşamı boyunca DNA’sını milyarlarca kez kopyalar ve çoğu kez bu işlem kusursuz gerçekleşir. Ancak kopyalama mekanizması zorlandığında DNA parçaları kaybolabilir, çoğalabilir veya yeniden düzenlenebilir—bunlara kopya sayı varyantları denir. Bu değişiklikler beyin hastalıklarında ve kanserlerde yaygındır, fakat ilk ortaya çıkış mekanizmaları uzun süredir belirsiz kaldı. Bu çalışma merkezi bir suçluyu ortaya koyuyor: DNA kırıklarının biriktiği, uzun beyin genlerindeki özel zayıf noktalar, kalıcı genetik değişikliklerin çeşitli biçimlerine zemin hazırlıyor.
Genomun çatlama eğiliminde olduğu yerler
Araştırmacılar “tekrarlayan DNA‑kırık kümeleri”ne odaklandı; bunlar nöral progenitör hücrelerdeki çok uzun genlerin içindeki bölgeler—nöronlara dönüşen bölünen hücreler. Bu uzun genler yoğun biçimde kullanılır ve hücrenin DNA replikasyon takviminde geç kopyalanır, bu da onları özellikle savunmasız kılar. DNA polimerazları nazikçe yavaşlatılarak replikasyon stresi indükleyen bir ilaç kullanıldığında, ekip bütün genomun derin sekanslamasıyla nerelerin inceldiğini izledi. Küçük ama tutarlı DNA kayıpları ve daha keskin, odaklı delesyonların bu kırılmaya yatkın bölgelerde yoğunlaştığını; bunların tesadüfen beklenenden çok daha sık görüldüğünü saptadılar.
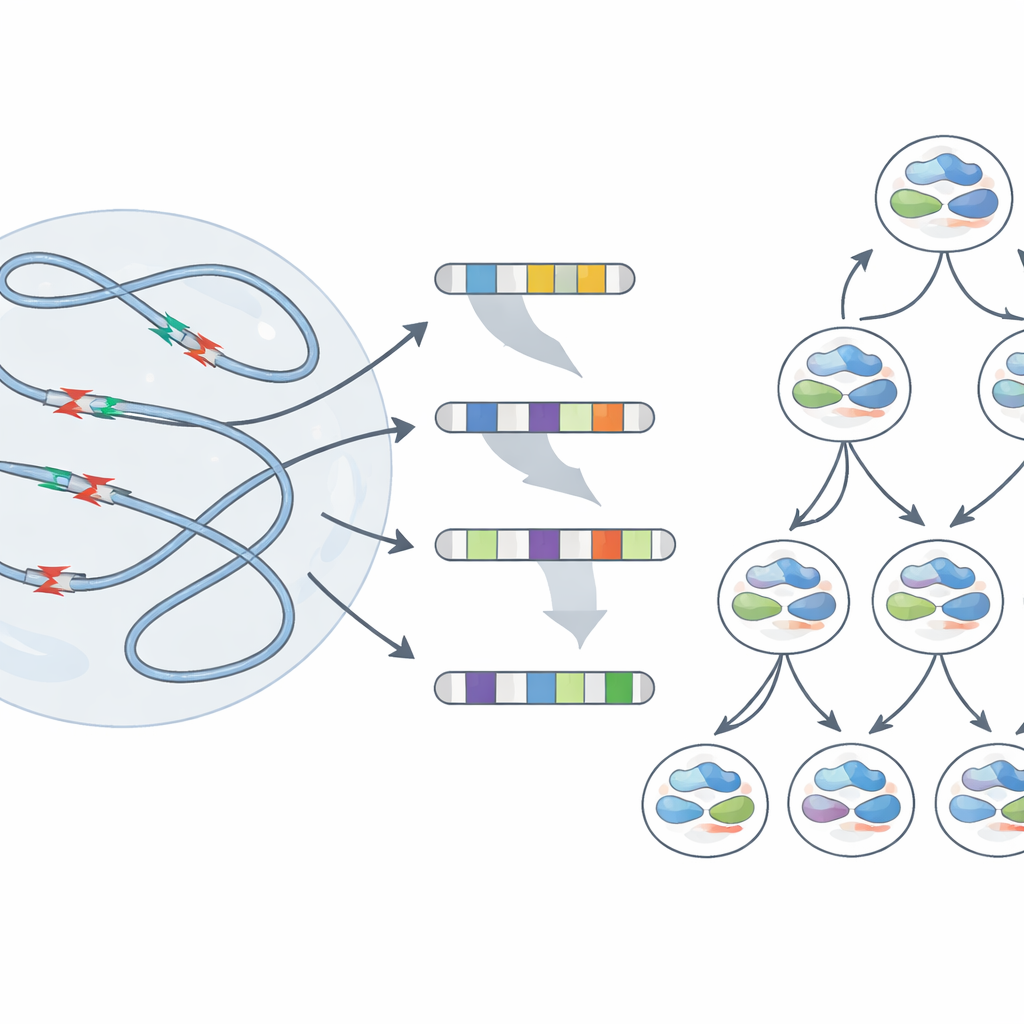
Geçici kırıklardan kalıcı izlere
Toplu sekanslama milyonlarca hücre genelindeki ortalama davranışı gösterir, ama tek bir hücrede neler olduğunu açığa çıkarmaz. Bireysel genomların strese nasıl yanıt verdiğini görmek için ekip, her kız hücrenin hangi orijinal DNA ipliklerini miras aldığını izleyen tek‑hücre yöntemleri kullandı. Replikasyon stresinden sonra birçok hücre milyonlarca DNA harfine yayılan büyük delesyonlar ve hatta tamamı kromozom kolu kayıpları taşıyordu. Önemli olarak, bu büyük değişikliklerin kırılma noktaları sıklıkla daha önce tespit edilen aynı zayıf bölgelerle örtüşüyordu. Bazen tek bir stresli atadan türeyen kardeş hücreler çok farklı yeniden düzenlenmelere sahip oluyordu—bu da bu sıcak noktalarda tek bir hasar olayının kız hücreleri genetik olarak farklı yollara sokabileceğinin kanıtı.
Transkripsiyon, kırılgan bölgeleri mutasyon fabrikalarına çeviriyor
Yazarlar sonra bu bölgeleri bu kadar özel kılanın ne olduğunu sordular. CRISPR araçlarını kullanarak kırık kümelerine ev sahipliği yaptığı bilinen iki dev beyin geninin yerel açıcılarını (promoter ve enhancer’ları) kapattılar. Transkripsiyonu kapattıklarında, karakteristik kırık kümeleri kayboldu ve ilişkili delesyonlar replikasyon stresi altında bile artık oluşmadı. Dikkate değer olarak, bu bölgelerdeki DNA replikasyonunun zamanlaması geç ya da biraz daha geç kalmaya devam etti; bu da önemli olanın hücre döngüsünde “ne zaman” kopyalandıkları değil, aktif kullanım ile kopyalanmanın birleşimi olduğunu gösteriyor. Başka bir deyişle, uzun genlerin kopyalanırken aynı anda transkribe edilmesi çatışma bölgeleri yaratıyor; bu çatışmalar kırılmalara yol açıyor ve bu kırılmalar kopya sayı varyantlarının tohumlarını oluşturuyor.
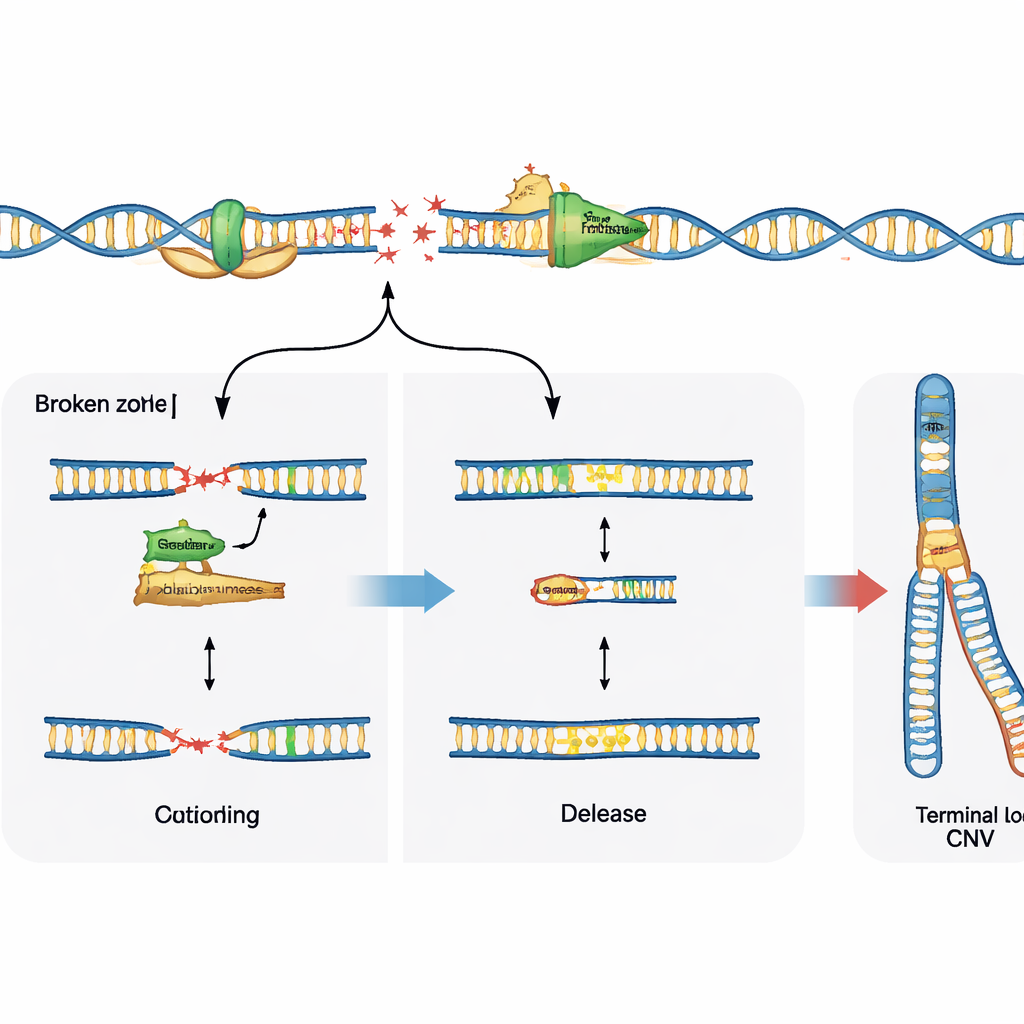
Onarım tercihleri sonucu yönlendirir
DNA kırılması hikâyenin yalnızca yarısıdır; hücrenin bu kırıkları nasıl onardığı nihai varyasyon desenini şekillendirir. Çalışma, kırık DNA uçlarını yamalayıp birleştirdiği bilinen özel bir enzim olan polimeraz theta’nın rolünü inceledi. Ana onarım yolu olan eş olmayan uç birleşimi (non‑homologous end joining) eksik olan nöral progenitör hücrelerde, polimeraz theta’yı engellemek kırılgan bölgelerdeki tipik tekrarlayan delesyonları keskin şekilde azalttı; bu, bu durumda enzimin kopya sayı değişikliklerini aktif olarak teşvik ettiğini gösteriyor. Buna karşılık, sağlam onarım sistemlerine sahip normal hücrelerde polimeraz theta inhibisyonu bu delesyonları engellemedi, bunun yerine kırılgan bölgelerde daha fazla ham DNA kırığı ortaya çıkardı. Bu, polimeraz theta’nın diğer onarım seçenekleri yokken genomun yeniden şekillenmesini destekleyebileceğini; ana onarım mekanizması mevcut olduğunda ise çatalları stabilize etmeye ve görünen hasarı sınırlamaya yardımcı olabileceğini düşündürüyor.
Bunun beyin sağlığı ve kanser için önemi
Bir araya getirildiğinde, bu çalışma net bir tablo çiziyor: replikasyon stresi altındaki nöral progenitör hücrelerde, uzun ve aktif olarak kullanılan genlerde kümelenmiş kırıklar hem yaygın hem de nadir kopya sayı varyantlarının merkezi merkezleri olarak davranıyor. Bu yapısal değişiklikler geçici değildir; kız hücrelerde sabitlenerek gelişen beyin hücrelerinin genomlarını çeşitlendiriyor ve uygun olmayan koşullarda kanser evrimini besleyebiliyor. Kırılgan gen bölgelerini, replikasyon stresini ve belirli onarım yollarını birbirine bağlayarak çalışma, günlük DNA kopyalama hataları ile nörolojik hastalıklar ve tümörlerde görülen karmaşık yapısal varyasyon desenleri arasında mekanistik bir köprü sunuyor.
Atıf: Corazzi, L., Ing, A., Benito, E. et al. Recurrent DNA break clusters drive replication-stress-induced copy number variants and genome diversification. Nat Commun 17, 3627 (2026). https://doi.org/10.1038/s41467-026-71790-5
Anahtar kelimeler: kopya sayı varyantları, replikasyon stresi, nöral progenitör hücreler, DNA kırık kümeleri, genom istikrarı