Clear Sky Science · zh
借助噬菌体辅助的全osteric 蛋白开关进化
将蛋白质变成开/关开关
想象一下能够在活细胞内拨动一个分子级的电灯开关——随意打开或关闭基因、酶或信号通路。本文描述了科学家如何构建一个进化“训练场”,教会蛋白质像这样的开关那样工作。通过利用感染细菌的病毒以及巧妙的选择策略,研究团队进化出对光有强烈响应的蛋白质,为研究、生物技术乃至潜在医学应用提供了强大的新工具。
为什么远程控制蛋白质重要
蛋白质是驱动细胞运作的微小机器。许多蛋白质天生具有变构性,意思是蛋白质上某处的变化——由糖、化学物质或光等信号触发——会在另一处远端引起功能上的转变。科学家希望重新设计这种内在连线,使几乎任何蛋白质都能被选定的输入(例如蓝光)控制。然而这很难:当研究者仅仅将一个传感域拼接到一个功能蛋白上时,嵌合体往往变得乏力、有泄漏或几乎没有响应。问题在于变构的“规则”分布在许多相互作用的残基和构象中,单凭设计很难准确预测。
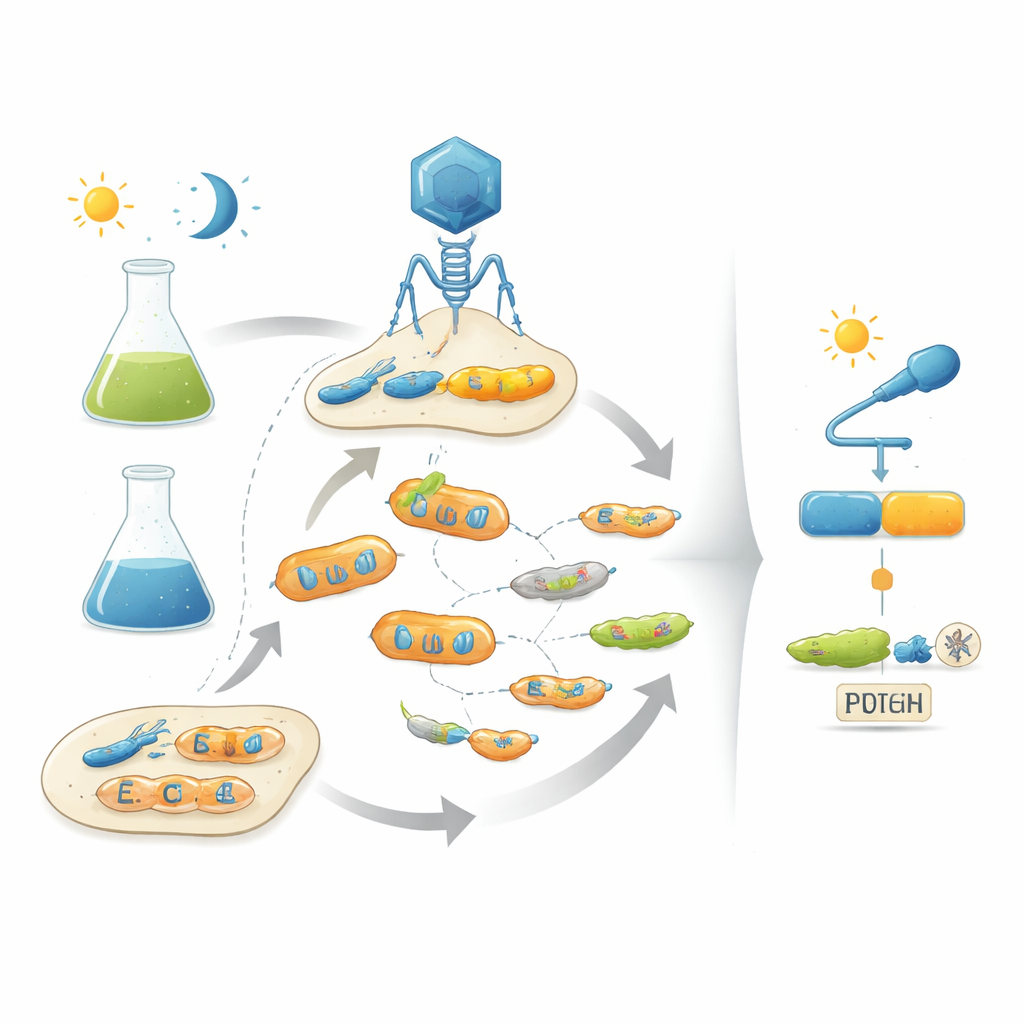
借用进化的剧本
作者通过在实验室中模仿自然进化来解决这一问题,使用噬菌体——感染细菌的病毒。他们的平台称为 POGO-PANCE,将每个噬菌体的成败与其编码的蛋白作为开关的表现联系起来。在一个阶段,如果蛋白在期望的条件下活性(例如在暗处),噬菌体就繁荣。在相反的阶段,如果蛋白在本该关闭时仍然活跃(例如在光照下),会产生一种破坏性的病毒成分版本,导致该噬菌体谱系崩溃。通过在不断变异蛋白的同时交替执行这些正向和负向选择步骤,系统将病毒群体逐步推向既强大又受输入信号严格控制的变体。
训练蛋白对光作出响应
为演示他们的方法,研究者聚焦于 AraC,一种研究透彻的细菌蛋白,通常对糖类阿拉伯糖作出响应以控制基因表达。首先,他们对 AraC 本身进行进化,使其即便在没有天然糖触发的情况下也能强烈活化,提供一个“高功率”的起点。接着,他们在预测能允许变构通讯的位置将一个蓝光敏感模块(称为 LOV 结构域)插入 AraC。起初,这种融合几乎破坏了 AraC:功能微弱,仅在过表达时显示出弱的光响应。然而,将这些残弱的杂交体置于 POGO-PANCE 中运行后,情况迅速改观。经过数轮在光与暗之间交替的选择,团队获得的变体几乎像数字开关一样,基因活性在暗与照明状态之间约有一千倍的变化。
窥见分子开关的连线
由于进化的蛋白被编码在噬菌体基因组上,研究者可以在每个循环后测序病毒群体。这揭示了哪些突变在不同选择步骤中兴起或衰落,追踪有效开关出现的路径。他们发现改变不仅出现在 AraC 和光传感器中,也出现在连接它们的短链接肽上。利用第二个工具 RAMPhaGE(基于 retron 引导的基因组编辑),他们通过添加、删除或互换小段氨基酸系统性地重塑这些连接肽。进化反复偏好那些使 LOV 结构域一侧的连接肽延伸成平滑螺旋、物理上桥接传感器与效应器的变体。这表明一段连续、对齐良好的螺旋有助于将光诱导的构象变化通过蛋白传递,从而使开/关响应更为锋利。
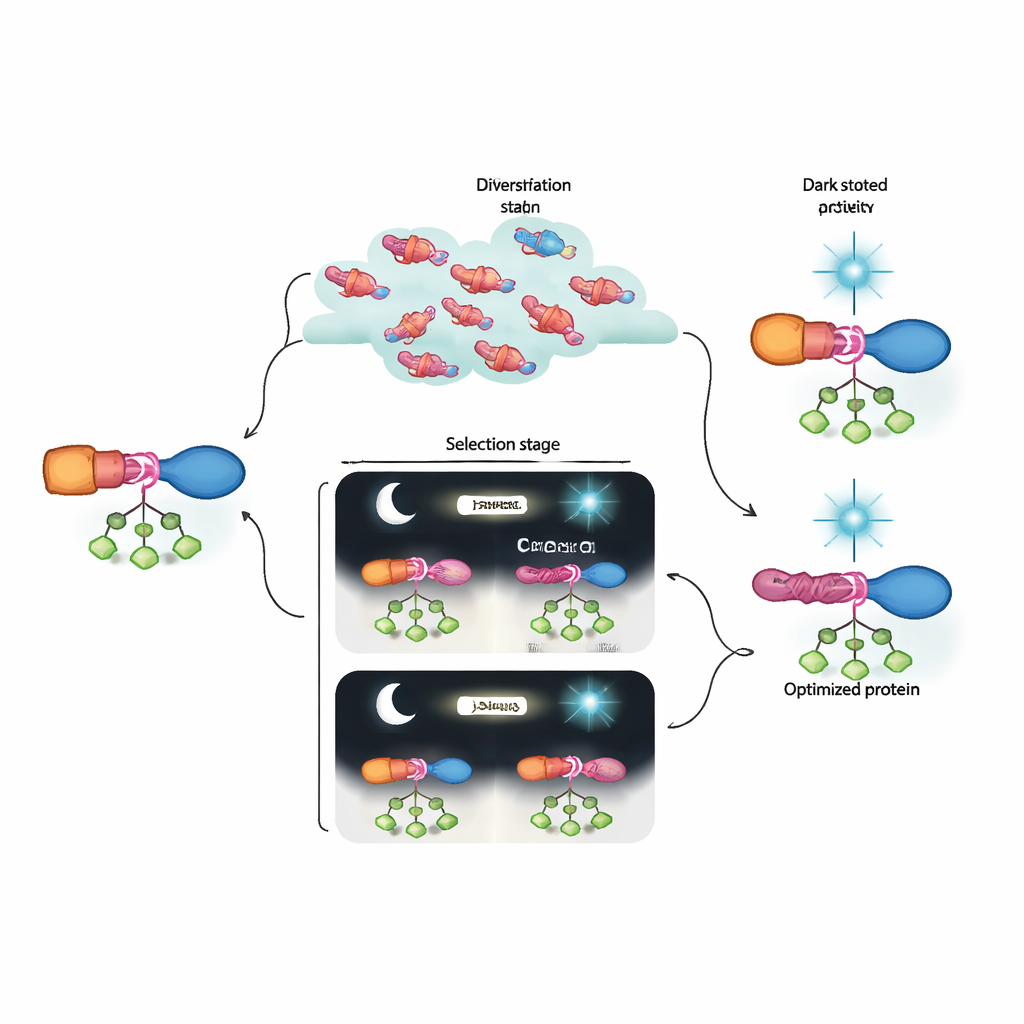
这对未来生物工程的意义
通俗地说,作者构建了一个实验室级的“进化机器”,能够发现并优化远超当前设计工具易于产生的蛋白开关。他们进化得到的 AraC–LOV 杂交体在需要时表现出强烈活性,并在蓝光下几乎完全关闭,优于早期的光遗传学版本。同样重要的是,动态选择与深度测序的结合揭示了微妙突变群如何协同构建变构通路。这一框架可被改编用于许多其他信号输入和蛋白目标,令我们更接近于用电子器件般的精确度编程细胞过程的未来,而这些组件正是由进化自身帮助设计的。
引用: Southern, N.T., von Bachmann, A., Hovsepyan, A. et al. Phage-assisted evolution of allosteric protein switches. Nat Commun 17, 3498 (2026). https://doi.org/10.1038/s41467-026-71717-0
关键词: 光遗传学, 定向进化, 变构调控, 蛋白质工程, 细菌噬菌体