Clear Sky Science · ru
Фаг-опосредованная эволюция аллостерических переключателей белков
Превращение белков в выключатели «включено–выключено»
Представьте, что можно щелкнуть молекулярный выключатель внутри живой клетки — включать и выключать гены, ферменты или сигнальные пути по желанию. В этой работе описывается, как учёные построили эволюционную «тренировочную площадку», которая учит белки вести себя как такие переключатели. Используя вирусы, инфицирующие бактерии, и хитрую стратегию отбора, команда эволюционирует белки, резко реагирующие на свет, что открывает мощные новые инструменты для исследований, биотехнологий и, возможно, медицины.
Почему важно дистанционное управление белками
Белки — это малые машины, управляющие жизнью клетки. Многие из них естественно аллостерические: изменение в одной части молекулы — вызванное, например, сахаром, химическим веществом или светом — вызывает функциональный сдвиг в другой, удалённой части. Учёные стремятся перестроить эту встроенную проводку так, чтобы почти любой белок можно было контролировать выбранным сигналом, например синим светом. Но это оказалось сложной задачей: если просто прицепить сенсорный домен к рабочему белку, гибрид часто получается слабым, с протечками или почти неотзывчивым. Проблема в том, что «правила» аллостерии распределены по многим взаимодействующим остаткам и конформациям, и их трудно предсказать только проектированием.
Заимствуя рецепты эволюции
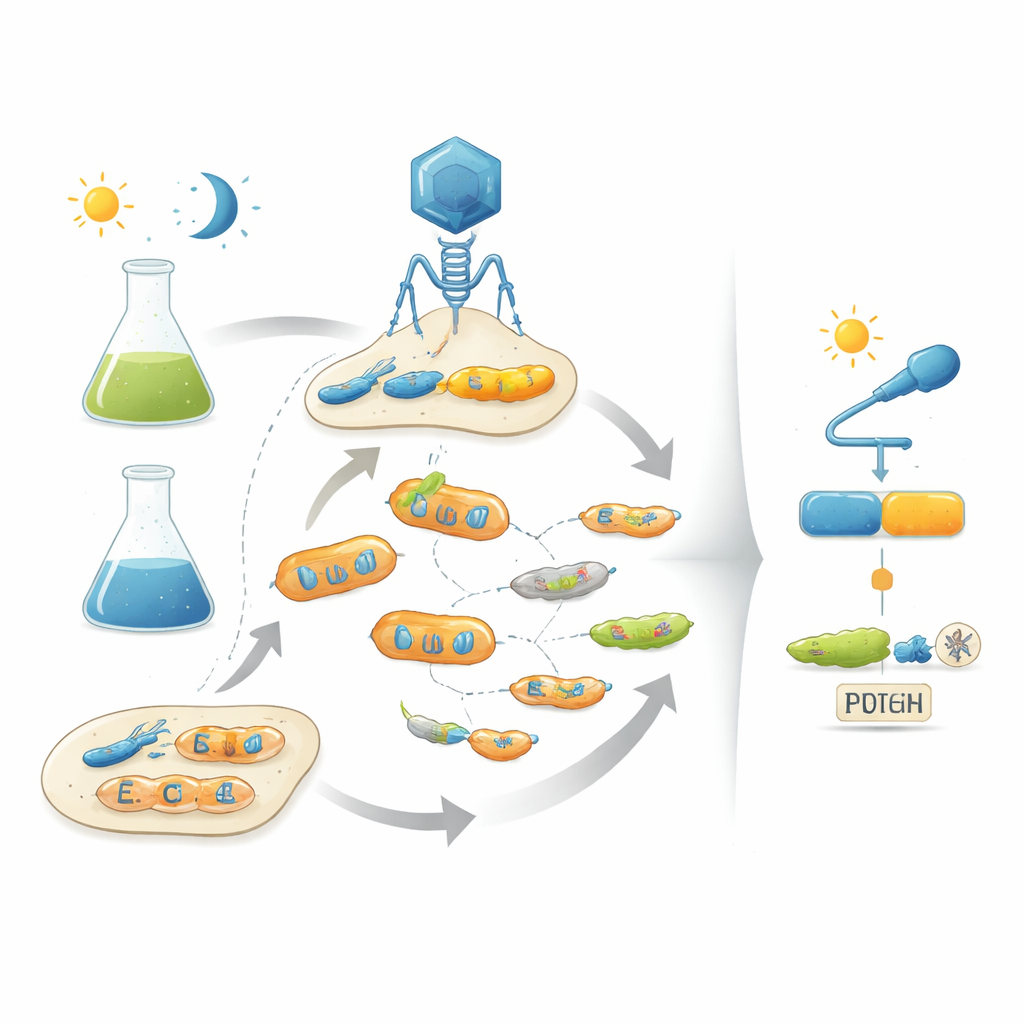
Авторы решают эту проблему, имитируя естественную эволюцию в лаборатории с помощью бактериофагов — вирусов, инфицирующих бактерии. Их платформа, названная POGO-PANCE, связывает успех каждого фага с тем, насколько хорошо кодируемый им белок действует как переключатель. В одной фазе, если белок активен при желаемом условии (например, в темноте), фаг процветает. В противоположной фазе, если белок активен тогда, когда он должен быть выключен (например, при освещении), производится саботирующая версия вирусного компонента, и соответствующая линия фага рушится. Чередуя эти положительный и отрицательный отборы при постоянном введении мутаций в белок, система подталкивает популяции фагов к вариантам, которые одновременно мощны и строго контролируются входным сигналом.
Обучение белка реагировать на свет
Чтобы продемонстрировать стратегию, исследователи сосредоточились на AraC — хорошо изученном бактериальном белке, который обычно реагирует на сахар арабинозу, контролируя экспрессию генов. Сначала они эволюционируют сам AraC так, чтобы он стал сильно активен даже без естественного сахара, получив «мощную» отправную точку. Затем они вставляют в AraC светочувствительный модуль LOV, чувствительный к синему свету, в сайт, предсказанный как допускающий аллостерическую связь. Первоначально такой фьюжн почти разрушает AraC: он едва функционирует и проявляет слабую световую отзывчивость только при сильной сверхэкспрессии. Однако пропускание этих ослабленных гибридов через POGO-PANCE быстро их преображает. После нескольких циклов чередующегося отбора в светлых и тёмных условиях команда получает варианты, которые ведут себя почти как цифровые переключатели: активность гена меняется примерно в тысячу раз между тёмным и освещённым состояниями.
Заглядывая в проводку молекулярного переключателя
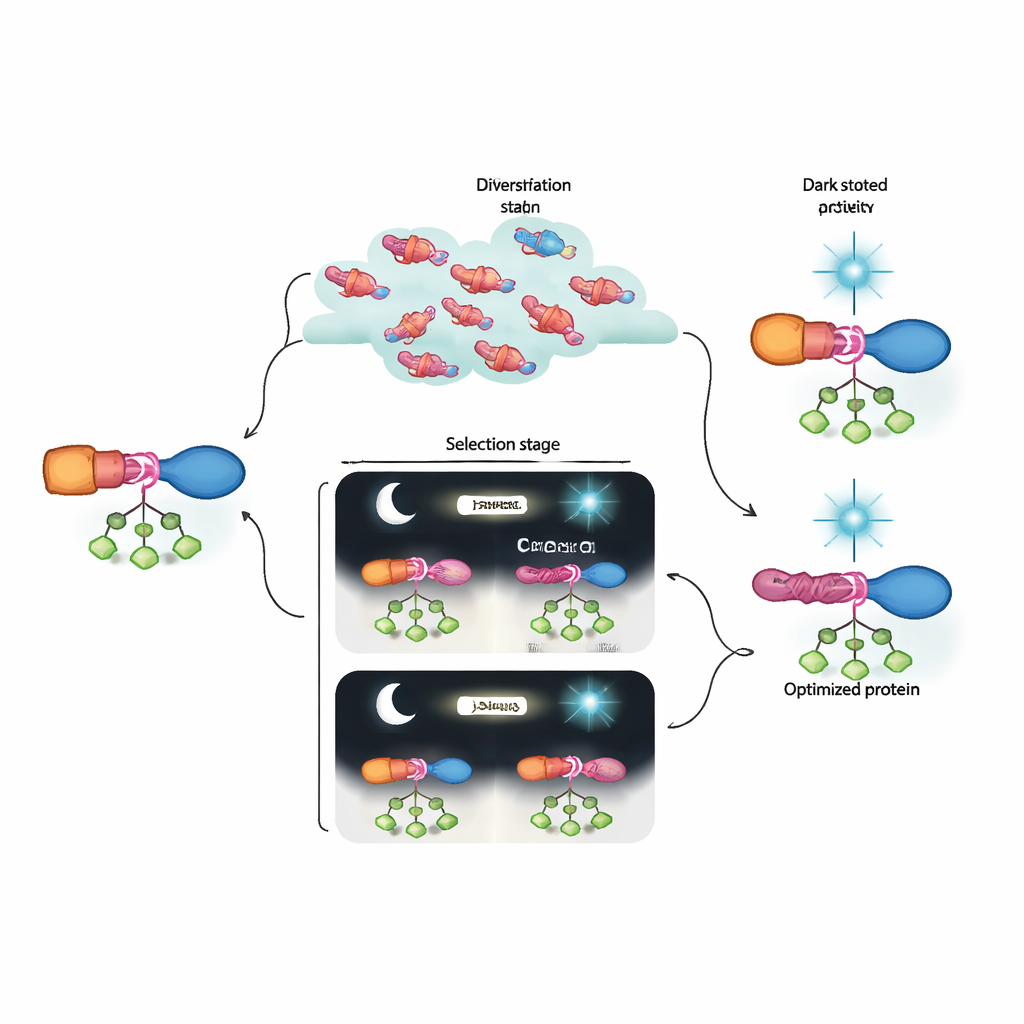
Поскольку эволюционирующие белки кодируются в геноме фага, исследователи могут секвенировать популяции вирусов после каждого цикла. Это показывает, какие мутации растут или исчезают при разных шагах отбора, отслеживая пути, по которым возникают эффективные переключатели. Они находят изменения не только в AraC и сенсоре света, но и в коротких линкерах, которые их соединяют. С помощью второго инструмента, RAMPhaGE, основанного на ретрон-направленном редактировании генома, они систематически перестраивают эти линкеры, добавляя, удаляя или меняя небольшие участки аминокислот. Эволюция неоднократно отбирает варианты, где линкер с одной стороны домена LOV выпрямляется в гладкую спираль, физически связывающую сенсор и эффектор. Это предполагает, что непрерывная, хорошо выровненная спираль помогает передавать свет-индуцированное изменение формы через белок, делая ответ более резким — «вкл/выкл».
Что это значит для будущего биоинжиниринга
Проще говоря, авторы создали лабораторную «эволюционную машину», которая может открывать и улучшать белковые переключатели гораздо дальше, чем позволяют современные инструменты проектирования. Полученные гибриды AraC–LOV демонстрируют сильную активность при необходимости и почти полностью выключаются под синим светом, превосходя ранние оптогенетические версии. Не менее важно, что сочетание динамического отбора и глубокого секвенирования показывает, как группы тонких мутаций взаимодействуют, чтобы сформировать аллостерический путь. Эта платформа может быть адаптирована к многим другим сигналам и белковым мишеням, приближая нас к будущему, где клеточные процессы можно программировать с точностью электронных схем, но используя компоненты, которые сама эволюция помогла разработать.
Цитирование: Southern, N.T., von Bachmann, A., Hovsepyan, A. et al. Phage-assisted evolution of allosteric protein switches. Nat Commun 17, 3498 (2026). https://doi.org/10.1038/s41467-026-71717-0
Ключевые слова: оптогенетика, направленная эволюция, аллостерическая регуляция, инжиниринг белков, бактериофаг