Clear Sky Science · es
Evolución asistida por fagos de interruptores proteicos alostéricos
Convertir proteínas en interruptores de encendido y apagado
Imagínese poder accionar un interruptor molecular dentro de una célula viva: encender y apagar genes, enzimas o vías de señalización a voluntad. Este artículo describe cómo los científicos construyeron un “campo de entrenamiento” evolutivo que enseña a las proteínas a comportarse como esos interruptores. Aprovechando virus que infectan bacterias y una estrategia de selección ingeniosa, el equipo evoluciona proteínas que responden de forma nítida a la luz, ofreciendo herramientas potentes para la investigación, la biotecnología y, potencialmente, la medicina.
Por qué importa el control remoto de las proteínas
Las proteínas son las diminutas máquinas que hacen funcionar nuestras células. Muchas son alostéricas de forma natural, lo que significa que un cambio en un punto de la proteína —inducido por una señal como un azúcar, un químico o la luz— provoca un cambio funcional en otro punto distante. Los científicos desean rediseñar este cableado interno para que casi cualquier proteína pueda controlarse mediante una entrada elegida, como la luz azul. Sin embargo, esto ha resultado difícil: cuando los investigadores simplemente acoplan un dominio sensor a una proteína funcional, el quimérico suele volverse débil, con fugas o apenas sensible. El reto es que las “reglas” de la alostería están repartidas entre muchos residuos y conformaciones interdependientes, lo que dificulta predecirlas solo por diseño.
Tomando prestado el libro de jugadas de la evolución
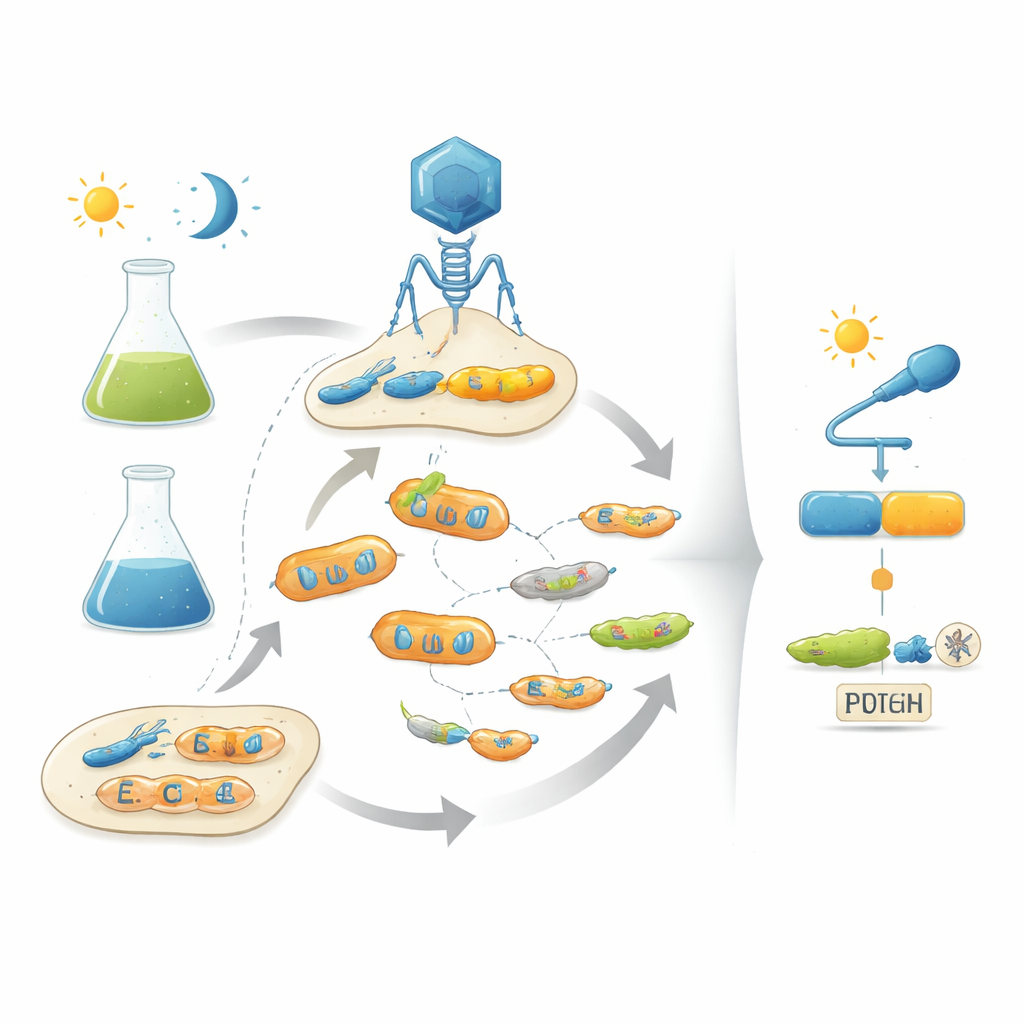
Los autores abordan este problema imitando la evolución natural en el laboratorio mediante bacteriófagos —virus que infectan bacterias. Su plataforma, llamada POGO-PANCE, vincula el éxito de cada fago a lo bien que su proteína codificada funciona como interruptor. En una fase, si la proteína está activa bajo la condición deseada (por ejemplo, en la oscuridad), el fago prospera. En la fase opuesta, si la proteína está activa cuando debería estar apagada (por ejemplo, bajo luz), se produce una versión saboteadora de un componente viral y la línea de fagos infractora colapsa. Alternando estos pasos de selección positiva y negativa mientras la proteína muta constantemente, el sistema empuja a las poblaciones virales hacia variantes que son tanto potentes como controladas de forma estricta por la señal de entrada.
Entrenar una proteína para responder a la luz
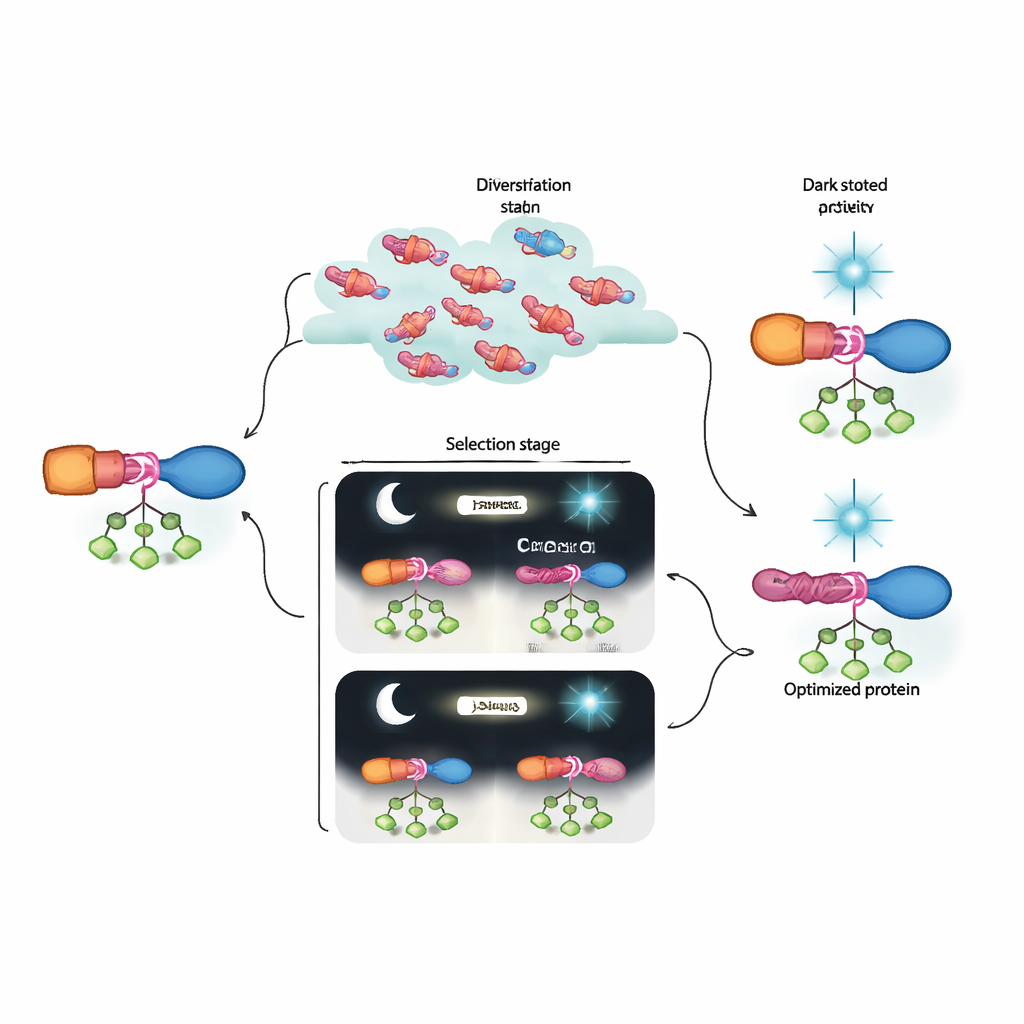
Para demostrar su estrategia, los investigadores se centran en AraC, una proteína bacteriana bien estudiada que normalmente responde al azúcar arabinosa para controlar la expresión génica. Primero, evolucionan AraC para que se vuelva fuertemente activa incluso sin su desencadenante natural, proporcionando un punto de partida “de alta potencia”. A continuación, insertan un módulo sensible a la luz azul, conocido como dominio LOV, en AraC en un sitio predicho para permitir la comunicación alostérica. Inicialmente, esta fusión casi rompe AraC: funciona apenas y sólo muestra una débil respuesta a la luz cuando se sobreexpresa. Sin embargo, someter estos híbridos debilitados a POGO-PANCE los transforma rápidamente. Tras varias rondas de selección alternante bajo luz y oscuridad, el equipo recupera variantes que se comportan casi como interruptores digitales, con la actividad génica cambiando alrededor de mil veces entre los estados oscuro e iluminado.
Escudriñando el cableado de un interruptor molecular
Puesto que las proteínas en evolución están codificadas en el genoma del fago, los investigadores pueden secuenciar las poblaciones virales tras cada ciclo. Esto revela qué mutaciones suben y bajan bajo los distintos pasos de selección, trazando las rutas por las que emergen interruptores eficaces. Encuentran que aparecen cambios no solo en AraC y en el sensor de luz, sino también en los cortos enlazadores que los conectan. Usando una segunda herramienta, RAMPhaGE, basada en la edición genómica guiada por retrones, remodelan sistemáticamente estos enlazadores añadiendo, eliminando o intercambiando pequeños tramos de aminoácidos. La evolución favorece repetidamente variantes donde el enlazador en un lado del dominio LOV se extiende en una hélice suave que une físicamente sensor y efector. Esto sugiere que una hélice continua y bien alineada ayuda a transmitir el cambio conformacional inducido por la luz a través de la proteína, afinando la respuesta de encendido y apagado.
Qué significa esto para la futura bioingeniería
En términos sencillos, los autores han construido una “máquina de evolución” en el laboratorio que puede descubrir y refinar interruptores proteicos mucho más allá de lo que las herramientas de diseño actuales pueden producir con facilidad. Sus híbridos AraC–LOV evolucionados muestran una fuerte actividad cuando se necesita y se apagan casi por completo bajo luz azul, superando versiones optogenéticas anteriores. Igualmente importante, la combinación de selección dinámica y secuenciación profunda revela cómo grupos de mutaciones sutiles cooperan para construir una vía alostérica. Este marco podría adaptarse a muchos otros estímulos y objetivos proteicos, acercándonos a un futuro en el que los procesos celulares puedan programarse con la precisión de los circuitos electrónicos, pero usando componentes que la propia evolución ha ayudado a diseñar.
Cita: Southern, N.T., von Bachmann, A., Hovsepyan, A. et al. Phage-assisted evolution of allosteric protein switches. Nat Commun 17, 3498 (2026). https://doi.org/10.1038/s41467-026-71717-0
Palabras clave: optogenética, evolución dirigida, regulación alostérica, ingeniería de proteínas, bacteriófago