Clear Sky Science · pl
Ewolucja wspomagana fagami prowadząca do alosterycznych przełączników białkowych
Przekształcanie białek w przełączniki wł./wył.
Wyobraź sobie, że możesz pstryknąć molekularnym wyłącznikiem światła wewnątrz żywej komórki — włączać i wyłączać geny, enzymy lub szlaki sygnałowe na żądanie. W artykule opisano, jak naukowcy zbudowali ewolucyjne „treningowe pole”, które uczy białka zachowywać się jak takie przełączniki. Wykorzystując wirusy atakujące bakterie i sprytne strategie selekcji, zespół ewoluuje białka reagujące gwałtownie na światło, tworząc potężne nowe narzędzia dla badań, biotechnologii i potencjalnie medycyny.
Dlaczego zdalne sterowanie białkami ma znaczenie
Białka to drobne maszyny kierujące komórkami. Wiele z nich jest naturalnie alosterycznych — zmiana w jednym miejscu białka, wywołana sygnałem takim jak cukier, związek chemiczny czy światło, powoduje zmianę funkcji gdzie indziej w tym samym białku. Naukowcy chcieliby przeprojektować tę wbudowaną „okablowanie”, aby niemal każde białko mogło być kontrolowane przez wybrane wejście, na przykład niebieskie światło. To jednak jest trudne: gdy badacze po prostu doklejają domenę sensoryczną do działającego białka, chimera często staje się słaba, nieszczelna lub słabo reagująca. Problem polega na tym, że „zasady” alosterii rozproszone są po wielu współdziałających resztach i kształtach, co utrudnia przewidywanie ich jedynie metodami projektowania.
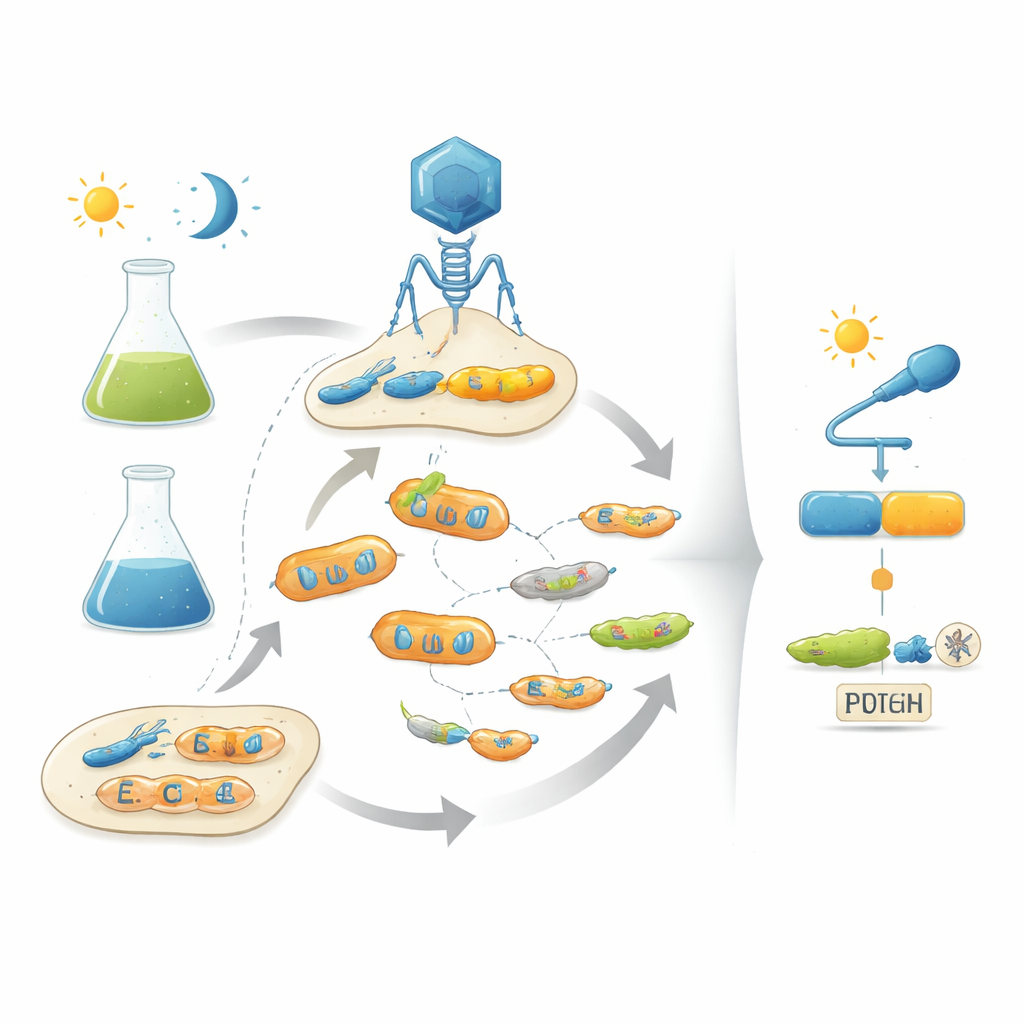
Korzystanie ze scenariusza ewolucji
Autorzy rozwiązują ten problem, naśladując naturalną ewolucję w laboratorium przy użyciu bakteriofagów — wirusów zakażających bakterie. Ich platforma, nazwana POGO-PANCE, powiązuje powodzenie każdego phaga z tym, jak dobrze zakodowane przez niego białko działa jako przełącznik. W jednej fazie, jeśli białko jest aktywne w pożądanym warunku (na przykład w ciemności), phag prosperuje. W przeciwnej fazie, jeśli białko jest aktywne wtedy, gdy powinno być wyłączone (na przykład w świetle), produkowana jest sabotująca wersja składnika wirusa i dany klon phaga upada. Przeplatając te pozytywne i negatywne kroki selekcyjne przy jednoczesnym ciągłym mutowaniu białka, system kieruje populacje wirusowe ku wariantom, które są zarówno silne, jak i ściśle kontrolowane przez sygnał wejściowy.
Trenowanie białka do reagowania na światło
Aby pokazać strategię, badacze skupiają się na AraC, dobrze poznanym białku bakteryjnym, które normalnie reaguje na cukier arabinozę, kontrolując ekspresję genów. Najpierw ewoluują samo AraC, aby stało się silnie aktywne nawet bez naturalnego liganda — zapewnia to „wysokoprądowy” punkt wyjścia. Następnie wstawiają moduł czuły na niebieskie światło, znany jako domena LOV, do AraC w miejscu przewidzianym jako umożliwiające komunikację alosteryczną. Początkowo taka fuzja niemal rujnuje AraC: działa słabo i wykazuje jedynie minimalną responsywność na światło przy nadprodukcji. Jednak przepuszczenie tych uszkodzonych hybryd przez POGO-PANCE szybko je transformuje. Po kilku rundach naprzemiennej selekcji w świetle i w ciemności zespół odzyskuje warianty zachowujące się niemal jak cyfrowe przełączniki, z aktywnością genów zmieniającą się około tysiąckrotnie między stanami ciemnym i oświetlonym.
Zaglądanie w okablowanie molekularnego przełącznika
Ponieważ ewoluujące białka są zakodowane w genomie phaga, badacze mogą sekwencjonować populacje wirusowe po każdym cyklu. To ujawnia, które mutacje rosną lub maleją w różnych etapach selekcji, śledząc ścieżki, dzięki którym powstają skuteczne przełączniki. Stwierdzają, że zmiany pojawiają się nie tylko w AraC i sensorze światła, lecz także w krótkich łącznikach łączących je. Korzystając z drugiego narzędzia, RAMPhaGE, opartego na edycji genomu kierowanej retronami, systematycznie przekształcają te łączniki poprzez dodawanie, usuwanie lub zamianę krótkich odcinków aminokwasów. Ewolucja wielokrotnie faworyzuje warianty, w których łącznik po jednej stronie domeny LOV rozwija się w gładką helisę, fizycznie łączącą sensor z elementem efektorowym. Sugeruje to, że ciągła, dobrze wyrównana helisa pomaga przenosić wywołaną światłem zmianę kształtu przez białko, wyostrzając reakcję wł./wył.
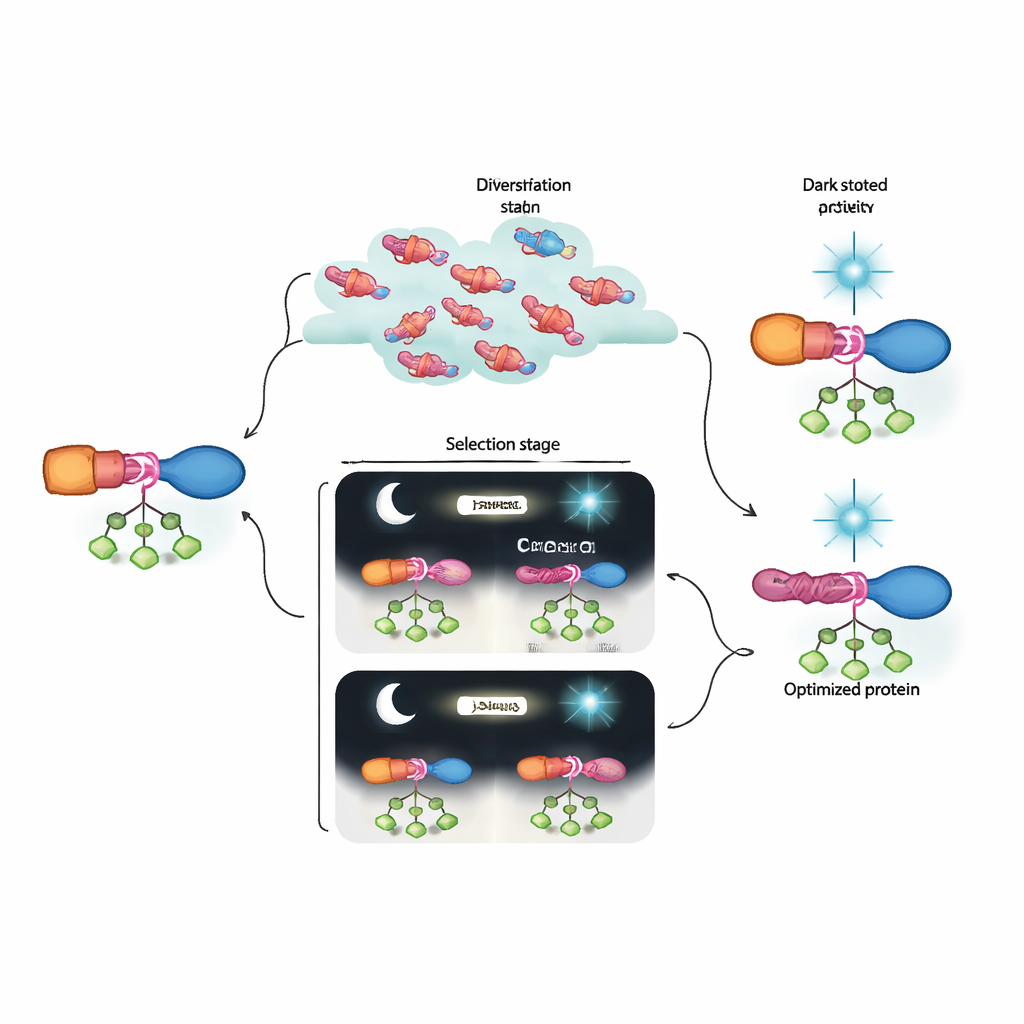
Co to oznacza dla przyszłej bioinżynierii
Mówiąc wprost, autorzy zbudowali laboratoryjną „maszynę ewolucyjną”, która potrafi odkrywać i dopracowywać przełączniki białkowe znacznie poza możliwościami łatwego projektowania. Ewoluowane hybrydy AraC–LOV wykazują silną aktywność, gdy jest potrzebna, i niemal całkowicie wyłączają się pod wpływem niebieskiego światła, przewyższając wcześniejsze wersje optogenetyczne. Równie ważne, połączenie dynamicznej selekcji i głębokiego sekwencjonowania ujawnia, jak grupy subtelnych mutacji współpracują, by zbudować ścieżkę alosteryczną. Ramy te można zaadaptować do wielu innych sygnałów i celów białkowych, przybliżając nas do przyszłości, w której procesy komórkowe da się programować z precyzją obwodów elektronicznych, lecz za pomocą elementów zaprojektowanych przez samą ewolucję.
Cytowanie: Southern, N.T., von Bachmann, A., Hovsepyan, A. et al. Phage-assisted evolution of allosteric protein switches. Nat Commun 17, 3498 (2026). https://doi.org/10.1038/s41467-026-71717-0
Słowa kluczowe: opto-genetyka, ewolucja ukierunkowana, regulacja alosteryczna, inżynieria białek, bakteriofag