Clear Sky Science · sv
Fag-assisterad evolution av allosteriska proteinswitchar
Göra proteiner till av–på-brytare
Föreställ dig att du kan slå om en molekylär ljusbrytare inne i en levande cell—styra gener, enzymer eller signalvägar av och på när du vill. Den här artikeln beskriver hur forskare byggt en evolutionär ”träningsarena” som lär proteiner att uppträda som sådana brytare. Genom att utnyttja virus som infekterar bakterier och en fiffig selektionsstrategi utvecklar teamet proteiner som svarar skarpt på ljus, vilket ger kraftfulla nya verktyg för forskning, bioteknik och potentiellt medicin.
Varför fjärrstyrning av proteiner är viktig
Proteiner är de små maskinerna som driver våra celler. Många av dem är naturligt allosteriska, vilket innebär att en förändring på en plats i proteinet—utlöst av en signal som ett socker, en kemikalie eller ljus—orsakar en funktionell förändring på en annan, avlägsen plats. Forskare vill omprogrammera denna inbyggda koppling så att nästan vilket protein som helst kan styras av en vald ingång, till exempel blått ljus. Det har visat sig svårt: när forskare helt enkelt fäster en sensordomän på ett fungerande protein blir ofta kimen svag, läckande eller knappt responsiv. Utmaningen är att reglerna för allosteri är utspridda över många interagerande restämnen och strukturer, vilket gör dem svåra att förutsäga enbart genom design.
Låna evolutionens handbok
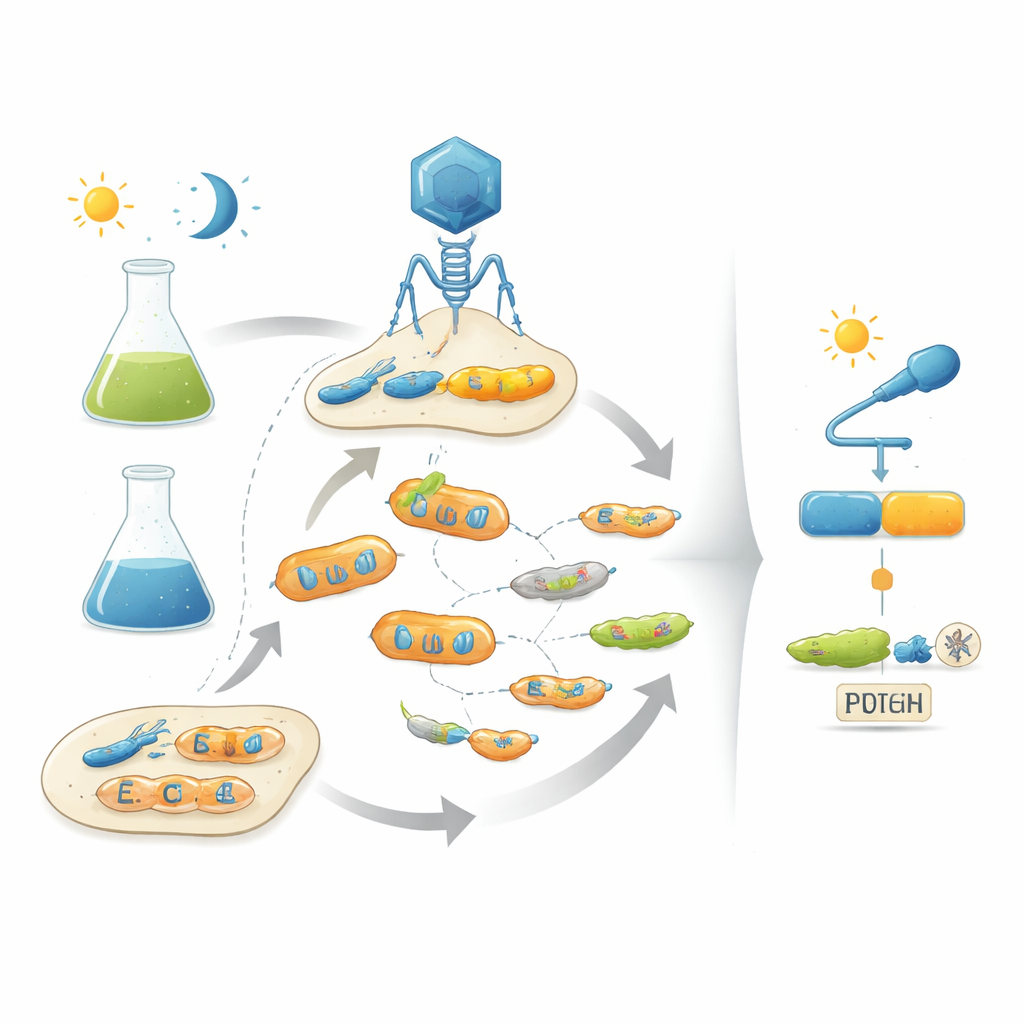
Författarna angriper problemet genom att efterlikna naturlig evolution i labbet med hjälp av bakteriofager—virus som infekterar bakterier. Deras plattform, kallad POGO-PANCE, kopplar varje fags framgång till hur väl dess kodade protein beter sig som en brytare. I en fas, om proteinet är aktivt under det önskade tillståndet (till exempel i mörker), gynnas fagen. I motsatt fas, om proteinet är aktivt när det borde vara av (till exempel under ljus), produceras en sabotageliknande version av en viral komponent och den aktuella faglinjen kollapsar. Genom att alternera dessa positiva och negativa selektionssteg samtidigt som proteinet ständigt muterar, styr systemet viruspopulationer mot varianter som både är kraftfulla och tajt kontrollerade av ingångssignalen.
Träna ett protein att reagera på ljus
För att demonstrera sin strategi fokuserar forskarna på AraC, ett välstuderat bakteriellt protein som normalt reagerar på sockret arabinos för att kontrollera genuttryck. Först utvecklar de AraC självt för att bli starkt aktivt även utan sitt naturliga sockertrigg, vilket ger en ”högpresterande” utgångspunkt. Därefter infogar de en blåljuskänslig modul, känd som en LOV-domän, i AraC på en plats som förutspåtts tillåta allosterisk kommunikation. Inledningsvis nästan förstör denna fusionskonstruktion AraC: den fungerar knappt och visar endast svag ljusrespons när den överproduceras. Genom att köra dessa försvagade hybrider genom POGO-PANCE förvandlas de dock snabbt. Efter flera omgångar av alternerande selektion under ljus och mörker återfår teamet varianter som beter sig nästan som digitala brytare, med genaktivitet som ändras ungefär tusenfalt mellan mörka och upplysta tillstånd.
Skåda ledningarna i en molekylär brytare
Eftersom de evolverande proteinerna kodas på fagens genom kan forskarna sekvensera viruspopulationerna efter varje cykel. Detta visar vilka mutationer som stiger och faller under olika selektionssteg och spårar vägarna genom vilka effektiva brytare uppstår. De finner att förändringar uppträder inte bara i AraC och ljussensorn utan också i de korta länkar som förenar dem. Med ett andra verktyg, RAMPhaGE, baserat på retronstyrd genomredigering, omformar de systematiskt dessa länkar genom att lägga till, ta bort eller byta ut korta stretchar av aminosyror. Evolutionen favoriserar upprepade gånger varianter där länken på ena sidan av LOV-domänen förlängs till en jämn helix som fysiskt binder sensor och effektor. Detta tyder på att en kontinuerlig, väljusterad helix hjälper till att överföra ljusinducerad formförändring genom proteinet och skärper av–på-responsen.
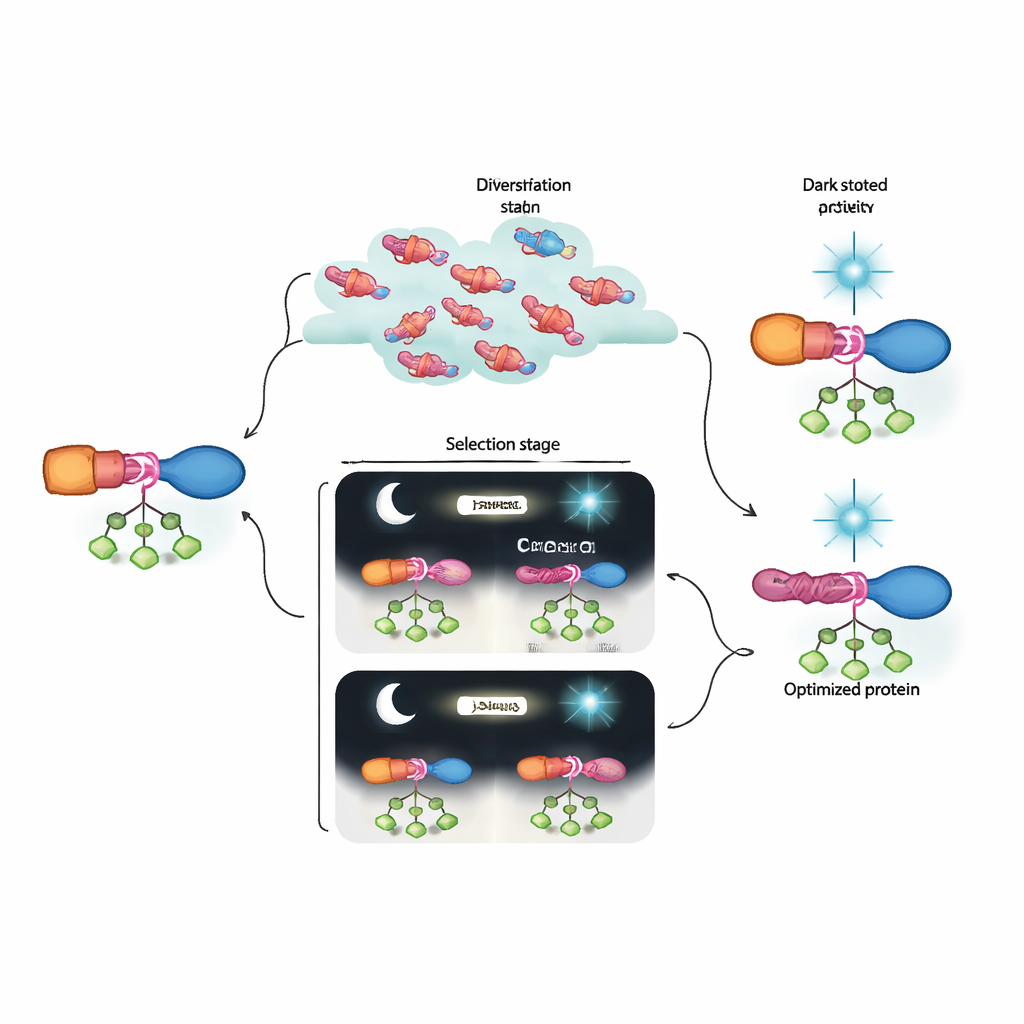
Vad detta betyder för framtidens bioengineering
Enkelt uttryckt har författarna byggt en labbbaserad ”evolutionsmaskin” som kan upptäcka och förfina proteinswitchar långt utöver vad nuvarande desig nverktyg lätt kan producera. Deras utvecklade AraC–LOV-hybrider visar stark aktivitet när det behövs och stängs nästan helt av under blått ljus, och överträffar tidigare optogenetiska versioner. Lika viktigt är att kombinationen av dynamisk selektion och djupsekvensering avslöjar hur grupper av subtila mutationer samverkar för att bygga en allosterisk väg. Denna ram kan anpassas till många andra signalingångar och proteintmål, och för oss närmare en framtid där cellulära processer kan programmeras med precisionen hos elektroniska kretsar—men med komponenter som evolutionen själv hjälpt till att utforma.
Citering: Southern, N.T., von Bachmann, A., Hovsepyan, A. et al. Phage-assisted evolution of allosteric protein switches. Nat Commun 17, 3498 (2026). https://doi.org/10.1038/s41467-026-71717-0
Nyckelord: optogenetik, styrd evolution, allosterisk reglering, proteinarkitektur, bakteriofag