Clear Sky Science · it
Evoluzione assistita da fagi di interruttori proteici allosterici
Trasformare le proteine in interruttori on–off
Immaginate di poter azionare un interruttore molecolare all’interno di una cellula vivente, accendendo e spegnendo geni, enzimi o vie di segnalazione a comando. Questo articolo descrive come gli scienziati abbiano costruito un “campo di addestramento” evolutivo che insegna alle proteine a comportarsi come tali interruttori. Sfruttando virus che infettano batteri e una strategia di selezione ingegnosa, il gruppo evolve proteine che rispondono in modo netto alla luce, offrendo strumenti potenti per la ricerca, la biotecnologia e, potenzialmente, la medicina.
Perché il controllo a distanza delle proteine è importante
Le proteine sono le piccole macchine che fanno funzionare le nostre cellule. Molte sono naturalmente allosteriche, cioè una modifica in un punto della proteina — innescata da un segnale come uno zucchero, una molecola chimica o la luce — provoca un cambiamento funzionale in un’altra regione distante. Gli scienziati vorrebbero riprogettare questo cablaggio intrinseco in modo che quasi qualsiasi proteina possa essere controllata da un input scelto, per esempio la luce blu. Ciò si è dimostrato difficile: quando i ricercatori semplicemente collegano un dominio sensore a una proteina funzionante, il chimerico spesso diventa debole, perde specificità o risponde poco. La sfida è che le “regole” dell’allosteria sono distribuite su molti residui e conformazioni che interagiscono, rendendole difficili da prevedere solo con il design.
Prendere in prestito il manuale dell’evoluzione
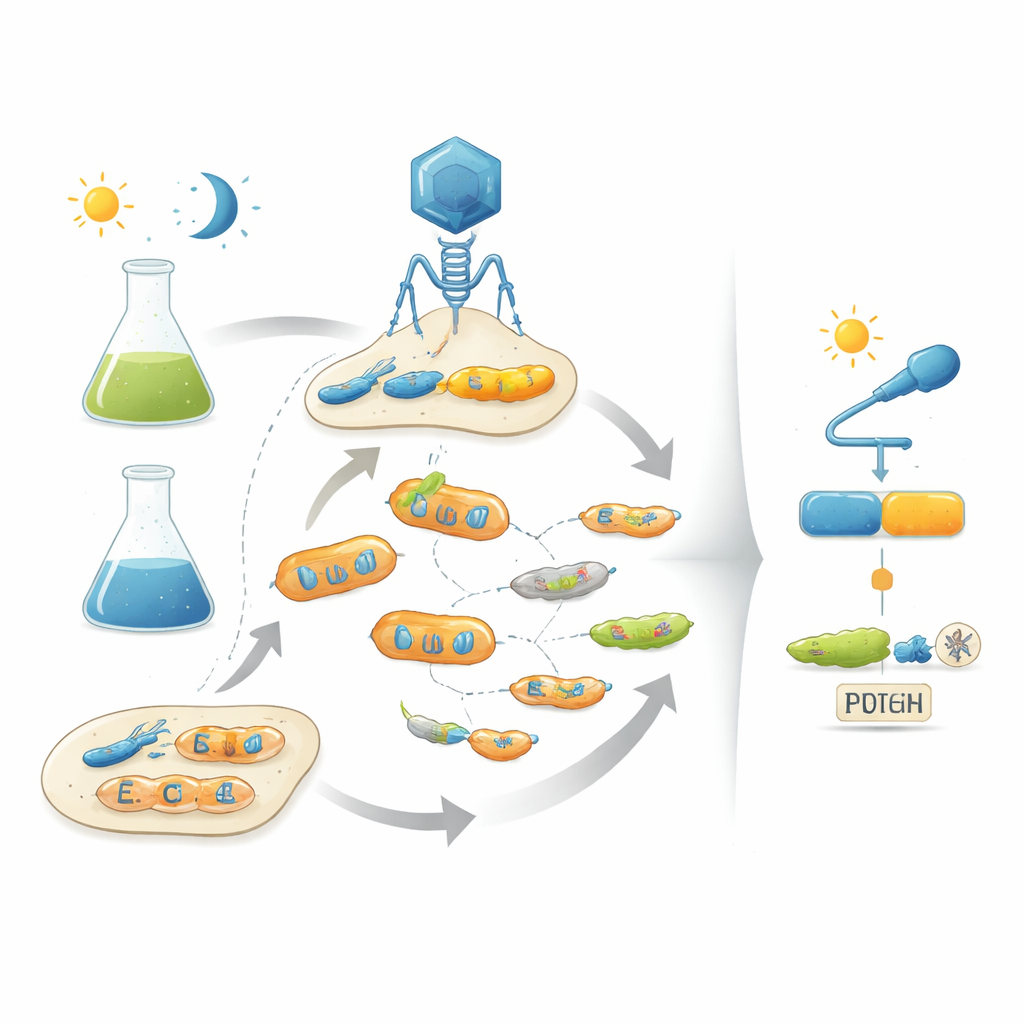
Gli autori affrontano il problema imitando l’evoluzione naturale in laboratorio usando batteriofagi — virus che infettano batteri. La loro piattaforma, chiamata POGO-PANCE, collega il successo di ciascun fago a quanto bene la proteina codificata funzioni come interruttore. In una fase, se la proteina è attiva nella condizione desiderata (per esempio al buio), il fago prospera. Nella fase opposta, se la proteina è attiva quando dovrebbe essere spenta (per esempio alla luce), viene prodotta una versione sabotante di un componente virale e la linea fagica colpevole crolla. Alternando questi passi di selezione positiva e negativa mentre la proteina è soggetta a mutazioni continue, il sistema spinge le popolazioni virali verso varianti potenti e strettamente regolate dall’input.
Addestrare una proteina a rispondere alla luce
Per dimostrare la loro strategia, i ricercatori si concentrano su AraC, una proteina batterica ben studiata che normalmente risponde allo zucchero arabinosio per controllare l’espressione genica. Prima evolvono AraC stesso per diventare fortemente attivo anche senza il suo attivatore naturale, ottenendo un punto di partenza “ad alta potenza”. Poi inseriscono in AraC un modulo sensibile alla luce blu, noto come dominio LOV, in un sito predetto capace di consentire comunicazione allosterica. Inizialmente questa fusione quasi compromette AraC: funziona a malapena e mostra solo una debole risposta alla luce quando è sovraespresso. Sottoponendo questi ibridi difettosi a POGO-PANCE, tuttavia, essi si trasformano rapidamente. Dopo diversi cicli di selezione alternata tra luce e buio, il gruppo recupera varianti che si comportano quasi come interruttori digitali, con l’attività genica che cambia di circa mille volte tra stato di buio e stato illuminato.
Scrutare il cablaggio di un interruttore molecolare
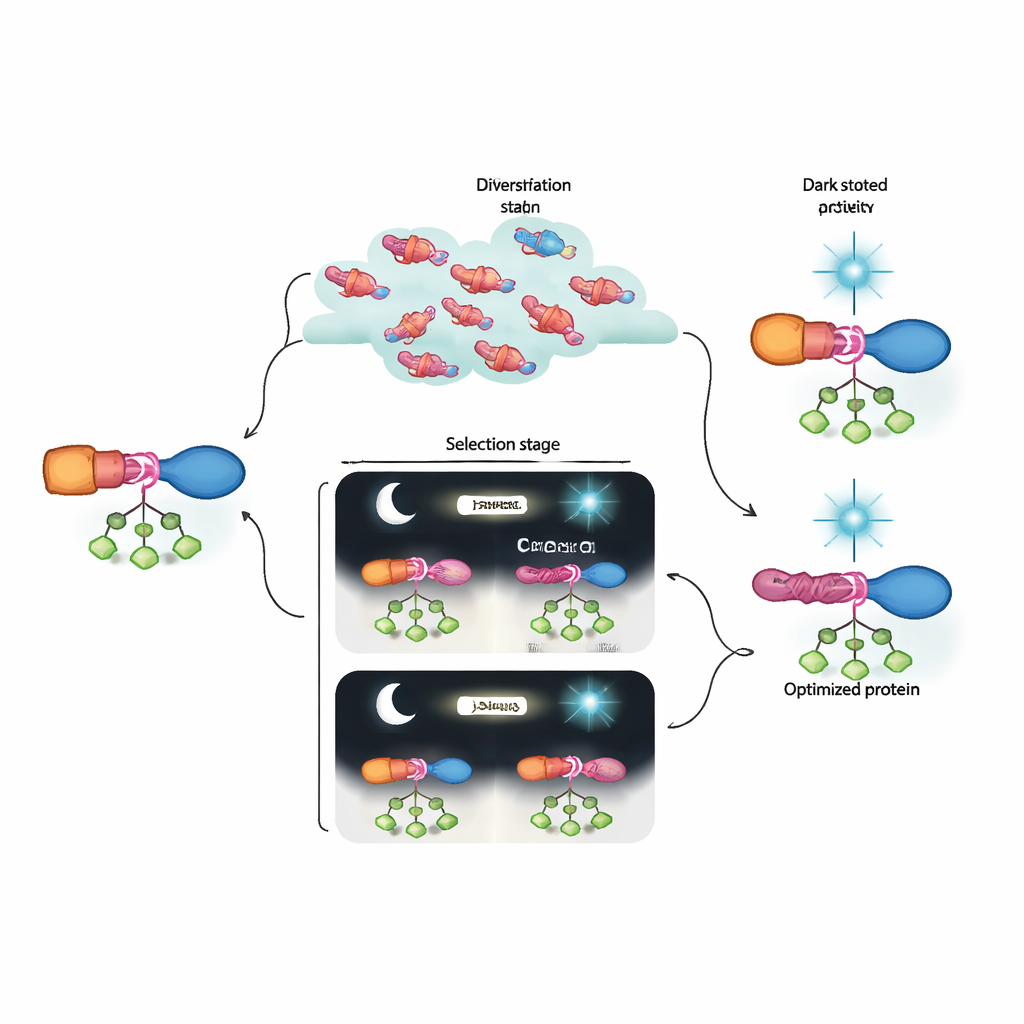
Poiché le proteine in evoluzione sono codificate sul genoma del fago, i ricercatori possono sequenziare le popolazioni virali dopo ogni ciclo. Questo rivela quali mutazioni aumentano o diminuiscono sotto i diversi passi di selezione, tracciando le vie con cui emergono interruttori efficaci. Riscontrano modifiche non solo in AraC e nel sensore di luce ma anche nei brevi linker che li collegano. Usando un secondo strumento, RAMPhaGE, basato su editing genomico guidato da retroni, rimodellano sistematicamente questi linker aggiungendo, rimuovendo o scambiando piccoli tratti di amminoacidi. L’evoluzione favorisce ripetutamente varianti in cui il linker su un lato del dominio LOV si estende in un’elica liscia che collega fisicamente sensore ed effettore. Ciò suggerisce che un’elica continua e ben allineata aiuti a trasmettere il cambiamento conformazionale indotto dalla luce attraverso la proteina, affinando la risposta on–off.
Cosa significa questo per l’ingegneria biologica futura
In termini semplici, gli autori hanno costruito una “macchina evolutiva” in laboratorio capace di scoprire e perfezionare interruttori proteici ben oltre quanto gli attuali strumenti di design possano facilmente ottenere. I loro ibridi AraC–LOV evoluti mostrano forte attività quando necessario e si spengono quasi completamente sotto luce blu, superando versioni optogenetiche precedenti. Altrettanto importante, la combinazione di selezione dinamica e sequenziamento profondo rivela come gruppi di mutazioni sottili cooperino per costruire un percorso allosterico. Questo quadro potrebbe essere adattato a molti altri input di segnalazione e bersagli proteici, avvicinandoci a un futuro in cui i processi cellulari possano essere programmati con la precisione dei circuiti elettronici, ma usando componenti che la stessa evoluzione ha contribuito a progettare.
Citazione: Southern, N.T., von Bachmann, A., Hovsepyan, A. et al. Phage-assisted evolution of allosteric protein switches. Nat Commun 17, 3498 (2026). https://doi.org/10.1038/s41467-026-71717-0
Parole chiave: optogenetica, evoluzione diretta, regolazione allosterica, ingegneria delle proteine, batteriofago