Clear Sky Science · pt
Evolução assistida por fagos de chaves proteicas alostéricas
Transformando Proteínas em Interruptores Liga–Desliga
Imagine poder acionar um interruptor molecular dentro de uma célula viva — ligando ou desligando genes, enzimas ou vias de sinalização à vontade. Este artigo descreve como cientistas construíram um “campo de treinamento” evolutivo que ensina proteínas a se comportarem como esses interruptores. Aproveitando vírus que infectam bactérias e uma estratégia de seleção engenhosa, a equipe evolui proteínas que respondem de forma nítida à luz, oferecendo novas ferramentas potentes para pesquisa, biotecnologia e, potencialmente, medicina.
Por que o Controle Remoto de Proteínas Importa
Proteínas são as pequenas máquinas que fazem as células funcionarem. Muitas delas são naturalmente alostéricas, o que significa que uma mudança em um ponto da proteína — desencadeada por um sinal como um açúcar, um composto químico ou luz — provoca uma alteração funcional em outro ponto distante. Cientistas gostariam de redesenhar essa fiação interna para que quase qualquer proteína pudesse ser controlada por um estímulo escolhido, como luz azul. Mas isso tem se mostrado difícil: quando pesquisadores simplesmente acoplam um domínio sensor a uma proteína funcional, o quimera frequentemente fica fraco, com vazamento de atividade ou pouco responsivo. O desafio é que as “regras” da alosteria estão espalhadas por muitos resíduos e conformações interativos, tornando-as difíceis de prever apenas por projeto racional.
Pegando o Manual de Evolução emprestado
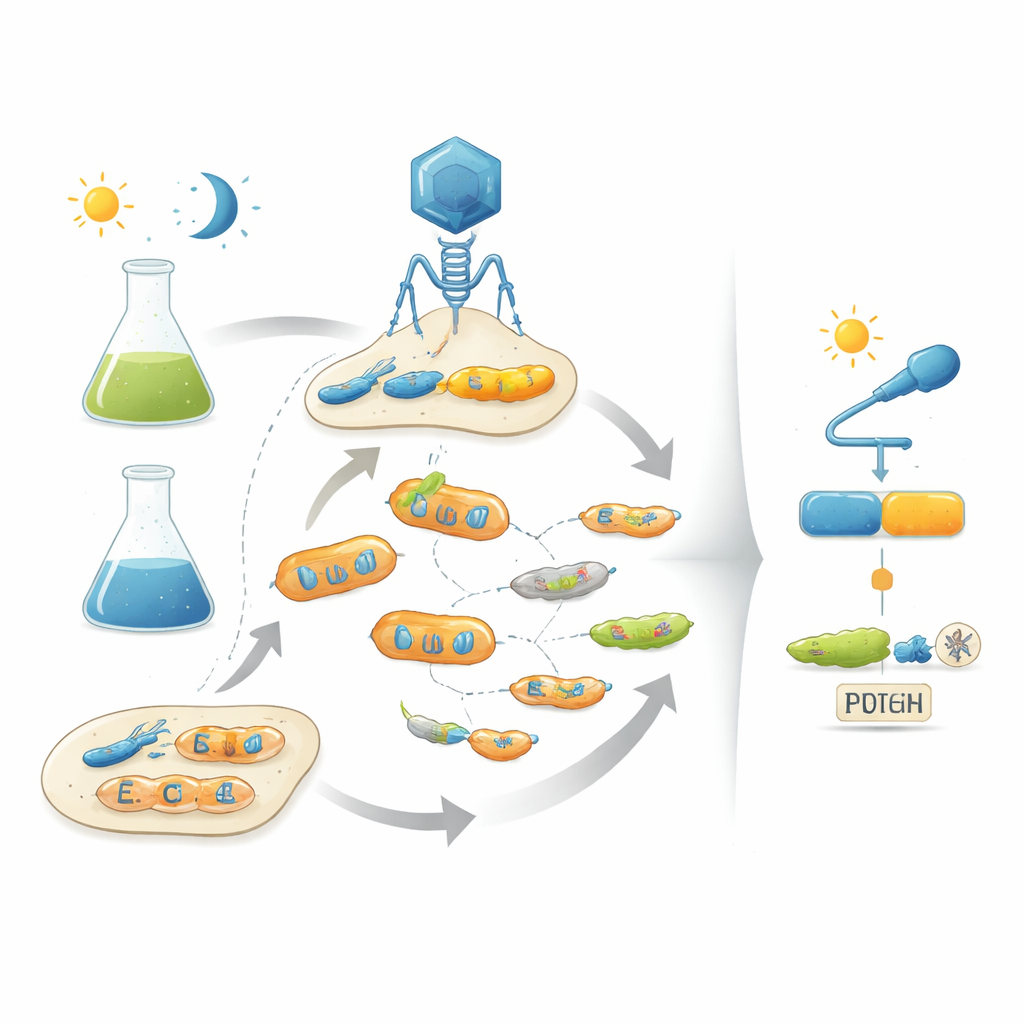
Os autores enfrentam esse problema imitando a evolução natural em laboratório usando bacteriófagos — vírus que infectam bactérias. A plataforma deles, chamada POGO-PANCE, liga o sucesso de cada fago à eficiência com que a proteína codificada age como um interruptor. Em uma fase, se a proteína está ativa nas condições desejadas (por exemplo, no escuro), o fago prospera. Na fase oposta, se a proteína fica ativa quando deveria estar desligada (por exemplo, sob luz), é produzida uma versão sabotadora de um componente viral, e a linhagem de fago ofensora colapsa. Alternando essas etapas de seleção positiva e negativa enquanto a proteína sofre mutações constantes, o sistema direciona as populações virais para variantes que são ao mesmo tempo potentes e estritamente controladas pelo sinal de entrada.
Treinando uma Proteína para Responder à Luz
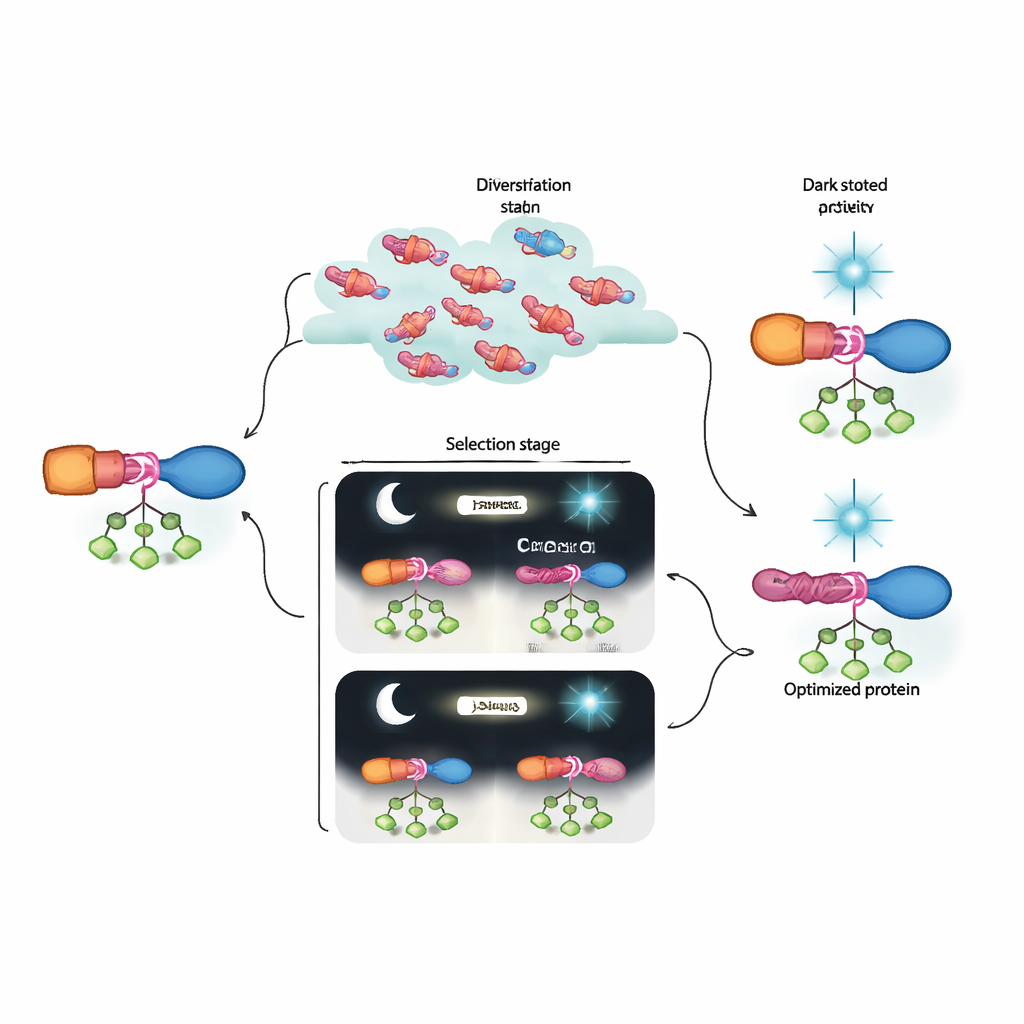
Para demonstrar a estratégia, os pesquisadores focam em AraC, uma proteína bacteriana bem estudada que normalmente responde ao açúcar arabinose para controlar a expressão gênica. Primeiro, eles evoluem a própria AraC para se tornar fortemente ativa mesmo sem o gatilho açucarado natural, fornecendo um ponto de partida “de alta potência”. Em seguida, inserem um módulo sensível à luz azul, conhecido como domínio LOV, na AraC em um sítio previsto para permitir comunicação alostérica. Inicialmente, essa fusão quase quebra a AraC: funciona mal e só mostra fraca responsividade à luz quando superexpressa. Submeter esses híbridos defeituosos ao POGO-PANCE, no entanto, os transforma rapidamente. Após várias rodadas de seleção alternada sob luz e escuridão, a equipe recupera variantes que se comportam quase como interruptores digitais, com a atividade gênica mudando cerca de mil vezes entre os estados escuro e iluminado.
Entrando na Fiação de um Interruptor Molecular
Como as proteínas em evolução estão codificadas no genoma do fago, os pesquisadores podem sequenciar as populações virais após cada ciclo. Isso revela quais mutações sobem e caem sob diferentes etapas de seleção, traçando os caminhos pelos quais interruptores eficazes emergem. Eles observam que mudanças aparecem não apenas em AraC e no sensor de luz, mas também nos curtos conectores (linkers) que os unem. Usando uma segunda ferramenta, RAMPhaGE, baseada em edição genômica guiada por retrons, eles remodelam sistematicamente esses linkers adicionando, removendo ou trocando pequenos trechos de aminoácidos. A evolução favorece repetidamente variantes onde o linker de um lado do domínio LOV se estende em um hélice contínua que conecta fisicamente sensor e efetor. Isso sugere que uma hélice contínua e bem alinhada ajuda a transmitir a mudança conformacional induzida pela luz através da proteína, aguçando a resposta liga–desliga.
O Que Isso Significa para a Bioengenharia Futura
Em termos simples, os autores construíram uma “máquina de evolução” em laboratório capaz de descobrir e refinar interruptores de proteína muito além do que as ferramentas de projeto atuais conseguem produzir com facilidade. Os híbridos AraC–LOV evoluídos mostram forte atividade quando necessário e desligam quase por completo sob luz azul, superando versões optogenéticas anteriores. Igualmente importante, a combinação de seleção dinâmica e sequenciamento profundo revela como grupos de mutações sutis cooperam para construir um caminho alostérico. Esse arcabouço poderia ser adaptado a muitos outros estímulos e alvos proteicos, aproximando-nos de um futuro em que processos celulares podem ser programados com a precisão de circuitos eletrônicos, mas usando componentes que a própria evolução ajudou a moldar.
Citação: Southern, N.T., von Bachmann, A., Hovsepyan, A. et al. Phage-assisted evolution of allosteric protein switches. Nat Commun 17, 3498 (2026). https://doi.org/10.1038/s41467-026-71717-0
Palavras-chave: optogenética, evolução dirigida, regulação alostérica, engenharia de proteínas, bacteriófago