Clear Sky Science · tr
Allosterik protein anahtarlarının bakteriyofaj destekli evrimi
Proteinleri Aç–Kapa Anahtarlarına Çevirmek
Yaşayan bir hücre içinde moleküler bir ışık anahtarını parmak hareketiyle açıp kapatabildiğinizi hayal edin—genleri, enzimleri veya sinyal yolaklarını isteğe bağlı olarak etkinleştirmek veya durdurmak. Bu makale, bilim insanlarının proteinleri böyle anahtarlara benzetmeyi öğreten evrimsel bir “eğitim alanı” nasıl kurduklarını anlatıyor. Bakterileri enfekte eden virüsleri ve zekice bir seçilim stratejisini kullanarak, ekip ışığa keskin şekilde yanıt veren proteinler geliştiriyor; bu, araştırma, biyoteknoloji ve potansiyel olarak tıp için güçlü yeni araçlar sunuyor.
Proteinlerin Uzaktan Kontrolünün Önemi
Proteinler hücrelerimizi çalıştıran küçük makineler gibidir. Birçoğu doğal olarak allosteriktir; yani proteindeki bir yerde—örneğin bir şeker, bir kimyasal veya ışığın tetiklemesiyle—meydana gelen değişiklik, uzaktaki başka bir yerde işlevsel bir kaymaya yol açar. Bilim insanları bu yerleşik devrelemeyi yeniden tasarlayıp neredeyse her proteini seçilmiş bir girişle, örneğin mavi ışıkla, kontrol edilebilir kılmak istiyor. Ancak bu zordur: araştırmacılar yalnızca bir sensör bölümü bir proteine eklediklerinde, kimerik yapı sıklıkla zayıf, sızıntılı veya neredeyse yanıtsız hale geliyor. Zorluk şu ki, allosterinin “kuralları” birçok etkileşen kalıntı ve şekil boyunca dağılmıştır; bu nedenle yalnızca tasarım yoluyla tahmin edilmesi güçtür.
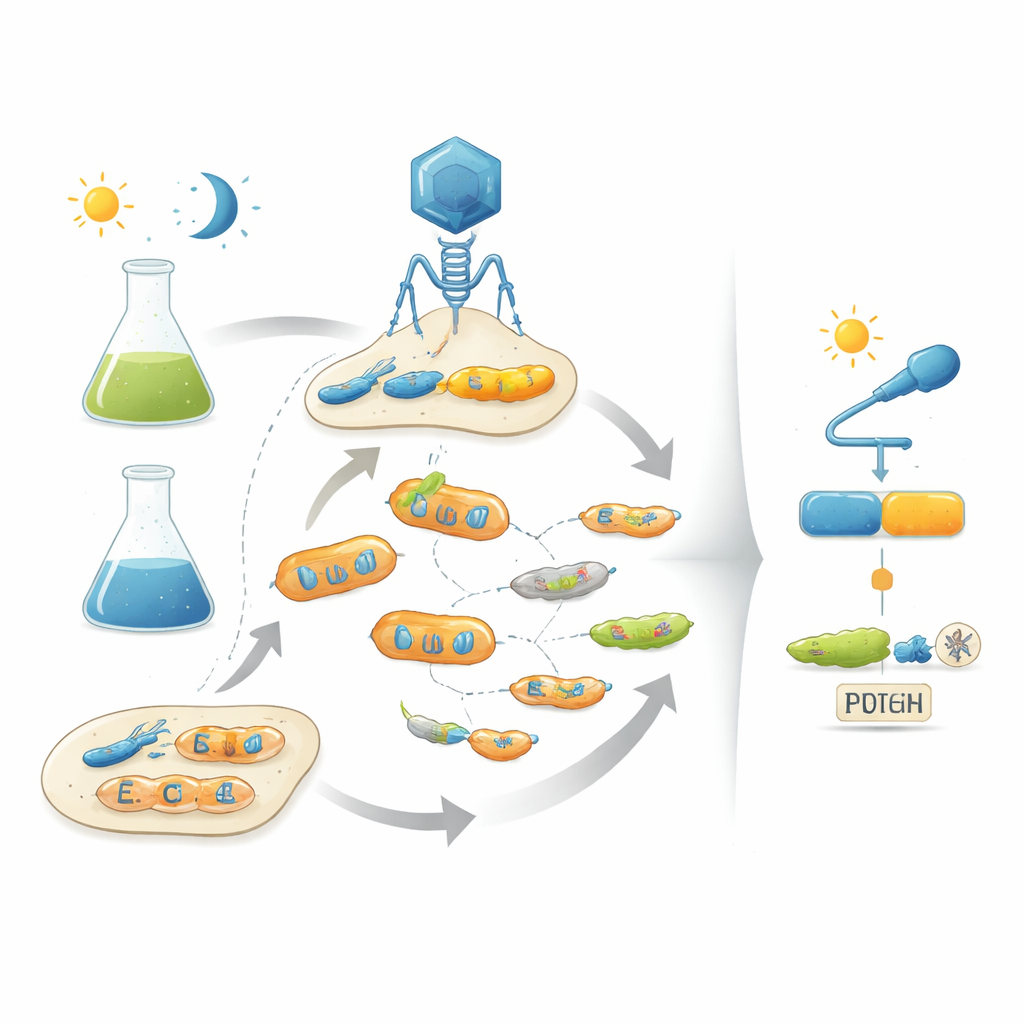
Evrimin Oyun Kitabını Ödünç Almak
Yazarlar bu sorunu, bakterileri enfekte eden virüsleri (bakteriyofajlar) kullanarak laboratuvarda doğal evrimi taklit ederek ele alıyor. POGO-PANCE adını verdikleri platformları, her fajın başarısını kodladığı proteinin bir anahtar gibi ne kadar iyi davrandığına bağlıyor. Bir aşamada, protein istenen koşulda (örneğin karanlıkta) aktifse faj başarılı oluyor. Karşı aşamada ise protein kapalı olması gerektiğinde (örneğin ışık altında) aktifse, viral bir bileşenin sabotaj edici bir versiyonu üretiliyor ve soruna yol açan faj hattı çökmeye başlıyor. Bu pozitif ve negatif seçilim adımlarını dönüşümlü uygulayıp proteini sürekli mutasyona tabi tutarak, sistem viral popülasyonları hem güçlü hem de giriş sinaliyle sıkı bir şekilde kontrol edilen varyantlara doğru yönlendiriyor.
Bir Proteini Işığa Yanıt Verecek Şekilde Eğitmek
Yöntemlerini göstermek için araştırmacılar, normalde şeker arabinozu ile yanıt verip gen ifadesini kontrol eden iyi çalışılmış bir bakteriyel protein olan AraC üzerinde yoğunlaşıyor. Önce, AraC’yi doğal şeker tetikleyicisi olmadan bile güçlü şekilde aktif olacak biçimde evrimleştiriyorlar ve bu “yüksek güçlü” bir başlangıç noktası sağlıyor. Ardından mavi ışığa duyarlı bir modül olan LOV domainini AraC’ye, allosterik iletişime izin verebileceği öngörülen bir noktaya yerleştiriyorlar. Başlangıçta bu füzyon AraC’yi neredeyse bozuyor: zayıf çalışıyor ve yalnızca aşırı üretildiğinde hafif ışık duyarlılığı gösteriyor. Ancak bu sakat hibritleri POGO-PANCE’den geçirerek hızla dönüştürüyorlar. Işık ve karanlık altında dönüşümlü seçilim turlarından sonra ekip, gen aktivitesinin karanlık ve aydınlatılmış durumlar arasında yaklaşık bin kat değiştiği, neredeyse dijital anahtarlar gibi davranan varyantlar elde ediyor.
Moleküler Bir Anahtarın Devrelerine Bakmak
Evrimleşen proteinler faj genomunda kodlandığı için araştırmacılar her döngü sonrasında viral popülasyonları dizileyebiliyor. Bu, hangi mutasyonların farklı seçilim adımları altında yükselip düştüğünü ortaya koyarak etkili anahtarların nasıl ortaya çıktığına dair yolları izlemeyi sağlıyor. Sadece AraC ve ışık sensöründe değil, onları birleştiren kısa bağlantılarda da değişiklikler görüyorlar. Retron ile yönlendirilen genom düzenlemeye dayanan RAMPhaGE adlı ikinci bir araç kullanarak, bu bağlantıları küçük amino asit dizileri ekleyip, çıkarıp veya değiştirerek sistematik olarak yeniden şekillendiriyorlar. Evrim, LOV domaininin bir tarafındaki bağlantının sensör ile efektörü fiziksel olarak birleştiren düzgün bir heliks halinde uzadığı varyantları tekrar tekrar favoriliyor. Bu, sürekli ve iyi hizalanmış bir heliksin ışıkla tetiklenen şekil değişikliğini protein boyunca iletmeye yardımcı olarak açma–kapama yanıtını keskinleştirdiğini düşündürür.
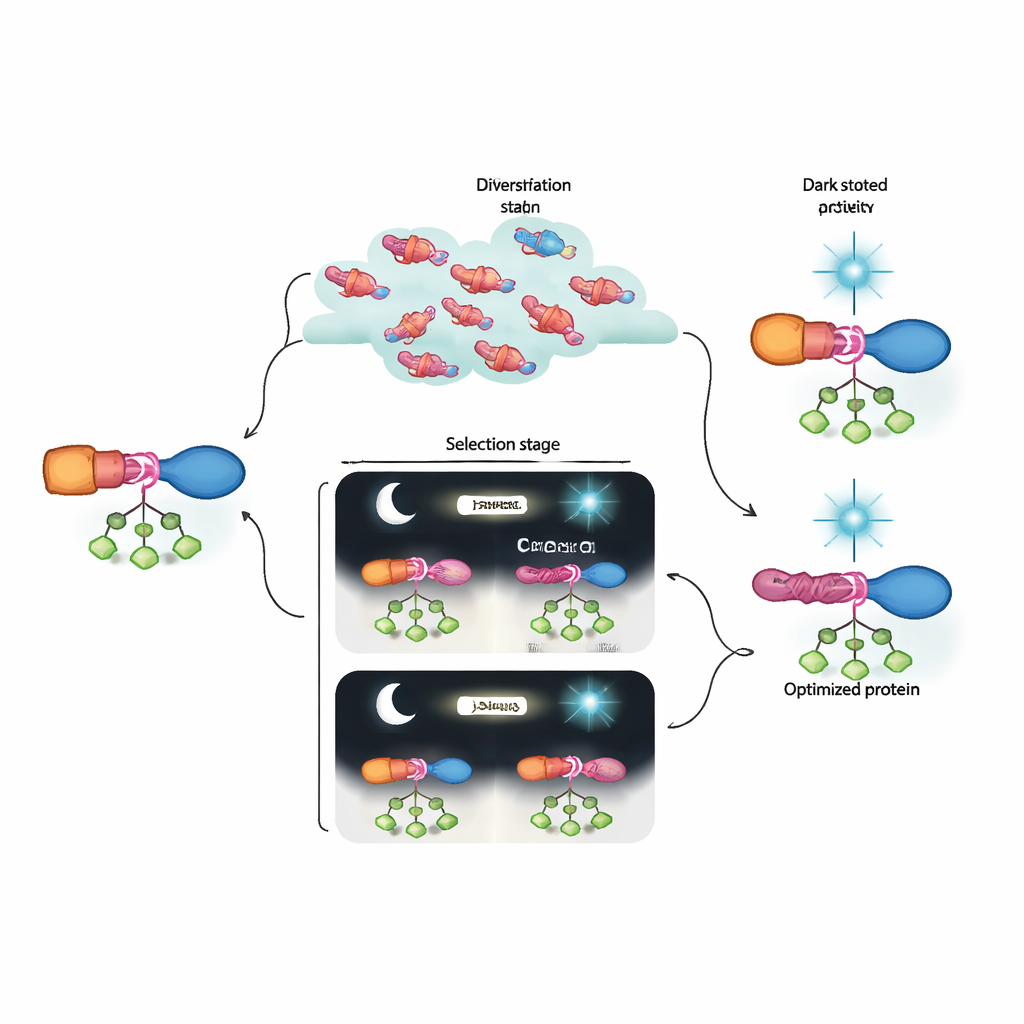
Geleceğin Biyo-mühendisliği İçin Anlamı
Basitçe söylemek gerekirse, yazarlar mevcut tasarım araçlarının kolayca üretemeyeceği protein anahtarlarını keşfedip rafine edebilen laboratuvar temelli bir “evrim makinesi” inşa ettiler. Evrimleştirdikleri AraC–LOV hibritleri gerektiğinde güçlü etkinlik gösteriyor ve mavi ışık altında neredeyse tamamen kapanarak önceki optogenetik sürümleri geride bırakıyor. Aynı derecede önemli olarak, dinamik seçilim ile derin dizilemenin birleşimi, ince mutasyon gruplarının nasıl işbirliği yaparak bir allosterik yol oluşturduğunu ortaya koyuyor. Bu çerçeve, birçok başka sinyal girişi ve protein hedefine uyarlanabilir; böylece hücresel süreçleri elektronik devreler kadar hassas programlayabildiğimiz, ama bunu evrimin kendisinin tasarımına yardımcı olduğu bileşenlerle yaptığımız bir geleceğe bizi daha da yaklaştırabilir.
Atıf: Southern, N.T., von Bachmann, A., Hovsepyan, A. et al. Phage-assisted evolution of allosteric protein switches. Nat Commun 17, 3498 (2026). https://doi.org/10.1038/s41467-026-71717-0
Anahtar kelimeler: optogenetik, yönlendirilmiş evrim, allosterik düzenleme, protein mühendisliği, bakteriyofaj