Clear Sky Science · he
אבולוציה בעזרת פאגים של מתגים חלבוניים אלוסטריים
הפיכת חלבונים למתגי הדלקה-כיבוי
דמיינו שאתם מסוגלים להדליק או לכבות מפתח מולקולרי בתוך תא חי — להפעיל גנים, אנזימים או מסלולי איתות כרצונכם. המאמר מתאר כיצד מדענים בנו "מגרש אימונים" אבולוציוני שמלמד חלבונים להתנהג כמתגים כאלה. על ידי שימוש בוירוסים שמדביקים חיידקים ובאסטרטגיית סלקציה מתוחכמת, הצוות מפתח חלבונים שמגיבים בחדות לאור, ומספק כלים רבי עוצמה למחקר, לביוטכנולוגיה ואולי בעתיד גם לרפואה.
מדוע שליטה מרחוק על חלבונים חשובה
חלבונים הם המכונות הזעירות שמפעילות את התאים שלנו. רבים מהם הם אלוסטריים מטבעם — שינוי באתר אחד בחלבון, שמעורר אות כמו סוכר, מולקול או אור, מביא לשינוי פונקציונלי באתר מרוחק אחר. המדענים שואפים לעצב מחדש את החיווט הזה כך שכמעט כל חלבון יוכל להיות נשלט על ידי קלט נבחר, למשל אור כחול. עם זאת הדבר קשה: כאשר חוקרים פשוט מחברים תחום חיישן על חלבון עובד, ההיבריד לעתים קרובות נחלש, דולף או כמעט שאינו רגיש. האתגר נובע מהעובדה ש"חוקי" האלוסטריה מפוזרים על פני שיירים וצורות מרובות שמתקשרות ביניהן, ולכן קשה לחזותם בעיצוב טהור.
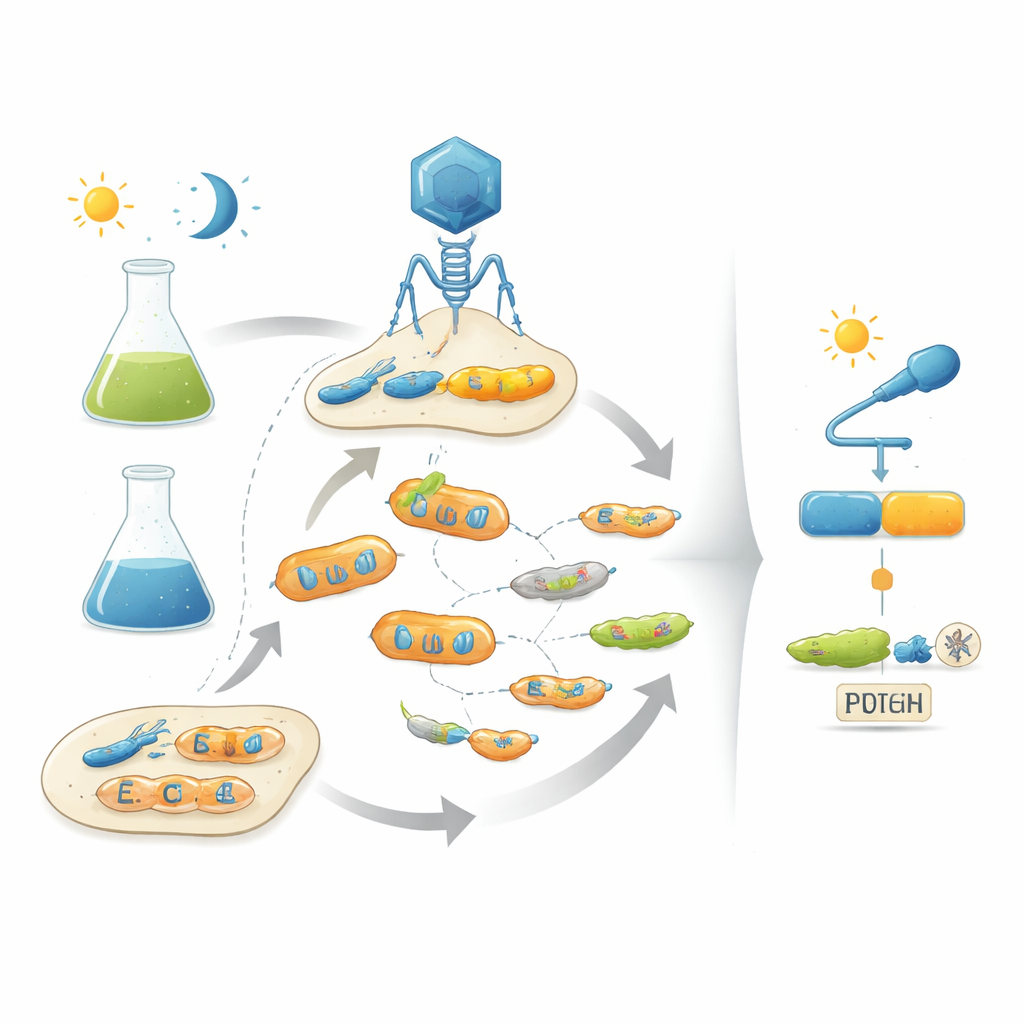
שימוש במתודולוגיית האבולוציה
המחברים פונים לבעיה זו על ידי חיקוי אבולוציה טבעית במעבדה באמצעות בקטריופאגים — וירוסים שמדביקים חיידקים. הפלטפורמה שלהם, שנקראת POGO-PANCE, מקשרת את הצלחת כל פאג לאופן שבו החלבון המקודד בו מתנהג כמתג. בשלב אחד, אם החלבון פעיל בתנאי הרצוי (למשל בחושך), הפאג משגשג. בשלב ההפוך, אם החלבון פעיל כשהוא אמור להיות כבוי (למשל באור), מיוצר עותק מזיק של רכיב ויראלי והקו הוויראלי המפריע קורסת. על ידי חילוף ביניהם של צעדי סלקציה חיוביים ושליליים אלו תוך כדי מוטציות מתמשכות בחלבון, המערכת דוחפת את האוכלוסיות הוויראליות לכיוון וריאנטים שגם חזקים וגם מבוקרים היטב על ידי אות הקלט.
אימון חלבון להגיב לאור
כדי להדגים את האסטרטגיה הם מתמקדים ב-AraC, חלבון חיידקי מוכר שמגיב בדרך כלל לסוכר ערבינוז כדי לשלוט בביטוי גנים. תחילה הם מפתחים את AraC עצמו כך שיהיה פעיל מאוד גם ללא הגירוי הסוכרי הטבעי שלו, וכך מקבלים נקודת התחלה "בעלת הספק גבוה". לאחר מכן הם משבצים מודול רגיש לאור כחול, הידוע כתחום LOV, בתוך AraC באתר שחזו שיאפשר תקשורת אלוסטרית. בתחילה ההיתוך כמעט שומט את AraC: הוא עובד בקושי ורק מראה תגובתיות קלה לאור כאשר מייצרים אותו בכמויות גבוהות. עם זאת, העברתם של ההיברידים המושבתים הללו דרך POGO-PANCE משנה אותם במהירות. לאחר מספר סבבי סלקציה חילופית באור ובחושך, הצוות משיב וריאנטים המתנהגים כמעט כמתגים דיגיטליים, עם שינוי של כאלף-פעמיים בפעילות הגן בין מצב חושך למצב מואר.
בחינת החיווט של מתג מולקולרי
מכיוון שהחלבונים המתפתחים מקודדים בגנום הפאג, החוקרים יכולים ברצף לרצף את האוכלוסיות הוויראליות אחרי כל מחזור. זה חושף אילו מוטציות עולות ויורדות בשלבי סלקציה שונים, ועוקב אחר הנתיבים שבאמצעותם מופיעים מתגים יעילים. הם מגלים ששינויים מופיעים לא רק ב-AraC ובחיישן האור אלא גם בקישוריות הקצרות שמחברות ביניהם. בעזרת כלי שני, RAMPhaGE, המבוסס על עריכת גנום מודרכת רטרון, הם מעצבים בצורה שיטתית את הקישורים האלה על ידי הוספה, הסרה או החלפה של מקטעים קצרים של חומצות אמיניות. האבולוציה במקביל מעדיפה וריאנטים שבהם הקישור בצד אחד של תחום ה-LOV מתארך לצורת הליקס חלקה שמגשרת פיזית בין החיישן למפעיל. ממצא זה מציע שלהליקס רציף ומיושר היטב יש סיוע בהעברת שינוי הצורה שמיוצר על ידי האור דרך החלבון, מה שמחדד את תגובת ההדלקה-כיבוי.
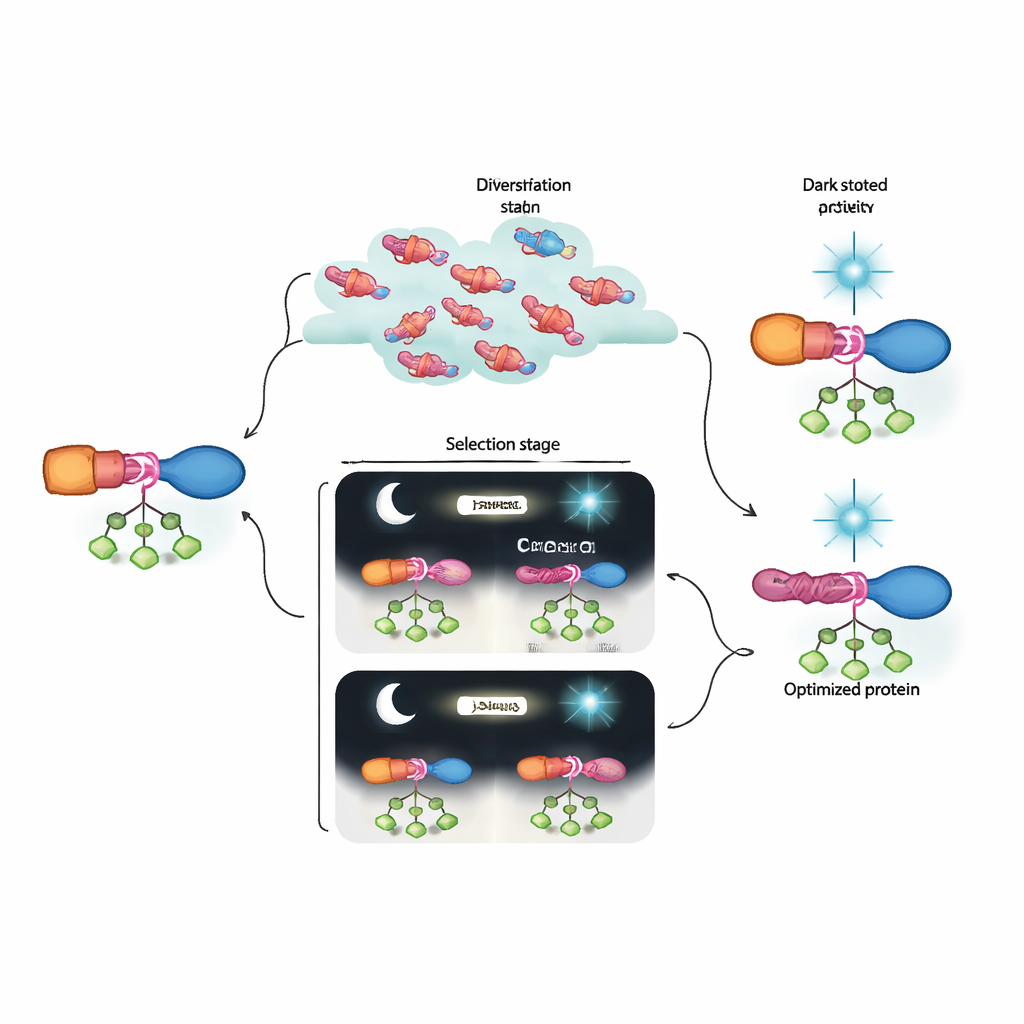
מובן הדבר לעתיד ההנדסה ביולוגית
באופן פשוט, המחברים בנו "מכונת אבולוציה" מבוססת מעבדה שיכולה לגלות ולשפר מתגי חלבון הרבה מעבר למה שכלי העיצוב הנוכחיים יכולים לייצר בקלות. ההיברידים האבולוציוניים של AraC–LOV שלהם מפגינים פעילות חזקה בעת הצורך וכמעט כיבוי מוחלט תחת אור כחול, ומתעלים על גרסאות אופטוגנטיות מוקדמות יותר. לא פחות חשוב, השילוב של סלקציה דינמית וריצוף עמוק מגלה כיצד קבוצות של מוטציות עדינות משתתפות בשיתוף פעולה לבניית מסלול אלוסטרי. מסגרת זו ניתנת להתאמה לקלטים וסוגי חלבונים רבים אחרים ותקרב אותנו לעתיד שבו ניתן לתכנת תהליכים תאיים בדיוק של מעגלים אלקטרוניים — אך באמצעות רכיבים שעוצבו בעצמם בעזרת האבולוציה.
ציטוט: Southern, N.T., von Bachmann, A., Hovsepyan, A. et al. Phage-assisted evolution of allosteric protein switches. Nat Commun 17, 3498 (2026). https://doi.org/10.1038/s41467-026-71717-0
מילות מפתח: אופטוגנטיקה, אבולוציה מכוונת, ויסות אלוסטרי, הנדסת חלבונים, בקטריופאג