Clear Sky Science · fr
Évolution assistée par phage de commutateurs protéiques allostériques
Transformer des protéines en interrupteurs marche–arrêt
Imaginez pouvoir actionner un interrupteur moléculaire à l’intérieur d’une cellule vivante — activer et désactiver des gènes, des enzymes ou des voies de signalisation à la demande. Cet article décrit comment des scientifiques ont construit un « terrain d’entraînement » évolutif qui apprend aux protéines à se comporter comme de tels interrupteurs. En exploitant des virus infectant les bactéries et une stratégie de sélection astucieuse, l’équipe fait évoluer des protéines qui répondent nettement à la lumière, offrant de nouveaux outils puissants pour la recherche, la biotechnologie et potentiellement la médecine.
Pourquoi la télécommande des protéines est importante
Les protéines sont les petites machines qui font fonctionner nos cellules. Beaucoup d’entre elles sont naturellement allostériques : une modification à un endroit de la protéine — déclenchée par un signal comme un sucre, un produit chimique ou la lumière — entraîne un changement fonctionnel à un endroit distant. Les scientifiques souhaitent reconfigurer ce câblage intégré pour que presque n’importe quelle protéine puisse être contrôlée par un signal choisi, comme la lumière bleue. Mais cela s’est avéré difficile : lorsque les chercheurs greffent simplement un domaine capteur sur une protéine fonctionnelle, le chimère devient souvent faible, fuyant ou à peine réactif. Le problème vient du fait que les « règles » de l’allostérie sont réparties sur de nombreux résidus et conformations interdépendants, ce qui les rend difficiles à prédire uniquement par conception.
Emprunter le mode d’emploi de l’évolution
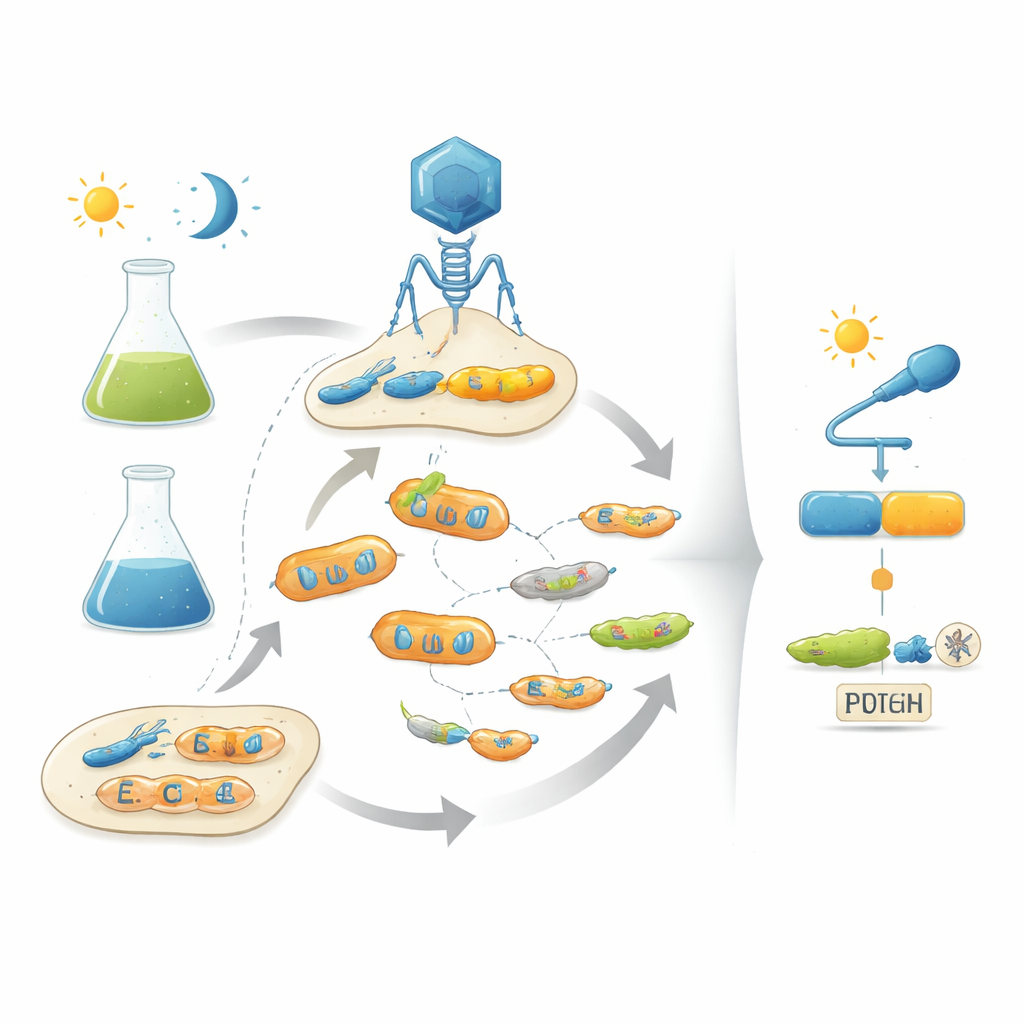
Les auteurs abordent ce problème en imitant l’évolution naturelle en laboratoire à l’aide de bactériophages — des virus qui infectent les bactéries. Leur plateforme, appelée POGO-PANCE, lie le succès de chaque phage à l’efficacité avec laquelle la protéine qu’il code fonctionne comme interrupteur. Dans une phase, si la protéine est active dans la condition souhaitée (par exemple, dans l’obscurité), le phage prospère. Dans la phase opposée, si la protéine est active alors qu’elle devrait être éteinte (par exemple, sous lumière), une version sabotée d’un composant viral est produite et la lignée phagique fautive s’effondre. En alternant ces étapes de sélection positive et négative tout en mutant constamment la protéine, le système pousse les populations virales vers des variantes à la fois puissantes et strictement contrôlées par le signal d’entrée.
Apprendre à une protéine à répondre à la lumière
Pour démontrer leur stratégie, les chercheurs se concentrent sur AraC, une protéine bactérienne bien étudiée qui répond normalement au sucre arabinose pour contrôler l’expression génique. D’abord, ils font évoluer AraC lui-même pour qu’il devienne fortement actif même sans son déclencheur sucré naturel, fournissant un point de départ « haute puissance ». Ensuite, ils insèrent un module sensible à la lumière bleue, connu sous le nom de domaine LOV, dans AraC à un site prédit pour permettre une communication allostérique. Initialement, cette fusion fragilise presque AraC : elle fonctionne à peine et montre seulement une faible réactivité à la lumière lorsqu’elle est surproduite. Faire passer ces hybrides handicapés dans POGO-PANCE les transforme toutefois rapidement. Après plusieurs cycles d’alternance de sélection sous lumière et obscurité, l’équipe obtient des variantes qui se comportent presque comme des interrupteurs numériques, avec une activité génique changeant d’environ mille fois entre l’état sombre et l’état illuminé.
Examiner le câblage d’un interrupteur moléculaire
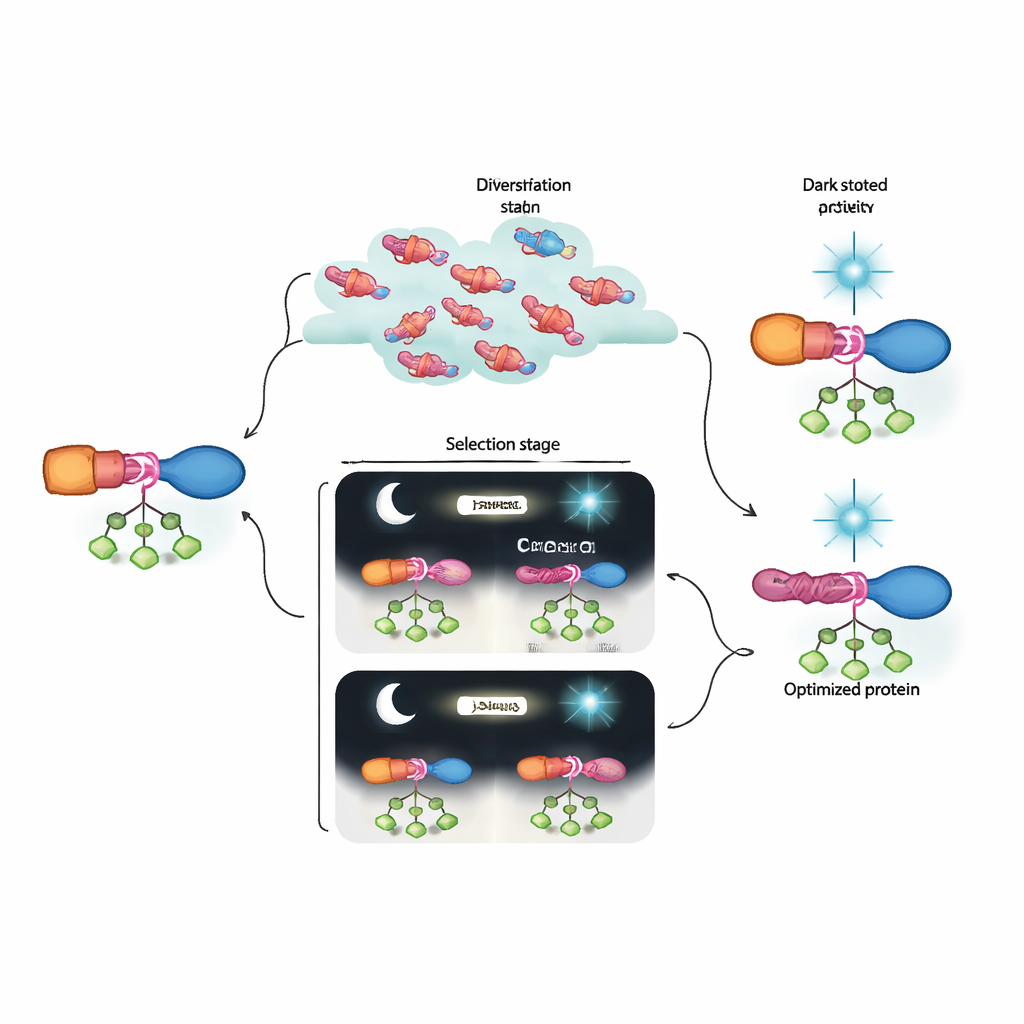
Parce que les protéines en évolution sont codées sur le génome du phage, les chercheurs peuvent séquencer les populations virales après chaque cycle. Cela révèle quelles mutations montent et descendent sous les différentes étapes de sélection, retraçant les voies par lesquelles émergent des interrupteurs efficaces. Ils constatent que des changements apparaissent non seulement dans AraC et le capteur lumineux mais aussi dans les courts linkers qui les relient. En utilisant un second outil, RAMPhaGE, basé sur l’édition génomique guidée par retrons, ils remodelent systématiquement ces linkers en ajoutant, supprimant ou échangeant de petits segments d’acides aminés. L’évolution favorise à plusieurs reprises des variantes où le linker d’un côté du domaine LOV s’étend en une hélice lisse qui relie physiquement senseur et effecteur. Cela suggère qu’une hélice continue et bien alignée aide à transmettre le changement de conformation induit par la lumière à travers la protéine, affinant la réponse marche–arrêt.
Ce que cela signifie pour le génie biologique futur
En termes simples, les auteurs ont construit une « machine à évoluer » en laboratoire capable de découvrir et d’affiner des interrupteurs protéiques bien au-delà de ce que les outils de conception actuels peuvent facilement produire. Leurs hybrides AraC–LOV évolués montrent une forte activité quand nécessaire et se ferment presque complètement sous lumière bleue, surpassant les versions optogénétiques antérieures. Tout aussi important, la combinaison d’une sélection dynamique et d’un séquençage profond révèle comment des groupes de mutations subtiles coopèrent pour construire une voie allostérique. Ce cadre pourrait être adapté à de nombreux autres signaux et cibles protéiques, nous rapprochant d’un avenir où les processus cellulaires pourront être programmés avec la précision des circuits électroniques, mais en utilisant des composants que l’évolution elle-même a contribué à concevoir.
Citation: Southern, N.T., von Bachmann, A., Hovsepyan, A. et al. Phage-assisted evolution of allosteric protein switches. Nat Commun 17, 3498 (2026). https://doi.org/10.1038/s41467-026-71717-0
Mots-clés: optogénétique, évolution dirigée, régulation allostérique, génie des protéines, bactériophage