Clear Sky Science · de
Phagen-gestützte Evolution allosterischer Proteinschalter
Proteine in Ein–/Aus‑Schalter verwandeln
Stellen Sie sich vor, Sie könnten einen molekularen Lichtschalter in einer lebenden Zelle umlegen—Gene, Enzyme oder Signalwege nach Belieben an- und ausschalten. Dieser Artikel beschreibt, wie Forscher einen evolutiven „Trainingsplatz“ aufgebaut haben, der Proteine dazu befähigt, genau so zu funktionieren. Indem sie Bakterien infizierende Viren und eine raffinierte Selektionsstrategie nutzen, entwickeln die Autoren Proteine, die empfindlich auf Licht reagieren und damit leistungsfähige neue Werkzeuge für Forschung, Biotechnologie und potenziell Medizin liefern.
Warum Fernsteuerung von Proteinen wichtig ist
Proteine sind die winzigen Maschinen in unseren Zellen. Viele von ihnen sind natürlicherweise allosterisch: Eine Änderung an einer Stelle des Proteins—ausgelöst durch ein Signal wie ein Zucker, eine Chemikalie oder Licht—bewirkt eine Funktionsänderung an einer anderen, entfernten Stelle. Wissenschaftler möchten diese eingebaute Verdrahtung so umgestalten, dass sich fast jedes Protein durch einen gewählten Input steuern lässt, etwa blaues Licht. Das ist jedoch schwierig: Wenn Forscher einfach eine Sensordomäne an ein funktionierendes Protein anheften, wird das Chimärprotein oft schwach, undicht oder kaum reagierend. Die Herausforderung liegt darin, dass die „Regeln“ der Allosterie über viele wechselwirkende Reste und Faltflächen verteilt sind und sich nur schwer allein durch Design vorhersagen lassen.
Vom Spielbuch der Evolution abschreiben
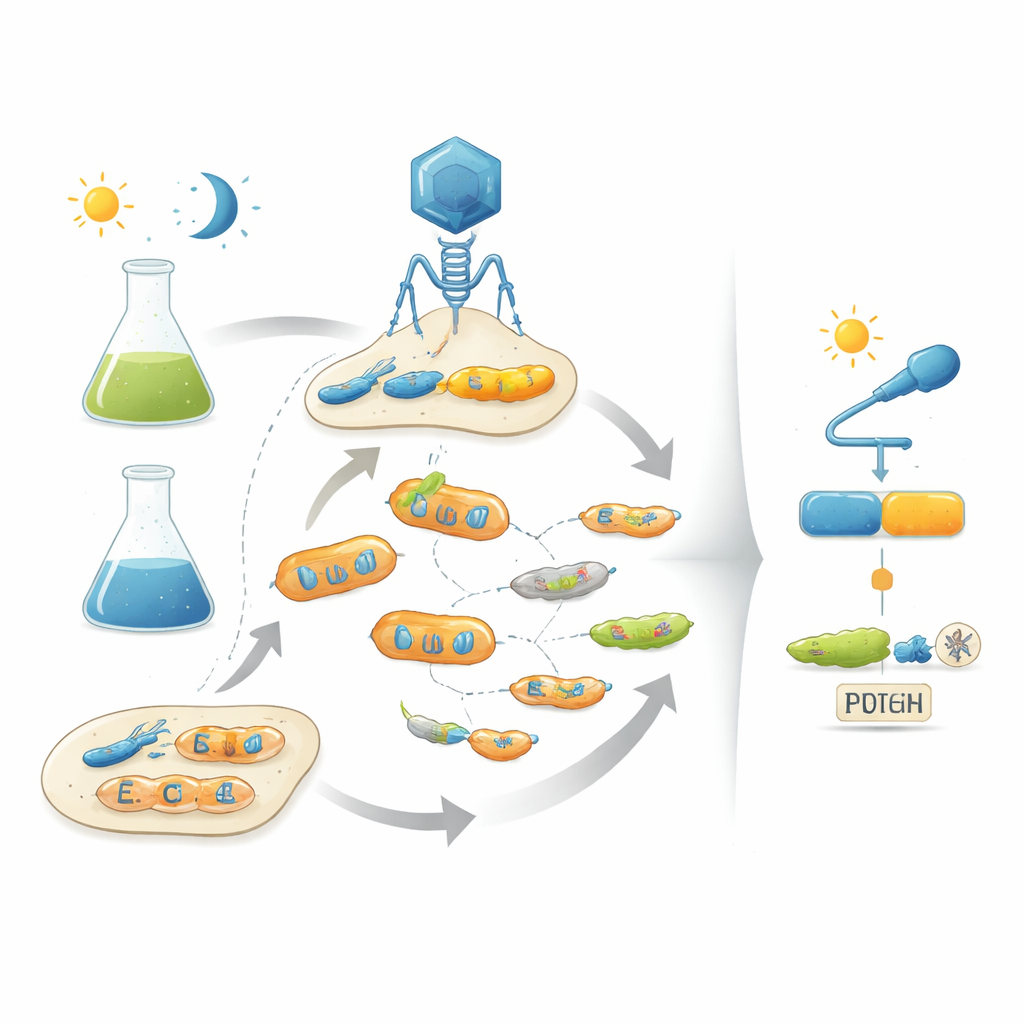
Die Autoren begegnen diesem Problem, indem sie die natürliche Evolution im Labor nachahmen und Bakteriophagen—Viren, die Bakterien infizieren—verwenden. Ihre Plattform, POGO-PANCE genannt, koppelt den Erfolg jedes Phagen an die Fähigkeit des von ihm codierten Proteins, als Schalter zu funktionieren. In einer Phase gedeiht der Phage, wenn das Protein unter der gewünschten Bedingung aktiv ist (zum Beispiel im Dunkeln). In der Gegenphase führt Aktivität des Proteins, wenn es abgeschaltet sein sollte (zum Beispiel bei Licht), zur Produktion einer sabotierenden Version einer viralen Komponente, und die betreffende Phagenlinie bricht zusammen. Durch das abwechselnde Anwenden dieser positiven und negativen Selektionsschritte bei gleichzeitiger kontinuierlicher Mutation des Proteins lenkt das System die Phagenpopulationen in Richtung Varianten, die sowohl leistungsfähig als auch eng vom Eingangssignal gesteuert sind.
Ein Protein darauf trainieren, auf Licht zu reagieren
Um ihre Strategie zu demonstrieren, konzentrieren sich die Forscher auf AraC, ein gut untersuchtes bakterielles Protein, das normalerweise auf den Zucker Arabinose reagiert, um die Genexpression zu steuern. Zunächst entwickeln sie AraC selbst so weiter, dass es stark aktiv ist, selbst ohne seinen natürlichen Zuckertrigger, und erhalten so einen „leistungsstarken“ Ausgangspunkt. Danach fügen sie eine blaulichtempfindliche Einheit, eine sogenannte LOV‑Domäne, an einer Stelle in AraC ein, die voraussichtlich allosterische Kommunikation erlaubt. Zunächst zerstört diese Fusion AraC nahezu: Sie funktioniert kaum und zeigt nur bei starker Überproduktion eine schwache Lichtantwort. Werden diese geschwächten Hybride jedoch durch POGO-PANCE geschickt, verwandeln sie sich schnell. Nach mehreren Runden abwechselnder Selektion bei Licht und Dunkelkeit gewinnen die Forscher Varianten, die sich fast wie digitale Schalter verhalten, wobei die Genaktivität zwischen dunklem und beleuchtetem Zustand um etwa das Tausendfache variiert.
Ein Blick in die Verdrahtung eines molekularen Schalters
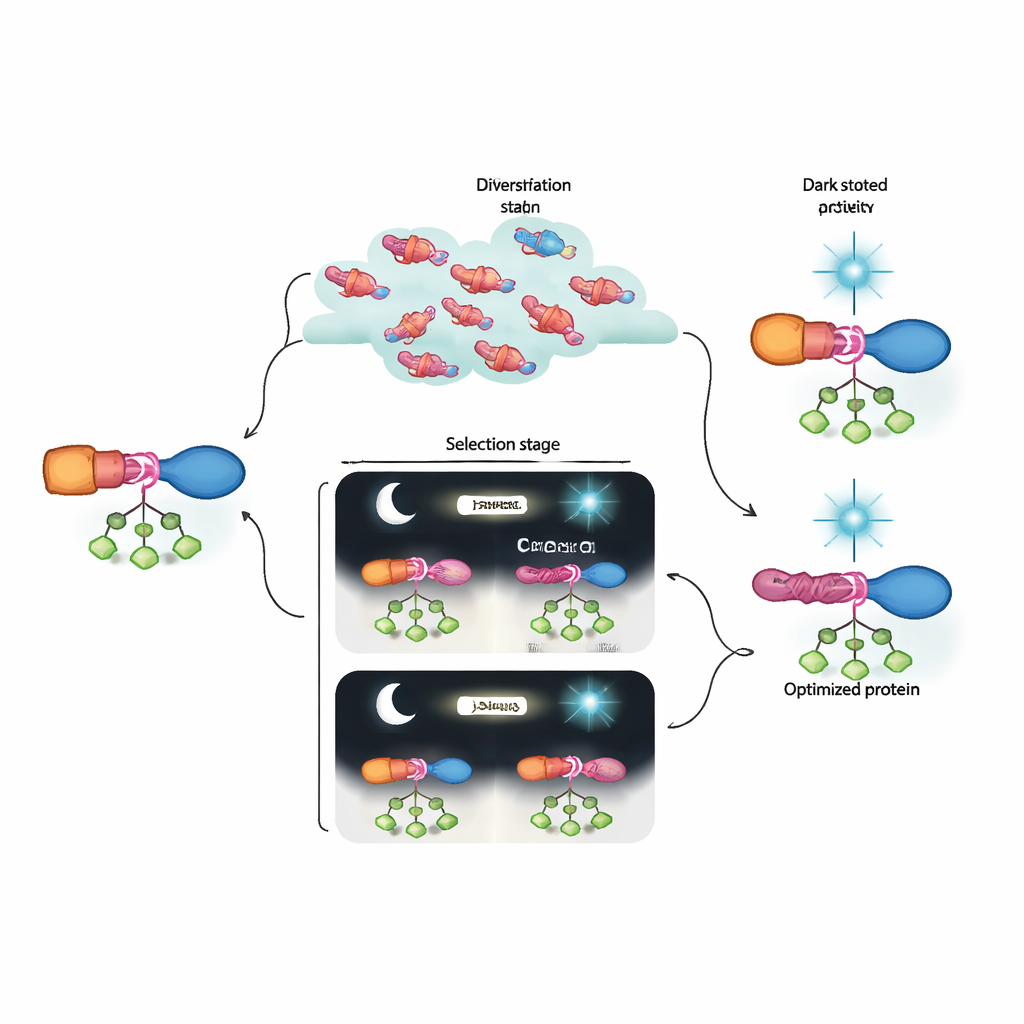
Da die sich entwickelnden Proteine im Phagengenom codiert sind, können die Forscher die viralen Populationen nach jedem Zyklus sequenzieren. Das zeigt, welche Mutationen unter den verschiedenen Selektionsschritten zunehmen oder abnehmen und zeichnet die Wege nach, über die effektive Schalter entstehen. Sie finden Veränderungen nicht nur in AraC und dem Lichtsensor, sondern auch in den kurzen Linkern, die diese verbinden. Mit einem zweiten Werkzeug, RAMPhaGE, das auf retron‑gesteuerter Genomeditierung basiert, gestalten sie diese Linker systematisch um, indem sie kleine Aminosäureabschnitte hinzufügen, entfernen oder austauschen. Die Evolution bevorzugt immer wieder Varianten, bei denen der Linker an einer Seite der LOV‑Domäne zu einer durchgehenden Helix verlängert, die Sensor und Effektor physikalisch verbindet. Das legt nahe, dass eine kontinuierliche, gut ausgerichtete Helix die lichtinduzierten Formänderungen durch das Protein überträgt und so die Ein‑/Aus‑Reaktion schärft.
Was das für künftiges Bioengineering bedeutet
Einfach gesagt haben die Autoren eine laborbasierte „Evolutionsmaschine“ gebaut, die Proteinschalter entdecken und verfeinern kann—weit über das hinaus, was aktuelle Designwerkzeuge leicht liefern. Ihre weiterentwickelten AraC–LOV‑Hybride zeigen starke Aktivität, wenn sie gebraucht wird, und schalten unter blauem Licht nahezu vollständig ab und übertreffen frühere optogenetische Versionen. Ebenso wichtig ist, dass die Kombination aus dynamischer Selektion und tiefgehender Sequenzierung zeigt, wie Gruppen subtiler Mutationen zusammenwirken, um einen allosterischen Pfad aufzubauen. Dieses Rahmenkonzept ließe sich auf viele andere Signaleingänge und Proteinziele anpassen und bringt uns der Zukunft näher, in der zelluläre Prozesse mit der Präzision elektronischer Schaltungen programmiert werden—aber mit Komponenten, die die Evolution selbst mitgestaltet hat.
Zitation: Southern, N.T., von Bachmann, A., Hovsepyan, A. et al. Phage-assisted evolution of allosteric protein switches. Nat Commun 17, 3498 (2026). https://doi.org/10.1038/s41467-026-71717-0
Schlüsselwörter: Optogenetik, gerichtete Evolution, allosterische Regulation, Protein-Engineering, Bakteriophagen