Clear Sky Science · nl
Fagen-gedreven evolutie van allosterische eiwitschakelaars
Proteïnen veranderen in aan‑/uit‑schakelaars
Stel je voor dat je een moleculaire lichtschakelaar in een levend cel kunt omzetten—genen, enzymen of signaalroutes aan of uit zetten wanneer je maar wilt. Dit artikel beschrijft hoe wetenschappers een evolutionair ‘trainingsveld’ bouwden dat eiwitten leert zich als zulke schakelaars te gedragen. Door gebruik te maken van virussen die bacteriën infecteren en een slimme selectiestrategie, evolueert het team eiwitten die scherp op licht reageren, wat krachtige nieuwe instrumenten oplevert voor onderzoek, biotechnologie en mogelijk de geneeskunde.
Waarom afstandsbediening van eiwitten ertoe doet
Eiwitten zijn de kleine machines die onze cellen aansturen. Veel eiwitten zijn van nature allosterisch: een verandering op de ene plek in het eiwit—geïnitieerd door een signaal zoals een suiker, een chemische stof of licht—overtuigt een functionele verandering op een andere, verder gelegen plek. Wetenschappers willen deze ingebouwde bedrading herontwerpen zodat bijna elk eiwit kan worden bestuurd door een gekozen input, bijvoorbeeld blauw licht. Dat is echter lastig gebleken: wanneer onderzoekers simpelweg een sensordomein aan een werkend eiwit vastmaken, wordt het chimera vaak zwak, lekgevoelig of nauwelijks responsief. De uitdaging is dat de ‘regels’ van allosterie verspreid liggen over veel interacterende residuen en vormen, waardoor ze moeilijk te voorspellen zijn met alleen ontwerpprincipën.
Het speelboek van evolutie lenen
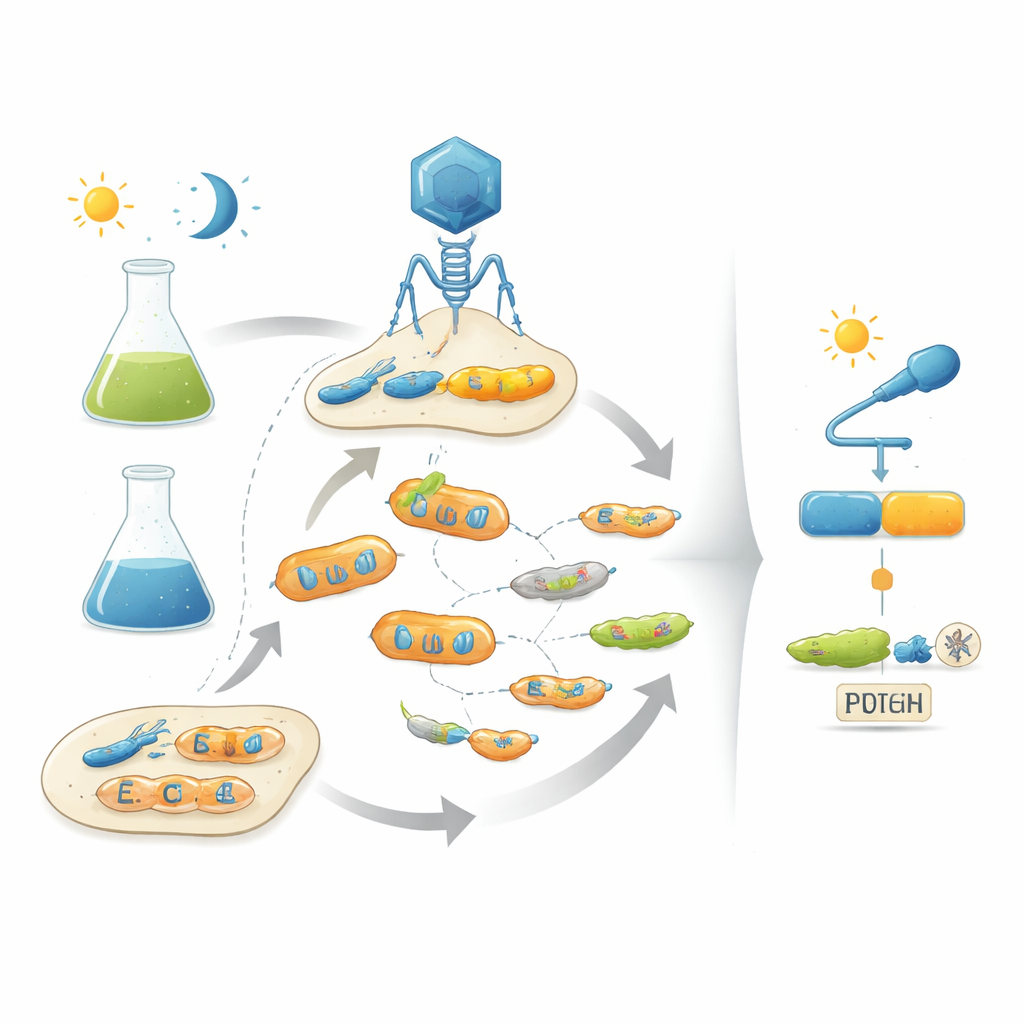
De auteurs pakken dit probleem aan door natuurlijke evolutie in het lab na te bootsen met bacteriofagen—virussen die bacteriën infecteren. Hun platform, POGO‑PANCE genoemd, koppelt het succes van elke faag aan hoe goed het gecodeerde eiwit zich als schakel gedraagt. In de ene fase floreert de faag als het eiwit actief is onder de gewenste conditie (bijvoorbeeld in het donker). In de tegenovergestelde fase, als het eiwit actief is wanneer het uit zou moeten zijn (bijvoorbeeld onder licht), wordt een sabotagevariant van een viraal component geproduceerd en stort de betreffende faaglijn in. Door deze positieve en negatieve selectiestappen af te wisselen terwijl het eiwit constant muteert, drijft het systeem de virale populaties in de richting van varianten die zowel krachtig als strak door het ingangssignaal worden gecontroleerd.
Een eiwit trainen om op licht te reageren
Om hun strategie te demonstreren richten de onderzoekers zich op AraC, een goed bestudeerd bacterieel eiwit dat normaal op de suiker arabinose reageert om genexpressie te regelen. Eerst evolueren ze AraC zelf zodat het sterk actief wordt zelfs zonder zijn natuurlijke suikertrechter, wat een ‘krachtige’ startpunt oplevert. Vervolgens voegen ze een blauwlicht‑gevoelige module, bekend als een LOV‑domein, in AraC op een plaats die voorspeld is allosterische communicatie mogelijk te maken. Aanvankelijk breekt deze fusie AraC bijna: het werkt nauwelijks en toont alleen zwakke lichtrespons wanneer het overgeproduceerd wordt. Het door POGO‑PANCE draaien van deze gehavende hybriden transformeert ze echter snel. Na enkele rondes van afwisselende selectie onder licht en donker herstellen de onderzoekers varianten die bijna als digitale schakelaars werken, met genactiviteit die ongeveer duizendvoudig verandert tussen donkere en verlichte toestanden.
In de bedrading van een moleculaire schakel kijken
Aangezien de evoluerende eiwitten op het faaggenoom gecodeerd zijn, kunnen de onderzoekers de virale populaties na elke cyclus sequentiëren. Dit onthult welke mutaties onder verschillende selectiestappen stijgen en dalen, en tekent de paden uit waarlangs effectieve schakelaars ontstaan. Ze vinden dat veranderingen niet alleen in AraC en de lichtsensor optreden, maar ook in de korte linkers die ze verbinden. Met een tweede hulpmiddel, RAMPhaGE, gebaseerd op retron‑geleid genoomediting, vormen ze deze linkers systematisch door het toevoegen, verwijderen of uitwisselen van kleine reeksen aminozuren. Evolutie geeft herhaaldelijk de voorkeur aan varianten waarbij de linker aan één zijde van het LOV‑domein uitgroeit tot een soepele helix die sensor en effector fysiek overbrugt. Dit suggereert dat een continue, goed uitgelijnde helix helpt de door licht geïnduceerde conformationele verandering door het eiwit te geleiden, waardoor de aan‑/uit‑respons verscherpt wordt.
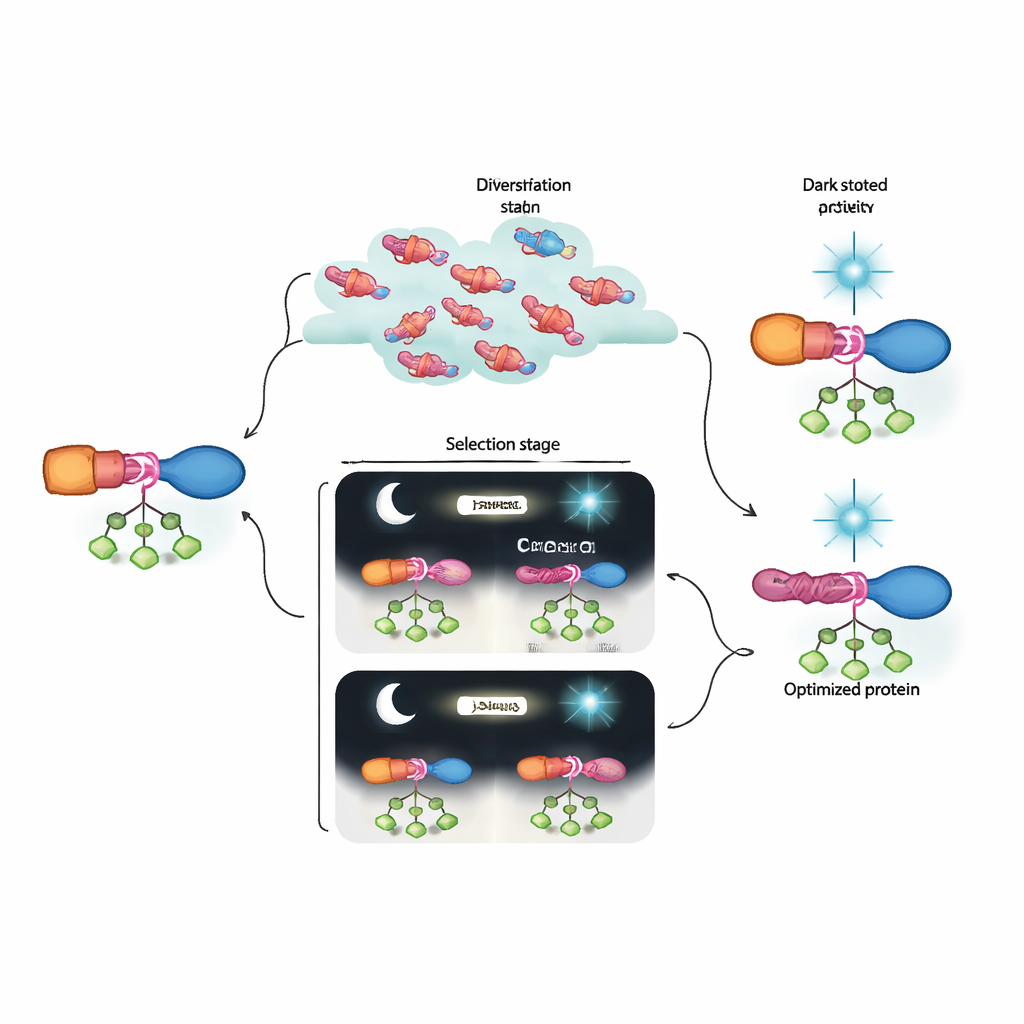
Wat dit betekent voor toekomstige bioengineering
Simpel gezegd hebben de auteurs een in het lab gebaseerde ‘evolutiemachine’ gebouwd die eiwitschakelaars kan ontdekken en verfijnen tot ver voorbij wat huidige ontwerptools gemakkelijk kunnen produceren. Hun geëvolueerde AraC–LOV‑hybriden tonen sterke activiteit wanneer dat nodig is en schakelen bijna volledig uit onder blauw licht, en presteren beter dan eerdere optogenetische versies. Even belangrijk is dat de combinatie van dynamische selectie en diepe sequentiebepaling onthult hoe groepen subtiele mutaties samenwerken om een allosterisch pad op te bouwen. Dit raamwerk kan worden aangepast aan vele andere signaalinputs en eiwitdoelen, en brengt ons dichter bij een toekomst waarin cellulaire processen met de precisie van elektronische schakelingen kunnen worden geprogrammeerd, maar met componenten die de evolutie zelf mede heeft ontworpen.
Bronvermelding: Southern, N.T., von Bachmann, A., Hovsepyan, A. et al. Phage-assisted evolution of allosteric protein switches. Nat Commun 17, 3498 (2026). https://doi.org/10.1038/s41467-026-71717-0
Trefwoorden: optogenetica, gerichte evolutie, allosterische regulatie, eiwitengineering, bacteriofaag