Clear Sky Science · zh
SPNS2 输出鞘氨醇-1-磷酸并输入葡萄糖
糖与细胞信号的隐秘守门员
我们的身体在维持血糖在安全范围的同时,不断处理成千上万种化学信号。这项研究发现了一个意想不到的参与者,能同时兼顾这两项任务:一种位于细胞膜上的小蛋白 SPNS2。研究者表明,SPNS2 不仅释放一种对免疫和血管重要的信号脂质分子,同时还有助于把葡萄糖——机体的主要燃料——拉入细胞。这个双重功能将细胞间的通讯与细胞的能量供给联系起来,对糖尿病、心血管病和癌症等具有重要意义。
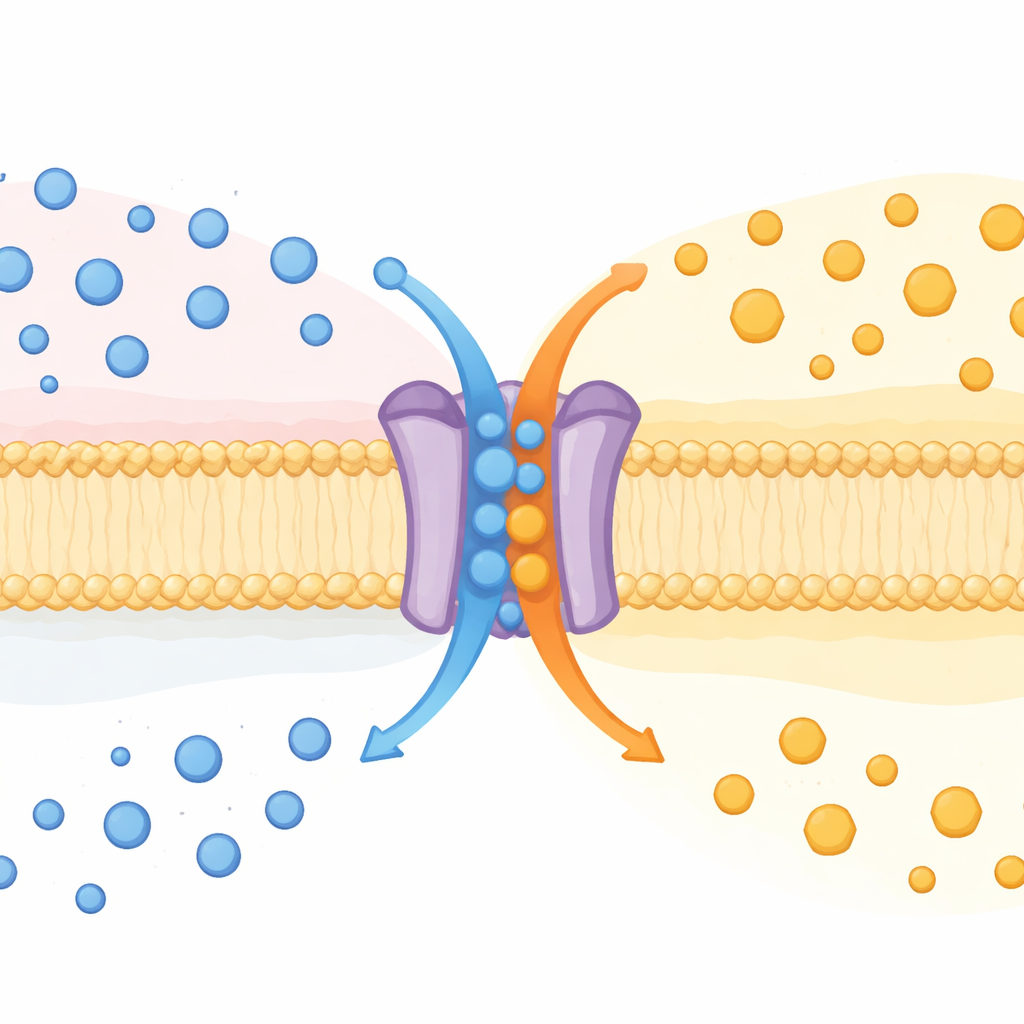
一蛋白,两重任务
长期以来人们认为 SPNS2 的作用是将信使分子鞘氨醇‑1‑磷酸(S1P)从细胞内运出。S1P 在血液和淋巴中循环,指导免疫细胞、塑造血管并影响炎症。此前 SPNS2 被视为单向的输出器。通过研究缺失 Spns2 基因的小鼠以及多种培养细胞,作者发现 SPNS2 实际上更像一种交换机器:它将 S1P 输出,同时将葡萄糖带入,类似于“反向转运蛋白”(antiporter)这类在膜两侧互换物质的转运体。
缺失 SPNS2 会发生什么
在基因改造缺失 SPNS2 的小鼠中,血液和淋巴中的 S1P 水平下降,而肝、肾、肺和心等组织中 S1P 积累——这正符合一个输出器被禁用时的预期。但它们的糖稳态也被扰乱。血糖升高,尿液和粪便中出现额外的葡萄糖,同时若干器官的内部葡萄糖水平降低。用放射性葡萄糖类示踪剂成像显示,这些小鼠从肠道吸收糖的能力正常,但其组织——尤其是肾脏——在从血液和滤过的尿液中回收葡萄糖方面表现不佳。综合这些发现,指向了一个把葡萄糖运进细胞并再利用的缺陷,尽管胰岛素水平和激素信号正常。
SPNS2 在推动信号的同时引入燃料
为检验 SPNS2 本身是否能移动葡萄糖,研究组在血管和其他细胞类型中操控其表达量。提高 SPNS2 水平时,细胞向周围液体释放出更多 S1P,并吸收更多葡萄糖,产生更多能量并表现出更强的呼吸和糖代谢活性。删除或阻断 SPNS2 时,细胞将 S1P 保留在细胞内且葡萄糖摄取减少。这些效应即便在经典糖转运蛋白(如 GLUT1 和 GLUT3)被抑制时仍然存在,且不依赖于细胞表面的 S1P 受体或胰岛素。在精心构建的人工“蛋白脂质囊泡”(将纯化的 SPNS2 嵌入膜中的微小实验泡)中,该蛋白能够直接将荧光或放射性标记的葡萄糖向内转运,但仅在内侧有 S1P 时效率较高。这表明 SPNS2 本身可以作为与 S1P 输出耦合的葡萄糖输入器。
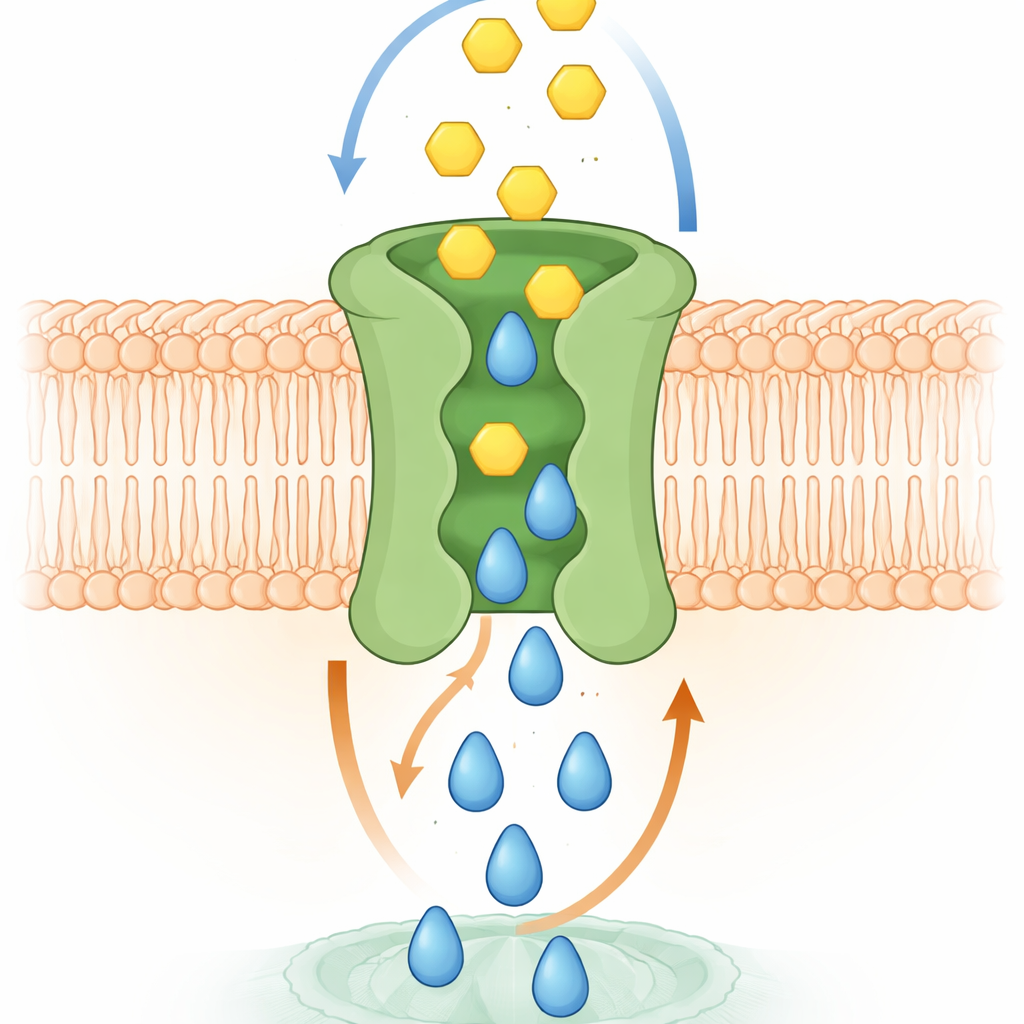
分子交换可能的工作机制
计算机模拟和结构实验帮助阐明了这一机制。膜中高分辨率的 SPNS2 模型显示 S1P 经由中央空腔向上滑动,触发细微的构象变化,打开外侧的临时口袋以容纳葡萄糖。随着 S1P 朝外侧移动,葡萄糖可在这些口袋中停靠,然后顺着相同的中央通道向细胞内滑入。研究者鉴定出与葡萄糖接触的特定位点氨基酸。当这些残基被突变时,葡萄糖结合下降且转运失败,即便变异蛋白仍能到达细胞表面。在活细胞中,失去这种耦合转运会削弱由 S1P 驱动的过程,例如细胞增殖、向闭合创伤样缺口移动以及内皮细胞层形成紧密屏障的能力——这些功能都需要信号与能量的共同作用。
这对健康与疾病的重要性
通过揭示 SPNS2 是一个双向门——在释放 S1P 的同时引入葡萄糖——这项工作将强有力的信号分子与基本能量供应在一步机制中连接起来。当 SPNS2 释放 S1P 以触发免疫或血管反应时,它同时帮助细胞摄取额外燃料以支持这些行动。这种耦合的破坏可能导致高血糖、肾脏糖丢失以及不依赖胰岛素的葡萄糖代谢紊乱形式。由于 SPNS2 和 S1P 信号还影响癌症转移、炎症和血管完整性,针对这一“信号-与-糖”守门员可能为治疗代谢病、自身免疫疾病以及依赖增强信号和增加葡萄糖摄取的肿瘤开辟新途径。
引用: Weigel, C., Hossen, M.L., Brown, R.D.R. et al. SPNS2 exports sphingosine-1-phosphate and imports glucose. Nat Commun 17, 3901 (2026). https://doi.org/10.1038/s41467-026-71659-7
关键词: 葡萄糖转运, 鞘氨醇-1-磷酸, 膜转运蛋白, 内皮生物学, 代谢信号