Clear Sky Science · sv
SPNS2 exporterar sphingosine-1-phosphate och importerar glukos
En dold grindvakt för socker och cellsignaler
Våra kroppar hanterar ständigt tusentals kemiska signaler samtidigt som de håller blodsockret inom ett säkert intervall. Denna studie avslöjar en oväntad aktör som hjälper till med båda uppgifterna: ett litet protein som heter SPNS2 och sitter i cellmembran. Forskarna visar att SPNS2 inte bara släpper ut ett signalsfett som är viktigt för immunförsvaret och blodkärl, utan samtidigt hjälper till att föra in glukos — kroppens huvudsakliga bränsle — i cellerna. Denna dubbla funktion kopplar hur celler kommunicerar med hur de försörjer sig själva, med konsekvenser för diabetes, hjärtsjukdomar och cancer.
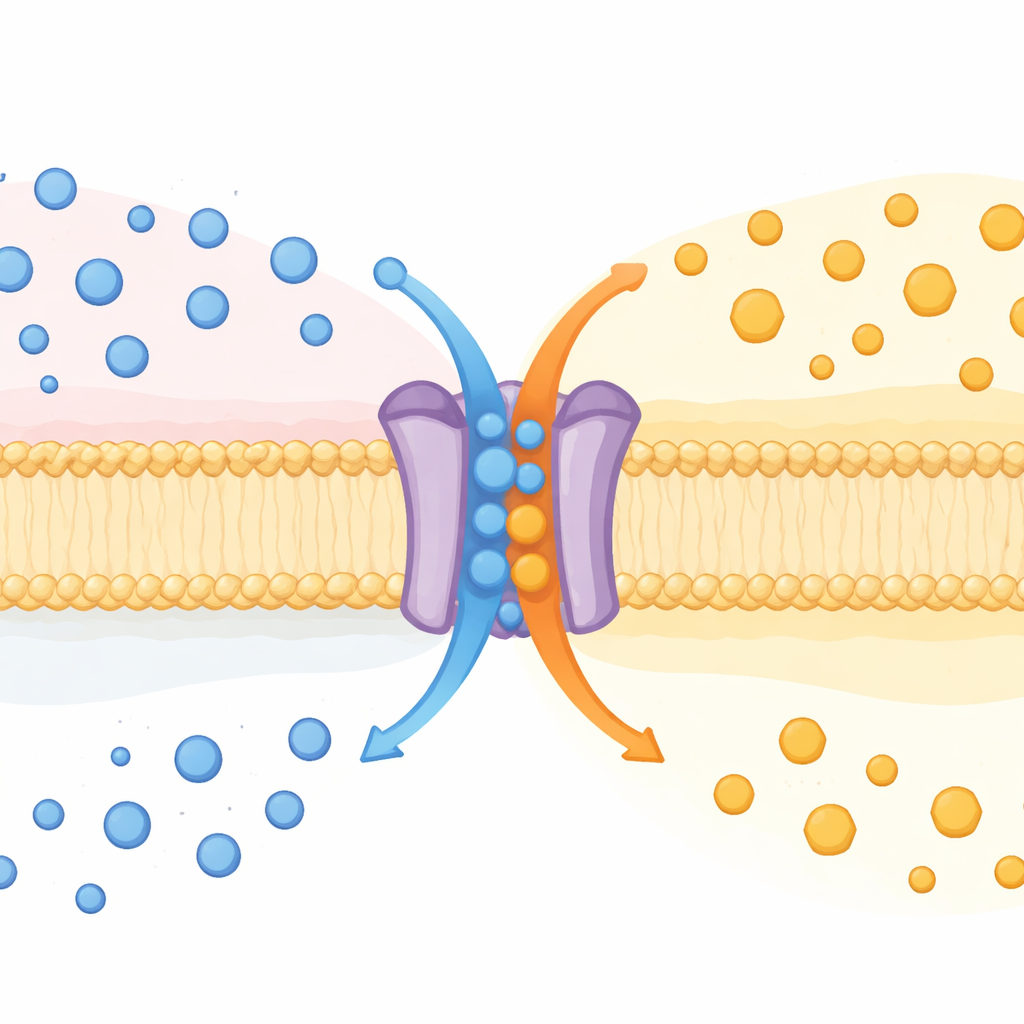
Ett protein, två uppgifter
SPNS2 har länge varit känt för att flytta en budbärarmolekyl kallad sphingosine‑1‑phosphate (S1P) ut ur celler. S1P cirkulerar i blod och lymfa, vägleder immunceller, formar blodkärl och påverkar inflammation. Fram till nu ansågs SPNS2 vara en envägsexportör. Genom att studera möss utan Spns2-genen, tillsammans med många typer av odlade celler, upptäckte författarna att SPNS2 faktiskt beter sig mer som en bytesmaskin. Den skickar ut S1P samtidigt som den tar in glukos, på ett sätt som liknar en ”antiport”, en klass av transportörer som byter en substans mot en annan över membran.
Vad händer när SPNS2 saknas
Hos möss konstruerade att sakna SPNS2 sjönk nivåerna av S1P i blod och lymfa, medan S1P ansamlade sig i vävnader som lever, njure, lunga och hjärta — precis vad man skulle förvänta sig om en exportör inaktiverats. Men deras sockerbalans stördes också. Blodglukos ökade, och extra glukos förekom i urin och avföring, samtidigt som flera organ visade lägre interna glukosnivåer. Avbildning med en radioaktiv glukoslik tracer visade att dessa möss absorberade socker från tarmen normalt, men deras vävnader — och särskilt njurarna — var dåliga på att återta glukos från blodet och från filtrerat urin. Tillsammans pekade dessa fynd på ett fel i att få glukos in i cellerna och återanvända det, trots normala insulinnivåer och hormonsignaler.
SPNS2 drar in bränsle samtidigt som den skjuter ut signaler
För att testa om SPNS2 själv flyttar glukos manipulerade teamet dess nivåer i blodkärls- och andra celltyper. När de ökade SPNS2 tog cellerna ut mer S1P i omgivningsvätskan och tog upp mer glukos, producerade mer energi och visade starkare respiration och sockerapptagning. När de tog bort eller blockerade SPNS2 höll cellerna kvar S1P inuti och tog upp mindre glukos. Dessa effekter kvarstod även när klassiska sockertransportörer (som GLUT1 och GLUT3) hämmades, och de berodde inte på S1P‑receptorer på cellytan eller på insulin. I noggrant kontrollerade artificiella ”proteoliposomer” — små laboratorietillverkade bubblor med renat SPNS2 inbyggt i membranen — kunde proteinet direkt flytta fluorescerande eller radioaktivt glukos inåt, men endast effektivt när S1P fanns på den inre sidan. Detta visade att SPNS2 själv kan fungera som en glukosimportör kopplad till S1P‑export.
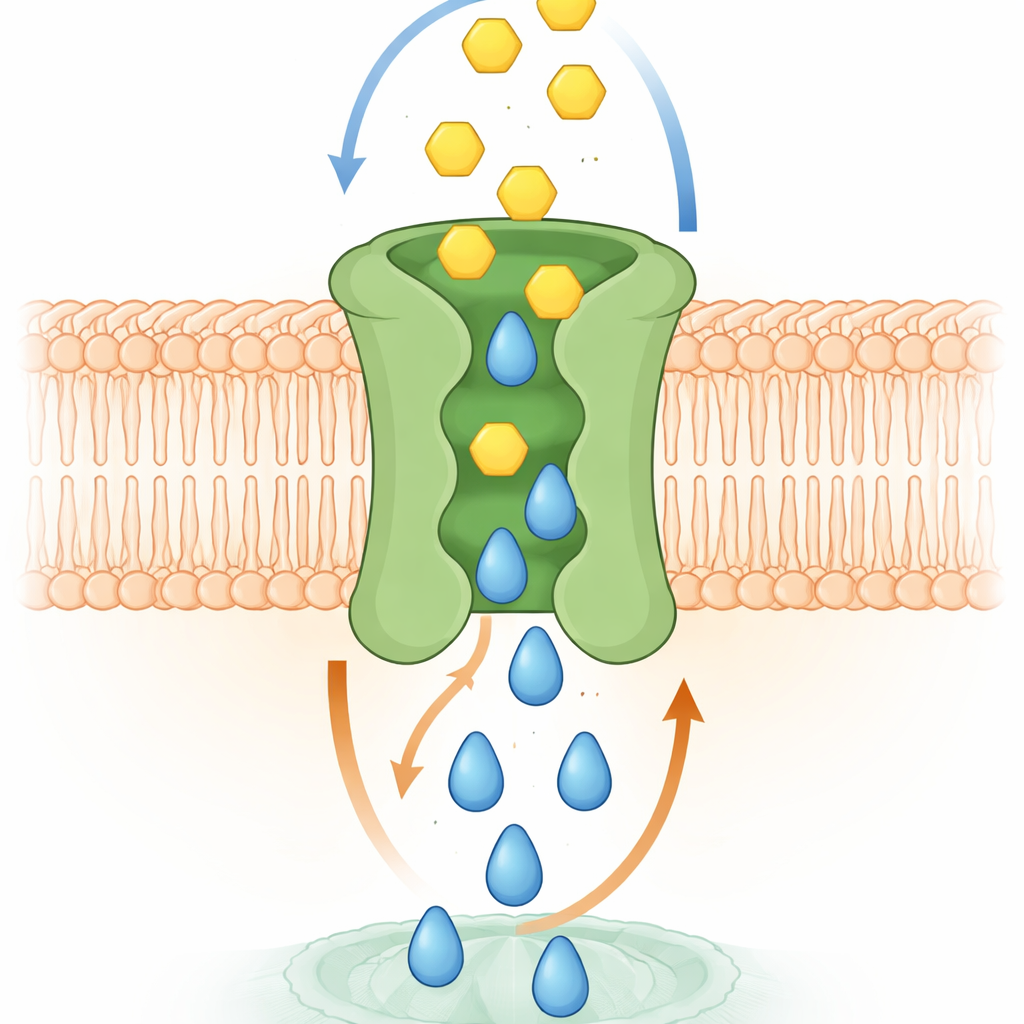
Hur det molekylära bytet sannolikt fungerar
Datorsimuleringar och strukturella experiment bidrog till att förklara mekanismen. Högupplösta modeller av SPNS2 i ett membran visade S1P glida uppåt genom ett centralt hålrum, vilket utlöste subtila formförändringar som öppnade tillfälliga fickor för glukos på utsidan. När S1P rör sig mot utsidan kan glukos fästa i dessa fickor och sedan glida ner genom samma centrala kanal mot cellens inre. Forskarna identifierade specifika aminosyror som kontaktar glukos i dessa fickor. När dessa rester muterades minskade glukosbindningen och transporten misslyckades, även om de förändrade proteinerna fortfarande nådde cellens yta. I levande celler försvagade förlusten av denna kopplade transport S1P‑drivna processer såsom celltillväxt, rörelse för att täta en sår‑liknande öppning och endotelcellers förmåga att bilda ett tätt barriärskikt — funktioner som kräver både signal och energi.
Varför detta är viktigt för hälsa och sjukdom
Genom att avslöja att SPNS2 är en tvåvägsgrind — som skickar ut S1P samtidigt som den tar in glukos — kopplar detta arbete en stark signalsubstans till grundläggande energiförsörjning i ett enda steg. När SPNS2 frigör S1P för att utlösa immun- eller vaskulära svar hjälper den samtidigt celler att importera extra bränsle för att driva dessa åtgärder. Störningar i denna koppling kan bidra till högt blodsocker, förlust av socker via njurarna och insulin‑oberoende former av rubbad glukosreglering. Eftersom SPNS2 och S1P‑signalering också påverkar cancerspridning, inflammation och blodkärlsintegritet, kan riktade insatser mot denna ”signal‑och‑socker” grindvakt öppna nya vägar för att behandla metabola sjukdomar, autoimmuna tillstånd och tumörer som förlitar sig på både ökad signalering och ökat glukosupptag.
Citering: Weigel, C., Hossen, M.L., Brown, R.D.R. et al. SPNS2 exports sphingosine-1-phosphate and imports glucose. Nat Commun 17, 3901 (2026). https://doi.org/10.1038/s41467-026-71659-7
Nyckelord: glukostransport, sphingosine-1-phosphate, membrantransportör, endotelbiologi, metaboliskt signalering