Clear Sky Science · fr
SPNS2 exporte la sphingosine‑1‑phosphate et importe le glucose
Un gardien caché du sucre et des signaux cellulaires
Notre organisme jongle en permanence avec des milliers de signaux chimiques tout en maintenant la glycémie dans une plage sûre. Cette étude met au jour un acteur inattendu qui participe à ces deux tâches simultanément : une petite protéine appelée SPNS2, située dans les membranes cellulaires. Les chercheurs montrent que SPNS2 non seulement libère une molécule lipidique signal importante pour l’immunité et les vaisseaux sanguins, mais aide en même temps à faire entrer le glucose — le principal carburant de l’organisme — dans les cellules. Ce double rôle relie la communication intercellulaire à l’alimentation cellulaire, avec des implications pour le diabète, les maladies cardiovasculaires et le cancer.
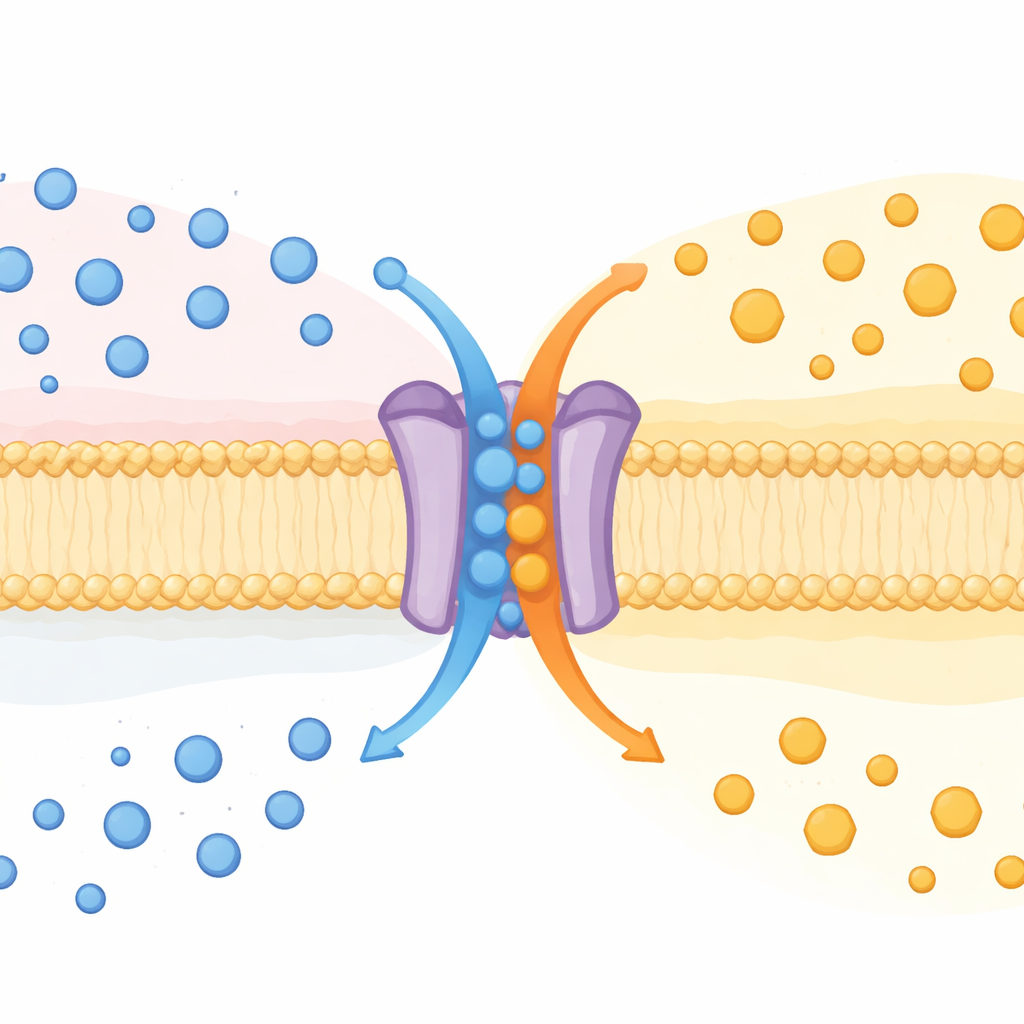
Une protéine, deux fonctions
On savait depuis longtemps que SPNS2 exporte une molécule messagère appelée sphingosine‑1‑phosphate (S1P) hors des cellules. La S1P circule dans le sang et la lymphe, guidant les cellules immunitaires, façonnant les vaisseaux sanguins et influençant l’inflammation. Jusqu’ici, SPNS2 était considéré comme un exportateur unidirectionnel. En étudiant des souris dépourvues du gène Spns2, ainsi que de nombreux types de cellules en culture, les auteurs ont découvert que SPNS2 se comporte en réalité davantage comme une machine d’échange. Il expédie la S1P vers l’extérieur tout en faisant entrer du glucose, à la manière d’un « antiport », une classe de transporteurs qui échangent une substance contre une autre à travers la membrane.
Que se passe‑t‑il quand SPNS2 manque
Chez des souris génétiquement modifiées pour ne pas exprimer SPNS2, les niveaux de S1P dans le sang et la lymphe ont diminué, tandis que la S1P s’est accumulée dans des tissus tels que le foie, le rein, le poumon et le cœur — exactement ce que l’on attendrait si un exportateur était désactivé. Mais leur équilibre sucré était aussi perturbé. La glycémie augmentait, et du glucose supplémentaire apparaissait dans l’urine et les selles, tandis que plusieurs organes présentaient des niveaux internes de glucose plus faibles. L’imagerie avec un traceur radioactif analogue du glucose a révélé que ces souris absorbaient normalement le sucre au niveau intestinal, mais que leurs tissus — et en particulier leurs reins — étaient mauvais pour récupérer le glucose depuis la circulation sanguine et depuis l’urine filtrée. Ensemble, ces résultats indiquent un défaut d’entrée du glucose dans les cellules et de sa réutilisation, malgré des taux d’insuline et des signaux hormonaux normaux.
SPNS2 attire le carburant pendant qu’il expulse les signaux
Pour tester si SPNS2 transporte directement le glucose, l’équipe a modulé son expression dans des cellules vasculaires et d’autres types cellulaires. Lorsqu’ils ont augmenté SPNS2, les cellules ont libéré davantage de S1P dans le milieu et ont absorbé plus de glucose, produisant plus d’énergie et montrant une respiration et une oxydation du sucre renforcées. Lorsqu’ils ont supprimé ou bloqué SPNS2, les cellules ont retenu la S1P à l’intérieur et pris moins de glucose. Ces effets persistaient même lorsque les transporteurs classiques du glucose (comme GLUT1 et GLUT3) étaient inhibés, et ils ne dépendaient ni des récepteurs de la S1P à la surface cellulaire ni de l’insuline. Dans des « protéoliposomes » artificiels soigneusement contrôlés — de petites bulles fabriquées en laboratoire avec la SPNS2 purifiée insérée dans leur membrane — la protéine pouvait directement faire entrer du glucose fluorescent ou radioactif, mais seulement efficacement lorsque la S1P était présente du côté interne. Cela montra que SPNS2 peut agir elle‑même comme importeur de glucose couplé à l’export de S1P.
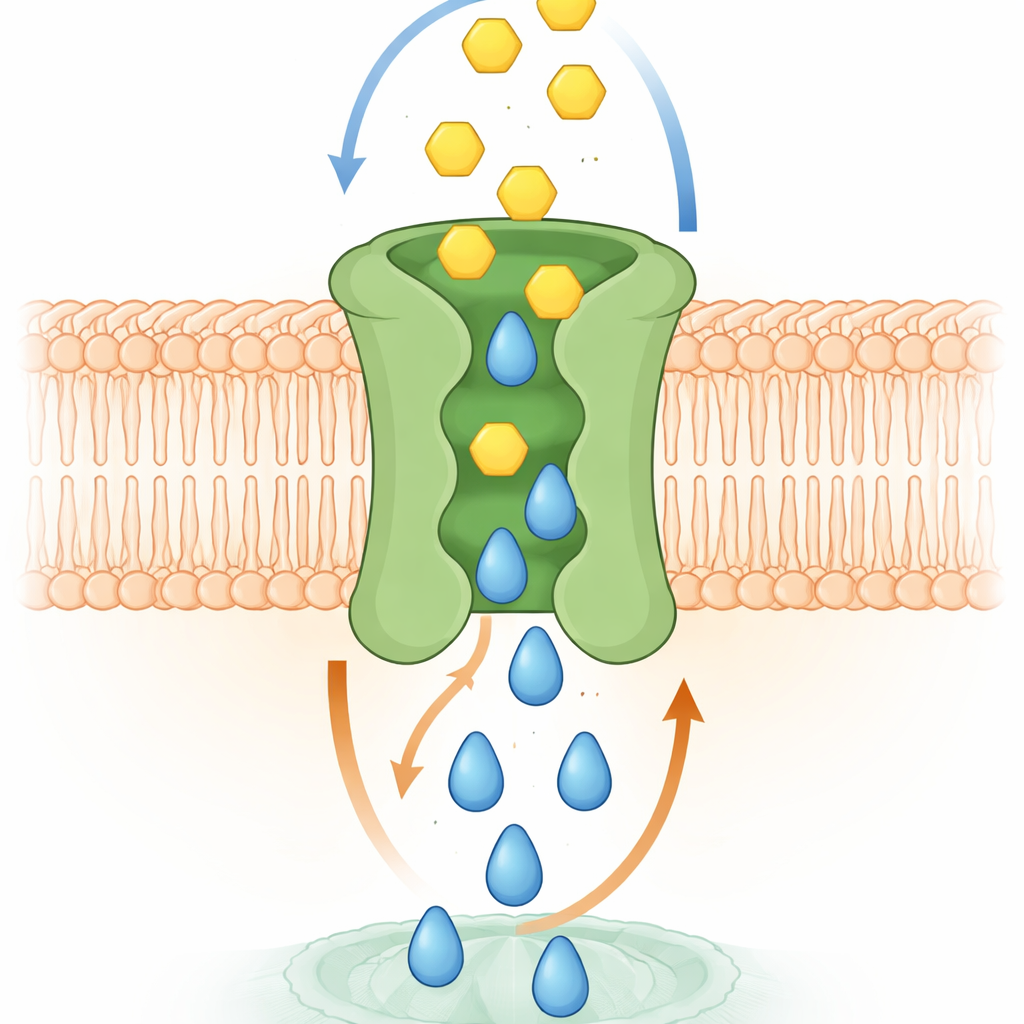
Comment l’échange moléculaire fonctionne probablement
Des simulations informatiques et des expériences structurales ont aidé à expliquer le mécanisme. Des modèles haute résolution de SPNS2 dans une membrane montrent la S1P glissant vers le haut à travers une cavité centrale, provoquant de subtils changements de conformation qui ouvrent des poches temporaires pour le glucose du côté externe. À mesure que la S1P se déplace vers l’extérieur, le glucose peut se fixer dans ces poches puis glisser le long de la même voie centrale vers l’intérieur de la cellule. Les chercheurs ont identifié des acides aminés spécifiques qui contactent le glucose dans ces poches. Quand ces résidus ont été mutés, l’affinité pour le glucose a chuté et le transport a échoué, même si les protéines modifiées atteignaient toujours la surface cellulaire. Dans les cellules vivantes, la perte de ce transport couplé affaiblissait des processus entraînés par la S1P, tels que la croissance cellulaire, le déplacement pour refermer une lacune simulant une plaie, et la capacité des couches endothéliales à former une barrière étanche — fonctions qui requièrent à la fois signal et énergie.
Pourquoi cela compte pour la santé et la maladie
En révélant que SPNS2 est une porte bidirectionnelle — envoyant la S1P vers l’extérieur tout en faisant entrer le glucose — ce travail relie en une seule étape une molécule de signalisation puissante à l’approvisionnement énergétique fondamental. Quand SPNS2 libère la S1P pour déclencher des réponses immunes ou vasculaires, il aide simultanément les cellules à importer le carburant supplémentaire pour alimenter ces actions. Des perturbations de ce couplage pourraient contribuer à l’hyperglycémie, à la perte de glucose par les reins et à des formes d’altération du métabolisme du glucose indépendantes de l’insuline. Parce que SPNS2 et la signalisation par la S1P influencent aussi la dissémination des cancers, l’inflammation et l’intégrité vasculaire, cibler ce « gardien du signal et du sucre » pourrait ouvrir de nouvelles pistes pour traiter les maladies métaboliques, les troubles auto‑immuns et les tumeurs qui dépendent à la fois d’une signalisation accrue et d’une captation de glucose élevée.
Citation: Weigel, C., Hossen, M.L., Brown, R.D.R. et al. SPNS2 exports sphingosine-1-phosphate and imports glucose. Nat Commun 17, 3901 (2026). https://doi.org/10.1038/s41467-026-71659-7
Mots-clés: transport du glucose, sphingosine‑1‑phosphate, transporteur membranaire, biologie endothéliale, signalisation métabolique