Clear Sky Science · pt
SPNS2 exporta esfingosina-1-fosfato e importa glicose
Um guardião oculto do açúcar e dos sinais celulares
Nossos corpos equilibram constantemente milhares de sinais químicos enquanto mantêm a glicemia em faixa segura. Este estudo revela um agente inesperado que ajuda em ambas as tarefas simultaneamente: uma pequena proteína chamada SPNS2 que fica na membrana celular. Os pesquisadores mostram que a SPNS2 não apenas libera uma molécula lipídica sinalizadora importante para a imunidade e os vasos sanguíneos, mas também ajuda a captar glicose — o principal combustível do corpo — para dentro das células. Esse papel duplo conecta a comunicação celular ao modo como as células se nutrem, com implicações para diabetes, doenças cardiovasculares e câncer.
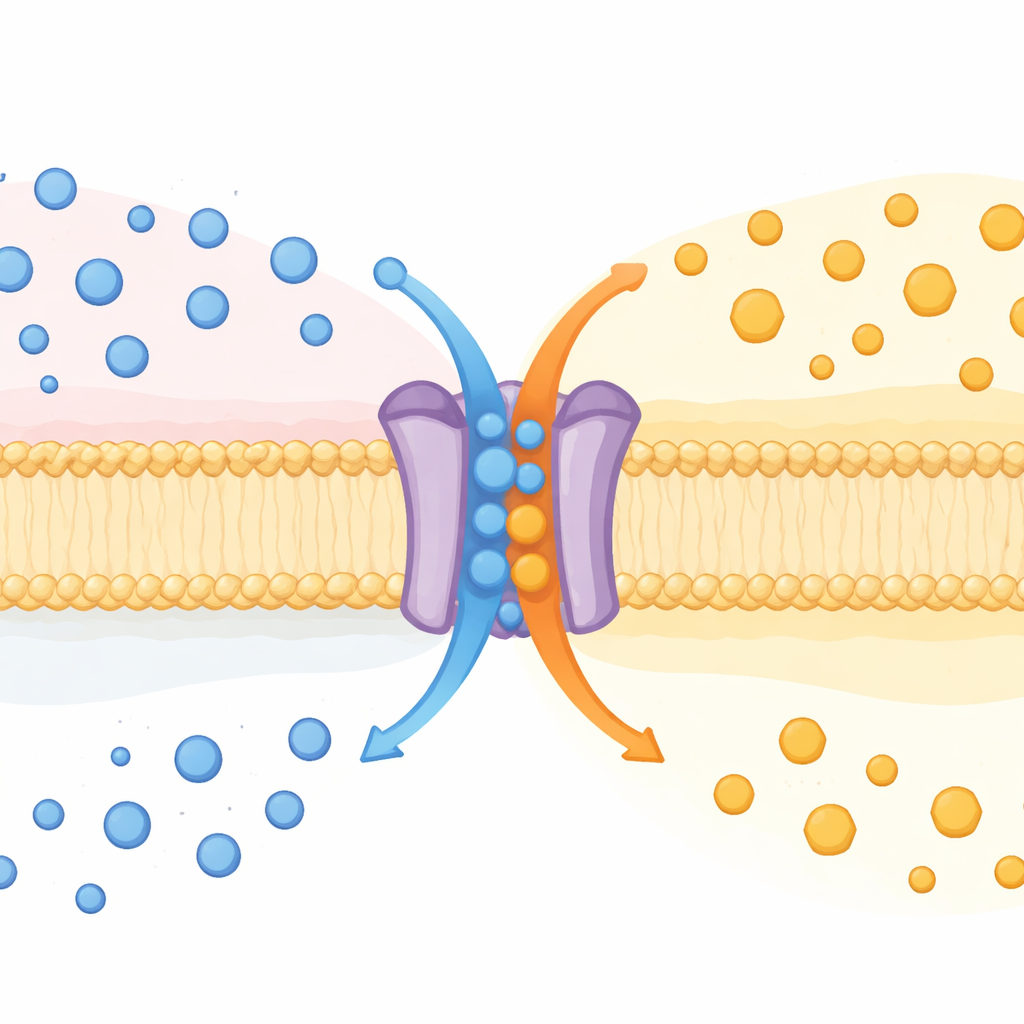
Uma proteína, duas funções
A SPNS2 há muito é conhecida por mover uma molécula mensageira chamada esfingosina‑1‑fosfato (S1P) para fora das células. O S1P circula no sangue e na linfa, guiando células imunes, moldando vasos sanguíneos e influenciando a inflamação. Até agora, a SPNS2 era vista como um exportador unidirecional. Ao estudar camundongos sem o gene Spns2, junto com muitos tipos de células em cultura, os autores descobriram que a SPNS2 na verdade se comporta mais como uma máquina de troca. Ela exporta S1P enquanto importa glicose, de modo semelhante a um “antiporter”, uma classe de transportadores que trocam uma substância por outra através da membrana.
O que acontece quando a SPNS2 está ausente
Em camundongos geneticamente modificados para não terem SPNS2, os níveis de S1P no sangue e na linfa caíram, enquanto o S1P se acumulou em tecidos como fígado, rim, pulmão e coração — exatamente o esperado se um exportador tivesse sido desativado. Mas o equilíbrio de açúcares também ficou perturbado. A glicemia subiu, e glicose extra apareceu na urina e nas fezes, enquanto vários órgãos mostraram níveis internos de glicose mais baixos. Imagens com um traçador radioativo análogo à glicose revelaram que esses camundongos absorviam açúcar do intestino normalmente, mas seus tecidos — e especialmente os rins — eram pobres em recuperar glicose da corrente sanguínea e da urina filtrada. Em conjunto, esses achados apontaram para um defeito em fazer a glicose entrar nas células e reutilizá‑la, apesar de níveis normais de insulina e sinais hormonais.
SPNS2 puxa combustível enquanto empurra sinais
Para testar se a própria SPNS2 movimenta glicose, a equipe manipulou seus níveis em células endoteliais e outros tipos celulares. Quando aumentaram a SPNS2, as células liberaram mais S1P para o meio e captaram mais glicose, produzindo mais energia e exibindo respiração e queima de açúcar mais intensas. Quando deletaram ou bloquearam a SPNS2, as células retiveram S1P internamente e captaram menos glicose. Esses efeitos persistiram mesmo quando transportadores clássicos de açúcar (como GLUT1 e GLUT3) foram inibidos, e não dependiam dos receptores de S1P na superfície celular nem da insulina. Em proteolipossomos artificiais cuidadosamente controlados — pequenas bolhas feitas em laboratório com SPNS2 purificada inserida em suas membranas — a proteína pôde mover diretamente glicose marcada fluorescente ou radioativa para dentro, mas apenas com eficiência quando S1P estava presente no lado interno. Isso mostrou que a própria SPNS2 pode agir como importador de glicose acoplado à exportação de S1P.
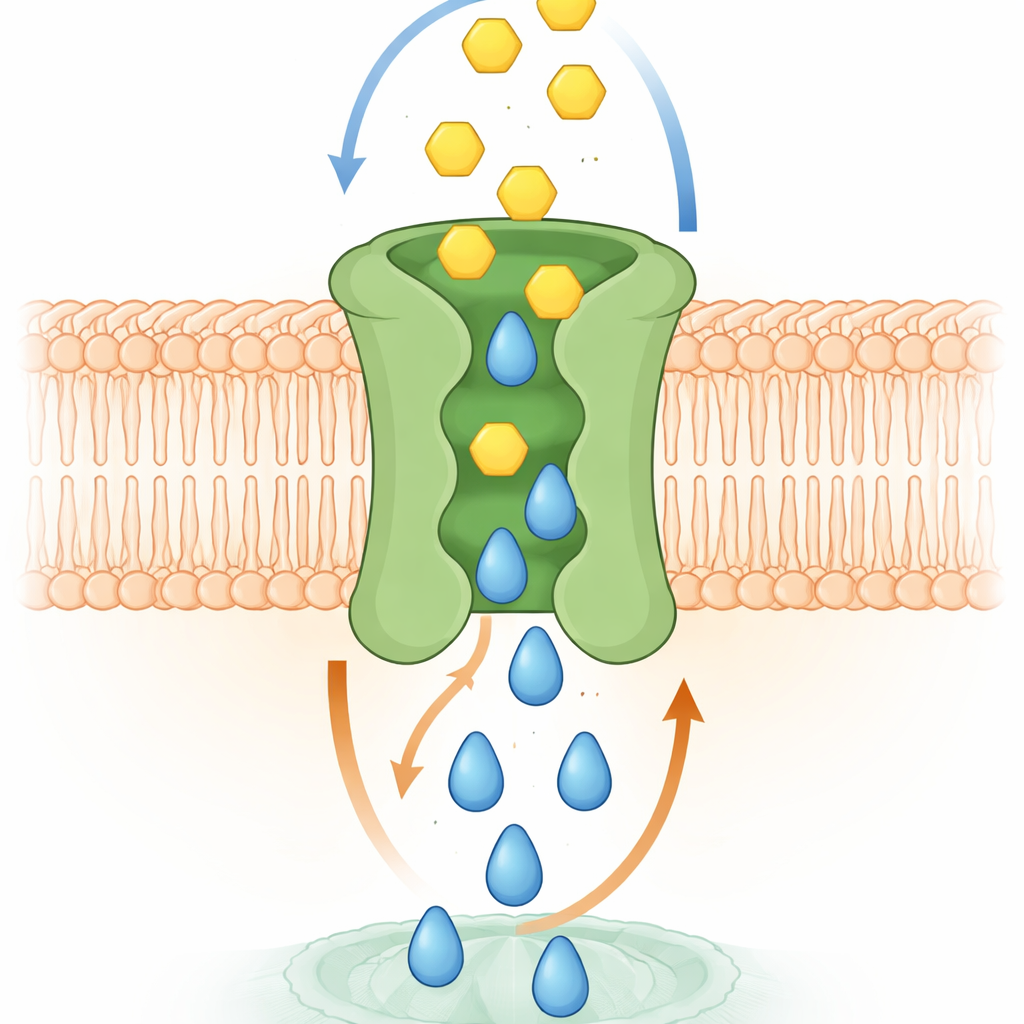
Como a troca molecular provavelmente funciona
Simulações por computador e experimentos estruturais ajudaram a explicar o mecanismo. Modelos de alta resolução da SPNS2 em uma membrana mostraram o S1P deslizando para cima através de uma cavidade central, desencadeando mudanças sutis de forma que abrem bolsões temporários para a glicose no lado externo. À medida que o S1P se move para fora, a glicose pode se acomodar nesses bolsões e então deslizar pelo mesmo caminho central em direção ao interior celular. Os pesquisadores identificaram aminoácidos específicos que fazem contato com a glicose nesses bolsões. Quando esses resíduos foram mutados, a ligação à glicose diminuiu e o transporte falhou, mesmo que as proteínas alteradas ainda chegassem à superfície celular. Em células vivas, a perda desse transporte acoplado enfraqueceu processos impulsionados por S1P, como crescimento celular, migração para fechar uma lacuna semelhante a uma ferida e a capacidade das camadas endoteliais de formar uma barreira estanque — funções que exigem tanto sinalização quanto energia.
Por que isso importa para saúde e doença
Ao revelar que a SPNS2 é um portão dupla via — enviando S1P enquanto traz glicose — este trabalho liga uma molécula sinalizadora poderosa ao fornecimento básico de energia em um único passo. Quando a SPNS2 libera S1P para disparar respostas imunes ou vasculares, ela simultaneamente ajuda as células a importar combustível extra para alimentar essas ações. Disrupções nesse acoplamento podem contribuir para hiperglicemia, perda renal de glicose e formas de desregulação glicêmica independentes da insulina. Como a SPNS2 e a sinalização por S1P também influenciam a disseminação do câncer, inflamação e integridade dos vasos, mirar nesse guardião “sinal‑e‑açúcar” pode abrir novas vias para tratar doenças metabólicas, condições autoimunes e tumores que dependem tanto de sinalização ampliada quanto de aumento da captação de glicose.
Citação: Weigel, C., Hossen, M.L., Brown, R.D.R. et al. SPNS2 exports sphingosine-1-phosphate and imports glucose. Nat Commun 17, 3901 (2026). https://doi.org/10.1038/s41467-026-71659-7
Palavras-chave: transporte de glicose, esfingosina-1-fosfato, transportador de membrana, biologia endotelial, sinalização metabólica