Clear Sky Science · es
SPNS2 exporta esfingosina‑1‑fosfato e importa glucosa
Un guardián oculto del azúcar y las señales celulares
Nuestros cuerpos gestionan constantemente miles de señales químicas mientras mantienen la glucosa en sangre dentro de un rango seguro. Este estudio descubre un actor inesperado que ayuda a ambas funciones a la vez: una pequeña proteína llamada SPNS2 que se ubica en las membranas celulares. Los investigadores muestran que SPNS2 no solo libera una grasa señalizadora importante para la inmunidad y los vasos sanguíneos, sino que al mismo tiempo ayuda a introducir glucosa —el combustible principal del organismo— en las células. Este papel dual conecta la comunicación intercelular con la manera en que las células se alimentan, con implicaciones para la diabetes, las enfermedades cardiovasculares y el cáncer.
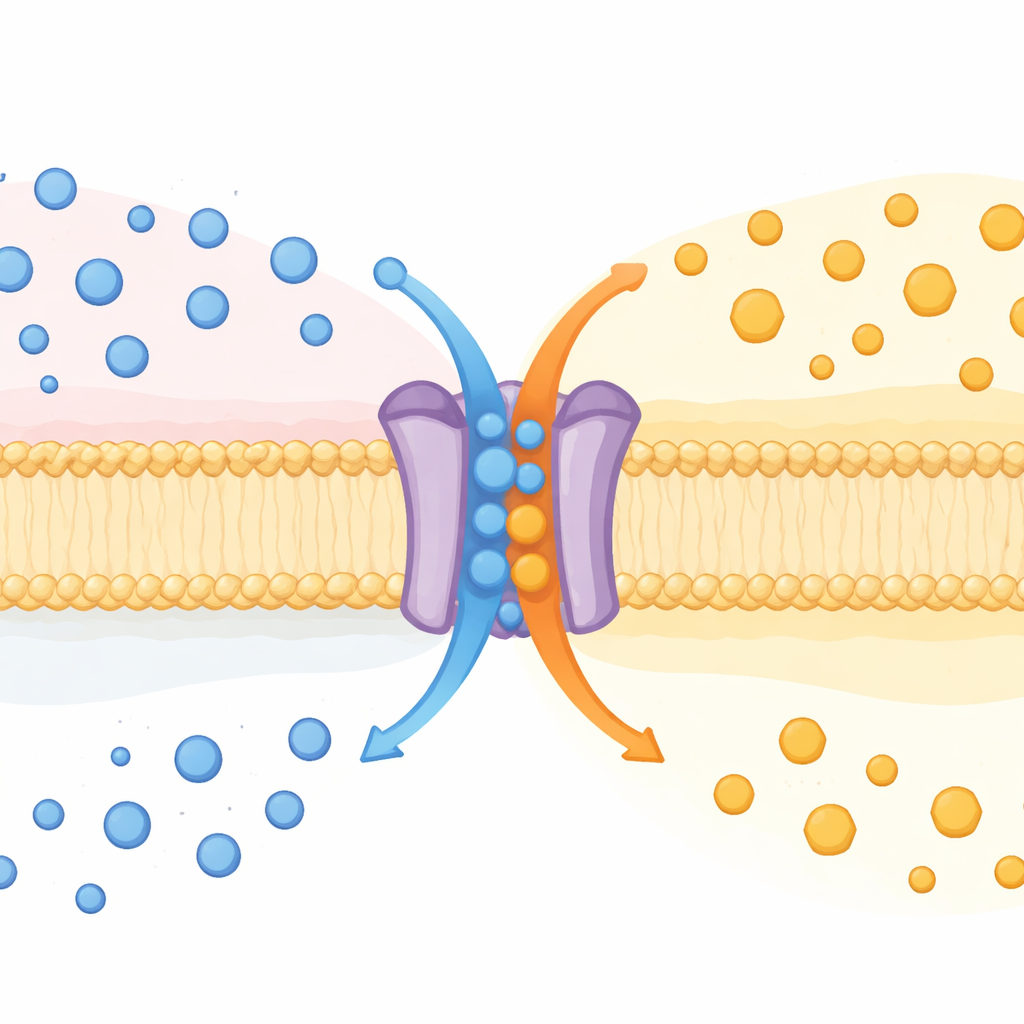
Una proteína, dos funciones
Hace tiempo se conoce que SPNS2 moviliza una molécula mensajera llamada esfingosina‑1‑fosfato (S1P) fuera de las células. S1P circula en la sangre y la linfa, orientando a las células inmunitarias, moldeando los vasos sanguíneos e influyendo en la inflamación. Hasta ahora, se pensaba en SPNS2 como un exportador unidireccional. Al estudiar ratones sin el gen Spns2, junto con muchos tipos de células en cultivo, los autores descubrieron que SPNS2 se comporta más como una máquina de intercambio. Expulsa S1P mientras introduce glucosa, de forma similar a un “antiporte”, una clase de transportadores que intercambian una sustancia por otra a través de la membrana.
Qué ocurre cuando falta SPNS2
En ratones diseñados genéticamente para carecer de SPNS2, los niveles de S1P en sangre y linfa disminuyeron, mientras que S1P se acumuló en tejidos como hígado, riñón, pulmón y corazón —exactamente lo esperado si se hubiera desactivado un exportador. Pero su equilibrio de azúcares también se alteró. La glucosa sanguínea aumentó y apareció glucosa extra en orina y heces, mientras que varios órganos mostraron niveles internos de glucosa más bajos. Imagenología con un trazador radiactivo similar a la glucosa reveló que estos ratones absorbían azúcar desde el intestino con normalidad, pero sus tejidos —y en especial los riñones— eran deficientes para recuperar glucosa desde la sangre y desde la orina filtrada. En conjunto, estos hallazgos apuntaron a un defecto en la entrada de glucosa en las células y en su reutilización, a pesar de niveles normales de insulina y señales hormonales.
SPNS2 toma combustible mientras expulsa señales
Para comprobar si SPNS2 mueve glucosa, el equipo manipuló sus niveles en células vasculares y otros tipos celulares. Cuando aumentaron SPNS2, las células liberaron más S1P al medio y absorbieron más glucosa, produciendo más energía y mostrando mayor respiración y quema de azúcares. Cuando eliminaron o bloquearon SPNS2, las células retuvieron S1P y captaron menos glucosa. Estos efectos persistieron incluso cuando se inhibieron los transportadores clásicos de azúcar (como GLUT1 y GLUT3), y no dependían de los receptores de S1P en la superficie celular ni de la insulina. En proteoliposomas cuidadosamente controlados —pequeñas burbujas sintéticas con SPNS2 purificado insertado en sus membranas—, la proteína pudo mover directamente glucosa fluorescente o radiactiva hacia el interior, pero solo de manera eficiente cuando S1P estaba presente en el lado interno. Esto demostró que SPNS2 puede actuar por sí misma como importador de glucosa acoplado a la exportación de S1P.
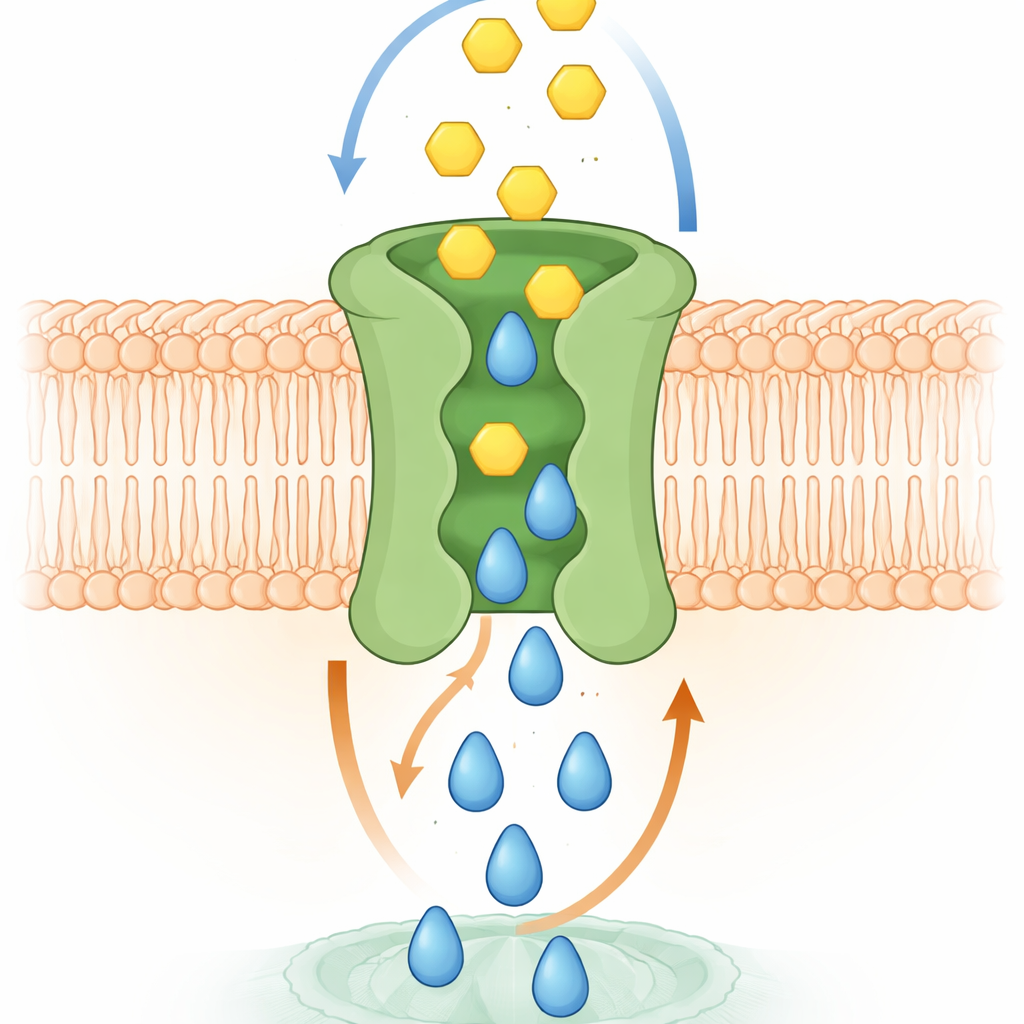
Cómo funciona probablemente el intercambio molecular
Simulaciones por ordenador y experimentos estructurales ayudaron a explicar el mecanismo. Modelos de alta resolución de SPNS2 en una membrana mostraron a S1P deslizándose hacia arriba a través de una cavidad central, provocando cambios sutiles de forma que abren bolsillos temporales para la glucosa en el lado exterior. A medida que S1P se mueve hacia el exterior, la glucosa puede alojarse en esos bolsillos y luego deslizarse por la misma vía central hacia el interior celular. Los investigadores identificaron aminoácidos específicos que contactan la glucosa en esos bolsillos. Cuando se mutaron esos residuos, la unión de glucosa disminuyó y el transporte falló, aunque las proteínas alteradas aún llegaban a la superficie celular. En células vivas, perder este transporte acoplado debilitó procesos impulsados por S1P como el crecimiento celular, el movimiento para cerrar una brecha semejante a una herida y la capacidad de las capas endoteliales para formar una barrera cerrada —funciones que requieren tanto señalización como energía.
Por qué importa para la salud y la enfermedad
Al revelar que SPNS2 es una puerta bidireccional —envía S1P mientras trae glucosa—, este trabajo conecta una potente molécula señal con el suministro básico de energía en un solo paso. Cuando SPNS2 libera S1P para desencadenar respuestas inmunitarias o vasculares, simultáneamente ayuda a las células a importar combustible extra para alimentar esas acciones. Las alteraciones en este acoplamiento pueden contribuir a hiperglucemia, pérdida de glucosa por el riñón y formas de manejo glucémico alterado independientes de la insulina. Dado que SPNS2 y la señalización por S1P también influyen en la diseminación del cáncer, la inflamación y la integridad vascular, dirigir este guardián “señal‑y‑azúcar” podría abrir nuevas vías para tratar enfermedades metabólicas, condiciones autoinmunes y tumores que dependen tanto de señalización aumentada como de mayor captación de glucosa.
Cita: Weigel, C., Hossen, M.L., Brown, R.D.R. et al. SPNS2 exports sphingosine-1-phosphate and imports glucose. Nat Commun 17, 3901 (2026). https://doi.org/10.1038/s41467-026-71659-7
Palabras clave: transporte de glucosa, esfingosina‑1‑fosfato, transportador de membrana, biología endotelial, señalización metabólica