Clear Sky Science · ru
SPNS2 выталкивает сфингозин‑1‑фосфат и импортирует глюкозу
Скрытый привратник для сахара и клеточных сигналов
Наш организм постоянно управляет тысячами химических сигналов, одновременно поддерживая уровень сахара в крови в безопасных пределах. Это исследование выявляет неожиданный компонент, который помогает делать и то, и другое одновременно: небольшой белок SPNS2, расположенный в клеточных мембранах. Авторы показывают, что SPNS2 не только экспортирует сигнальную жировую молекулу, важную для иммунитета и сосудов, но и одновременно способствует поступлению глюкозы — главного топлива организма — в клетки. Такая двойная роль связывает межклеточную коммуникацию с клеточным питанием и имеет значение для понимания диабета, сердечно‑сосудистых заболеваний и рака.
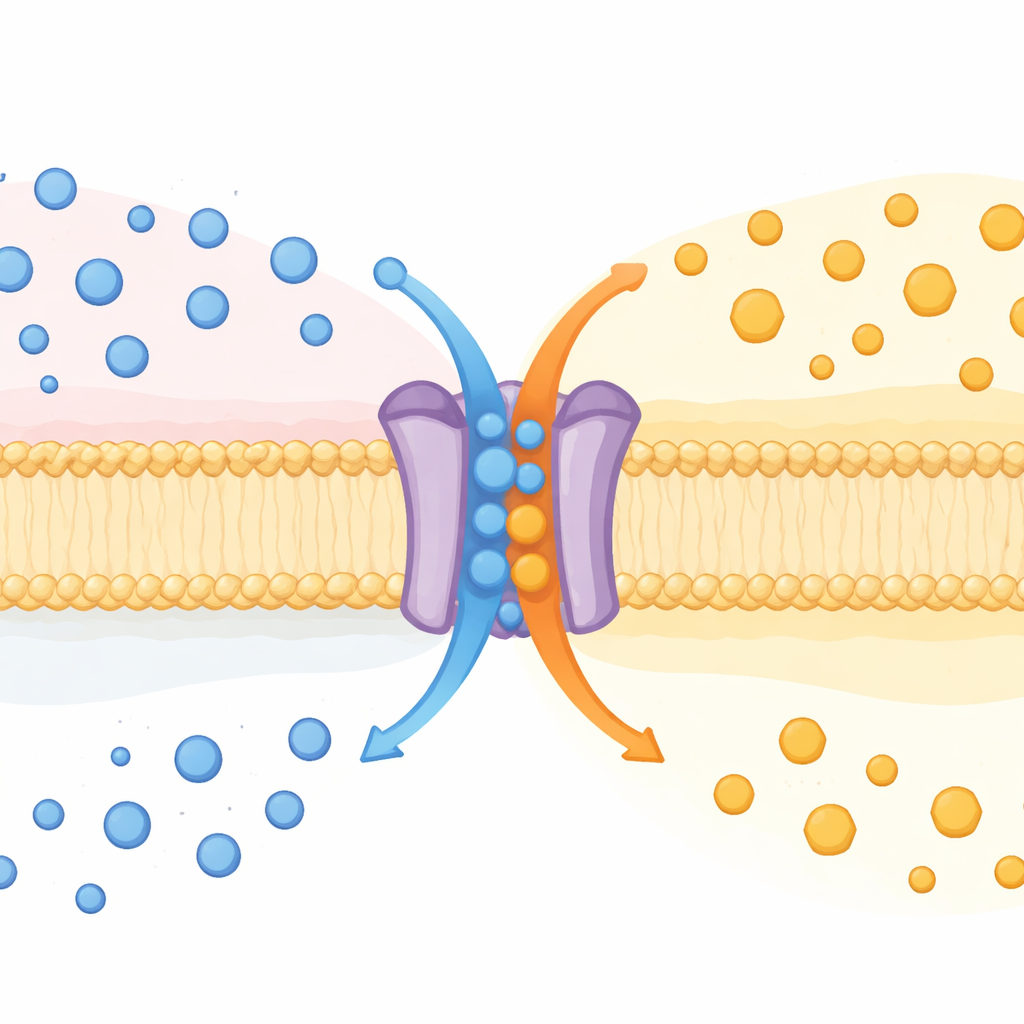
Один белок — две функции
Долгое время SPNS2 был известен как переносчик, выводящий из клеток молекулу‑мессенджер сфингозин‑1‑фосфат (S1P). S1P циркулирует в крови и лимфе, направляет иммунные клетки, формирует сосуды и влияет на воспаление. Ранее SPNS2 считали односторонним экспортером. Изучая мышей с выключенным геном Spns2 и различные типы культивируемых клеток, авторы обнаружили, что SPNS2 фактически работает скорее как обменник: он выталкивает S1P наружу и одновременно ввозит глюкозу, подобно «антипортеру» — классу транспортеров, которые меняют местами вещества через мембрану.
Что происходит при отсутствии SPNS2
У генетически модифицированных мышей без SPNS2 уровни S1P в крови и лимфе снизились, тогда как S1P накапливался в тканях, таких как печень, почки, легкие и сердце — именно то, чего следовало ожидать при отключении экспортёра. Но у них также нарушался сахарный гомеостаз. Глюкоза в крови повышалась, лишняя глюкоза появлялась в моче и фекалиях, а в ряде органов снижался внутриклеточный уровень глюкозы. Визуализация с помощью радиомеченого подобия глюкозы показала, что эти мыши нормально усваивали сахар из кишечника, но их ткани — особенно почки — плохо возвращали глюкозу из крови и фильтрата мочи. В совокупности данные указывали на дефект в захвате глюкозы клетками и её повторном использовании, несмотря на нормальные уровни инсулина и гормональные сигналы.
SPNS2 притягивает топливо, выталкивая сигналы
Чтобы проверить, переносит ли SPNS2 сам глюкозу, исследователи меняли его уровни в эндотелиальных и других клетках. При повышении экспрессии SPNS2 клетки выделяли больше S1P в окружающую среду и поглощали больше глюкозы, производя больше энергии и демонстрируя усиленное дыхание и окисление сахаров. При удалении или блокаде SPNS2 S1P оставался внутри клеток, а захват глюкозы снижался. Эти эффекты сохранялись даже при ингибировании классических переносчиков сахара (таких как GLUT1 и GLUT3) и не зависели от рецепторов S1P на поверхности клетки или от инсулина. В тщательно контролируемых искусственных «протеолипосомах» — крошечных лабораторных пузырьках с очищенным SPNS2, встроенным в мембрану — белок мог непосредственно переносить флуоресцентную или радиомеченую глюкозу внутрь, но эффективно только когда S1P присутствовал на внутренней стороне. Это показало, что сам SPNS2 может действовать как импортер глюкозы, связанный с экспортом S1P.
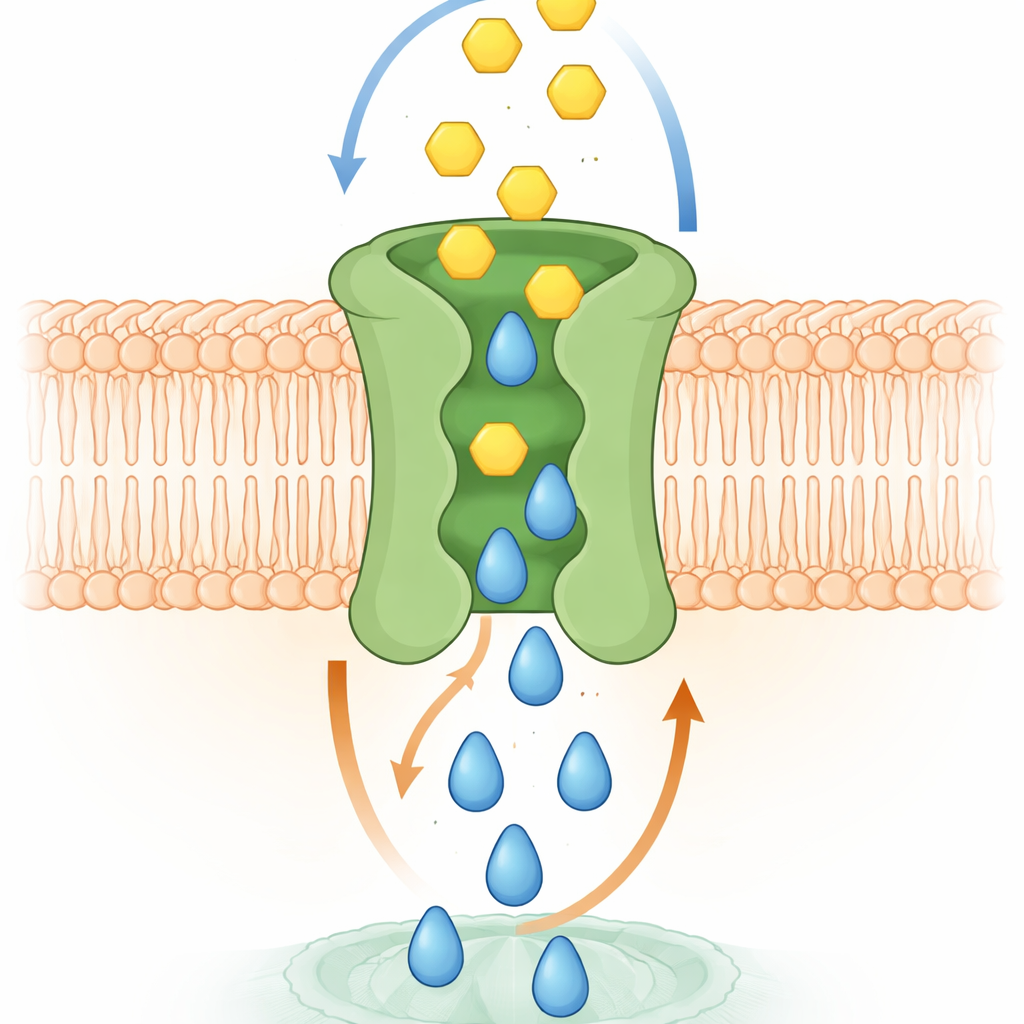
Как, вероятно, работает молекулярный обмен
Компьютерное моделирование и структурные эксперименты помогли объяснить механизм. Высокоточные модели SPNS2 в мембране показали, как S1P скользит вверх через центральную полость, вызывая тонкие изменения конформации, которые открывают временные карманы для глюкозы на внешней стороне. По мере продвижения S1P наружу глюкоза может встать в эти карманы, а затем проследовать по тому же центральному пути внутрь клетки. Авторы выделили специфические аминокислоты, контактирующие с глюкозой в этих карманах. При мутациях этих остатков связывание глюкозы снижалось, и транспорт не работал, хотя изменённые белки всё ещё достигали поверхности клетки. В живых клетках утрата этого сопряжённого транспорта ослабляла S1P‑опосредованные процессы, такие как клеточный рост, движение для заживления «раноподобного» разрыва и способность эндотелиальных слоев формировать плотный барьер — функции, требующие и сигнала, и энергии.
Почему это важно для здоровья и болезней
Показав, что SPNS2 является двунаправленной «вратой» — выпускающей S1P и одновременно ввозящей глюкозу, — работа связывает мощную сигнальную молекулу с базовым снабжением энергией в одном шаге. Когда SPNS2 высвобождает S1P для запуска иммунных или сосудистых ответов, он одновременно помогает клеткам импортировать дополнительное топливо для выполнения этих действий. Нарушения этой связи могут способствовать повышенному уровню сахара в крови, потере глюкозы почками и формам дисрегуляции глюкозы, независимым от инсулина. Поскольку SPNS2 и S1P‑сигнализация также участвуют в метастазировании, воспалении и поддержании целостности сосудов, воздействие на этот «сигнально‑сахарный» привратник может открыть новые подходы к лечению метаболических заболеваний, аутоиммунных состояний и опухолей, зависящих от усиленной сигнализации и повышенного поглощения глюкозы.
Цитирование: Weigel, C., Hossen, M.L., Brown, R.D.R. et al. SPNS2 exports sphingosine-1-phosphate and imports glucose. Nat Commun 17, 3901 (2026). https://doi.org/10.1038/s41467-026-71659-7
Ключевые слова: перенос глюкозы, сфингозин‑1‑фосфат, мембранный транспортер, эндоТелиальная биология, метаболическая сигнализация