Clear Sky Science · nl
SPNS2 exporteert sphingosine-1-fosfaat en importeert glucose
Een verborgen poortwachter voor suiker en celsignalen
Ons lichaam jongleert continu met duizenden chemische signalen en houdt tegelijk de bloedsuikerspiegel binnen veilige grenzen. Deze studie onthult een onverwachte speler die beide taken tegelijk helpt uitvoeren: een klein eiwit genaamd SPNS2 dat in celmembranen zit. De onderzoekers tonen aan dat SPNS2 niet alleen een signaalvetmolecuul dat belangrijk is voor immuniteit en bloedvaten vrijgeeft, maar tegelijk ook helpt glucose — de belangrijkste brandstof van het lichaam — in cellen te brengen. Deze dubbele rol koppelt hoe cellen met elkaar communiceren aan hoe ze zichzelf voeden, met implicaties voor diabetes, hartziekten en kanker.
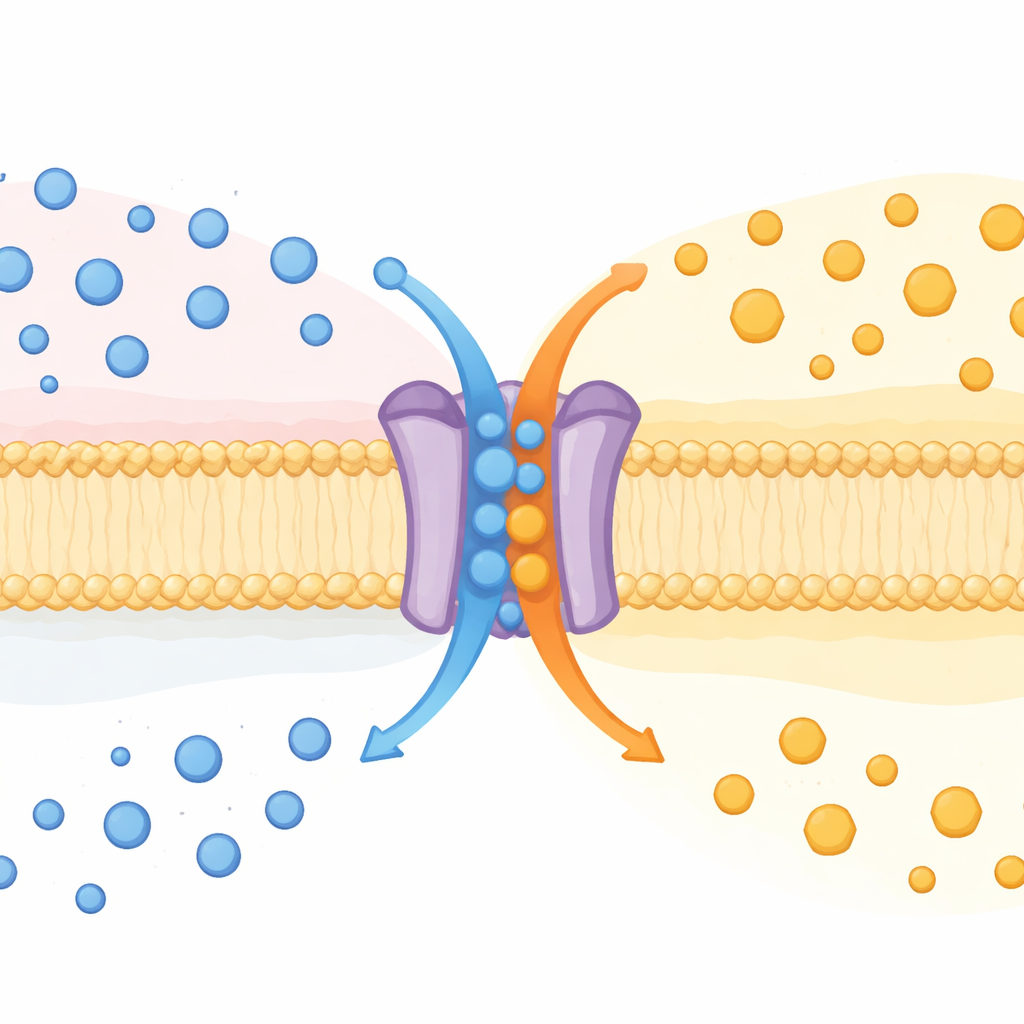
Één eiwit, twee taken
SPNS2 stond al langer bekend als transporter die de boodschapper sphingosine‑1‑fosfaat (S1P) uit cellen verplaatst. S1P circuleert in bloed en lymfe, stuurt immuuncellen, vormt bloedvaten en beïnvloedt ontstekingsreacties. Tot nu toe werd SPNS2 gezien als een eenrichtingsexporteur. Door muizen zonder het Spns2-gen te bestuderen, samen met veel verschillende gecultiveerde cellen, ontdekten de auteurs dat SPNS2 zich eerder gedraagt als een ruilmachine. Het voert S1P naar buiten terwijl het glucose naar binnen brengt, op een manier vergelijkbaar met een „antiporter”, een klasse transporters die de ene stof ruilt tegen een andere door membranen heen.
Wat gebeurt er als SPNS2 ontbreekt
In muizen die zodanig zijn gemodificeerd dat SPNS2 ontbreekt, daalden de S1P-niveaus in bloed en lymfe, terwijl S1P zich ophoopte in weefsels zoals lever, nier, long en hart — precies wat je zou verwachten als een exporteur buiten werking is gesteld. Maar ook hun suikerhuishouding raakte verstoord. Bloedglucose steeg, er kwam extra glucose in urine en ontlasting voor, terwijl verschillende organen lagere intracellulaire glucoseniveaus vertoonden. Beeldvorming met een radioactieve glucose-achtige tracer toonde dat deze muizen suiker uit de darm normaal absorbeerden, maar dat hun weefsels — en met name hun nieren — slecht waren in het terugwinnen van glucose uit de bloedbaan en uit gefilterde urine. Gezamenlijk wezen deze bevindingen op een defect in het inbrengen en hergebruiken van glucose in cellen, ondanks normale insulinewaarden en hormoonsignalen.
SPNS2 haalt brandstof binnen terwijl het signalen naar buiten duwt
Om te testen of SPNS2 zelf glucose verplaatst, manipuleerde het team de niveaus ervan in bloedvat- en andere celtypen. Toen ze SPNS2 verhoogden, gaven cellen meer S1P af aan het omringende medium en namen ze meer glucose op, waardoor ze meer energie produceerden en sterkere ademhaling en suikerverbranding vertoonden. Toen ze SPNS2 verwijderden of blokkeerden, bleef S1P binnenin de cellen en nam de glucose-opname af. Deze effecten bleven bestaan zelfs wanneer klassieke suikerdraagers (zoals GLUT1 en GLUT3) waren geremd, en ze waren niet afhankelijk van S1P-receptoren op het celoppervlak of van insuline. In zorgvuldig gecontroleerde kunstmatige „proteoliposomen” — kleine in het lab gemaakte belletjes met gezuiverde SPNS2 in hun membranen — kon het eiwit direct fluorescerende of radioactieve glucose naar binnen verplaatsen, maar alleen efficiënt wanneer S1P aan de binnenzijde aanwezig was. Dit toonde aan dat SPNS2 zelf kan functioneren als een glucose-importer die gekoppeld is aan S1P-export.
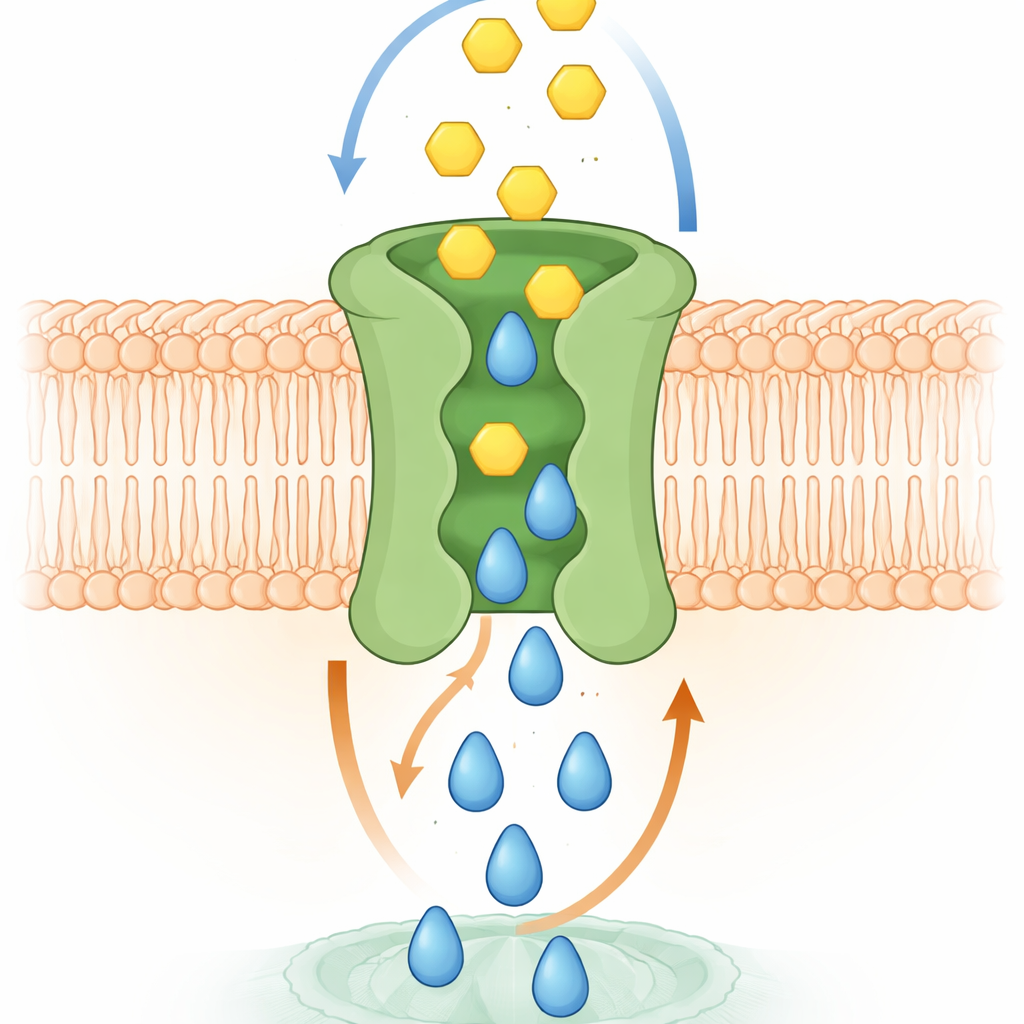
Hoe de moleculaire ruil waarschijnlijk werkt
Computersimulaties en structurele experimenten hielpen het mechanisme te verklaren. Hoogwaardige modellen van SPNS2 in een membraan lieten zien hoe S1P omhoog schuift door een centraal holte, subtiele vormveranderingen veroorzaakt die tijdelijke pockets voor glucose aan de buitenzijde openen. Terwijl S1P naar buiten beweegt, kan glucose zich in deze pockets nestelen en vervolgens naar beneden glijden door hetzelfde centrale pad naar het celinterieur. De onderzoekers identificeerden specifieke aminozuren die glucose in deze pockets aanraken. Wanneer deze residuen werden gemuteerd, daalde de glucosetoevoer en faalde het transport, ook al bereikten de gewijzigde eiwitten nog steeds het celoppervlak. In levende cellen verzwakte het verlies van deze gekoppelde transportfunctie S1P‑gedreven processen zoals celdeling, migratie om een wondachtige kloof te sluiten, en het vermogen van endotheliale cellagen om een dichte barrière te vormen — functies die zowel signaal als energie vereisen.
Waarom dit belangrijk is voor gezondheid en ziekte
Door te onthullen dat SPNS2 een tweerichtingspoort is — S1P naar buiten zendend terwijl het glucose naar binnen brengt — koppelt dit werk een krachtig signaalmolecuul aan de basale energievoorziening in één stap. Wanneer SPNS2 S1P loslaat om immuun- of vasculaire reacties te activeren, helpt het tegelijkertijd cellen extra brandstof binnen te halen om die acties mogelijk te maken. Verstoring van deze koppeling kan bijdragen aan hoge bloedsuiker, verlies van glucose via de nieren, en insuline-onafhankelijke vormen van verstoorde glucosehuishouding. Omdat SPNS2 en S1P-signaleringsroutes ook de uitzaaiing van kanker, ontsteking en de integriteit van bloedvaten beïnvloeden, zou het richten op deze „signaal-en-suiker” poortwachter nieuwe wegen kunnen openen voor de behandeling van metabole ziekten, auto-immuunziekten en tumoren die afhankelijk zijn van zowel verhoogde signalering als verhoogde glucose-opname.
Bronvermelding: Weigel, C., Hossen, M.L., Brown, R.D.R. et al. SPNS2 exports sphingosine-1-phosphate and imports glucose. Nat Commun 17, 3901 (2026). https://doi.org/10.1038/s41467-026-71659-7
Trefwoorden: glucosetransport, sphingosine-1-fosfaat, membraantransporter, endotheliale biologie, metabole signalering