Clear Sky Science · pl
SPNS2 eksportuje sfingozynę‑1‑fosforan i importuje glukozę
Ukryty strażnik cukru i sygnałów komórkowych
W organizmach nieustannie równoważy się tysiące sygnałów chemicznych, jednocześnie utrzymując poziom glukozy we krwi w bezpiecznym zakresie. Badanie to ujawnia nieoczekiwanego aktora, który pomaga robić obie rzeczy naraz: małe białko o nazwie SPNS2 osiadłe w błonach komórkowych. Autorzy wykazują, że SPNS2 nie tylko uwalnia sygnałowy lipid ważny dla odporności i naczyń krwionośnych, lecz jednocześnie pomaga wtłaczać glukozę — główne paliwo organizmu — do komórek. Ta podwójna rola łączy międzykomórkową komunikację z zaopatrzeniem energetycznym komórek i ma znaczenie dla cukrzycy, chorób serca oraz raka.
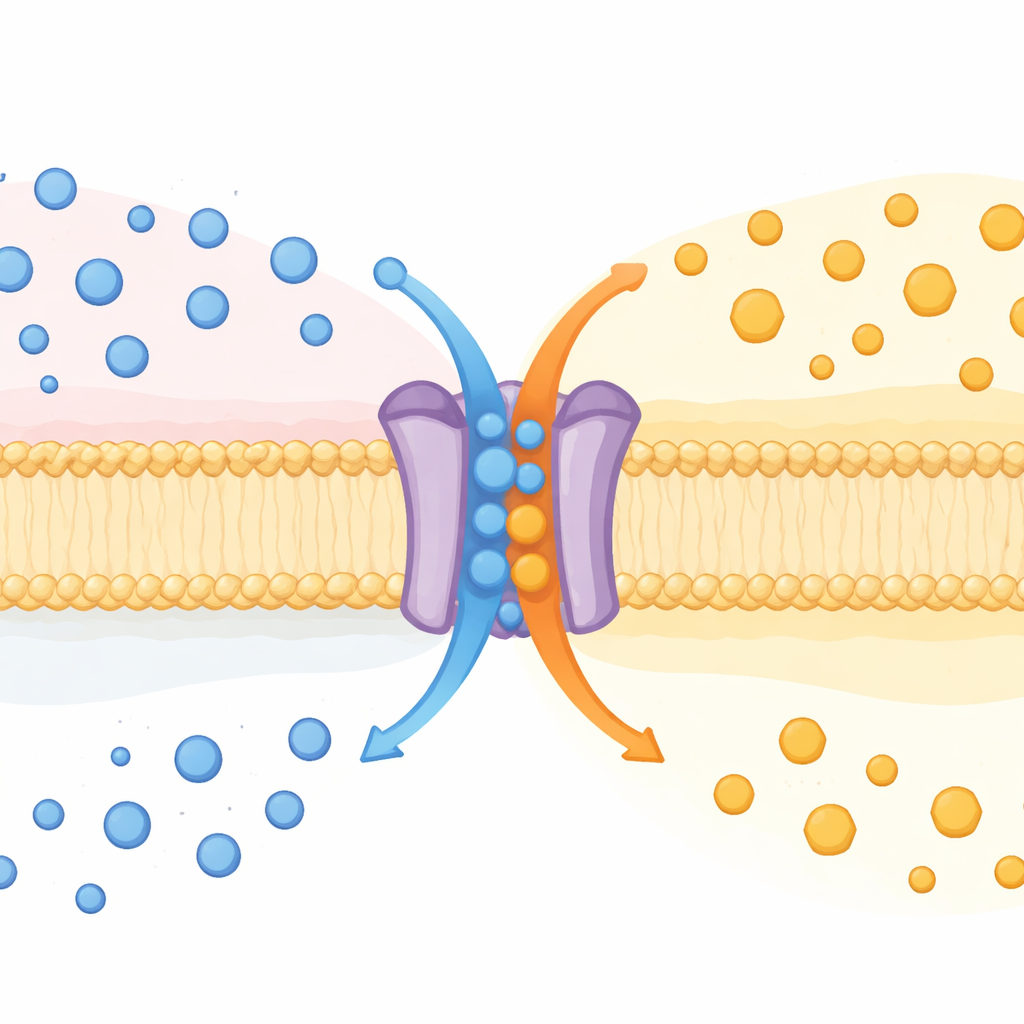
Jedno białko, dwie funkcje
SPNS2 od dawna było znane z transportu przekaźnika o nazwie sfingozyna‑1‑fosforan (S1P) na zewnątrz komórek. S1P krąży we krwi i limfie, kierując komórkami odpornościowymi, kształtując naczynia i wpływając na zapalenie. Do tej pory uważano SPNS2 za jednostronnego eksportera. Badania na myszach pozbawionych genu Spns2 oraz na licznych hodowlach komórkowych pokazały jednak, że SPNS2 zachowuje się raczej jak maszyna wymiany. Wysyła S1P na zewnątrz, a jednocześnie wciąga glukozę do wnętrza, podobnie do „antiportera” — klasy transporterów zamieniających jedną substancję na inną przez błonę.
Co się dzieje, gdy brakuje SPNS2
U myszy zaprojektowanych bez SPNS2 poziomy S1P we krwi i limfie spadły, podczas gdy S1P gromadził się w tkankach takich jak wątroba, nerka, płuca i serce — dokładnie to, czego można by oczekiwać po wyłączeniu eksportera. Jednak zaburzył się także bilans cukrowy. Poziom glukozy we krwi wzrósł, a dodatkowa glukoza pojawiła się w moczu i kale, podczas gdy w kilku narządach stwierdzono obniżone stężenia glukozy wewnątrzkomórkowej. Obrazowanie przy użyciu radioaktywnego znacznika podobnego do glukozy wykazało, że myszy te prawidłowo wchłaniały cukier z jelit, lecz ich tkanki — a w szczególności nerki — słabo odzyskiwały glukozę z krwi i z przesączu moczu. Razem te obserwacje wskazują na defekt w wnikaniu glukozy do komórek i jej ponownym wykorzystaniu, pomimo prawidłowych poziomów insuliny i sygnałów hormonalnych.
SPNS2 pobiera paliwo, wypychając sygnały
Aby sprawdzić, czy to samo SPNS2 przemieszcza glukozę, zespół manipulował jego poziomami w komórkach śródbłonka i innych typach komórek. Gdy zwiększano ilość SPNS2, komórki uwalniały więcej S1P do otaczającego płynu i jednocześnie pobierały więcej glukozy, wytwarzając większą ilość energii oraz wykazując silniejszą respirację i utlenianie cukru. Gdy SPNS2 usuwano lub blokowano, S1P pozostawał wewnątrz komórek, a pobór glukozy się zmniejszał. Efekty te utrzymywały się nawet po zahamowaniu klasycznych transporterów glukozy (jak GLUT1 i GLUT3) i nie zależały od receptorów S1P na powierzchni komórek ani od insuliny. W starannie kontrolowanych proteoliposomach — małych, laboratoryjnych pęcherzykach z oczyszczonym SPNS2 osadzonym w błonie — białko mogło bezpośrednio transportować fluorescencyjną lub radioaktywną glukozę do wnętrza, lecz efektywnie tylko wtedy, gdy S1P znajdował się po stronie wewnętrznej. Pokazało to, że SPNS2 może samodzielnie działać jako importer glukozy sprzężony z eksportem S1P.
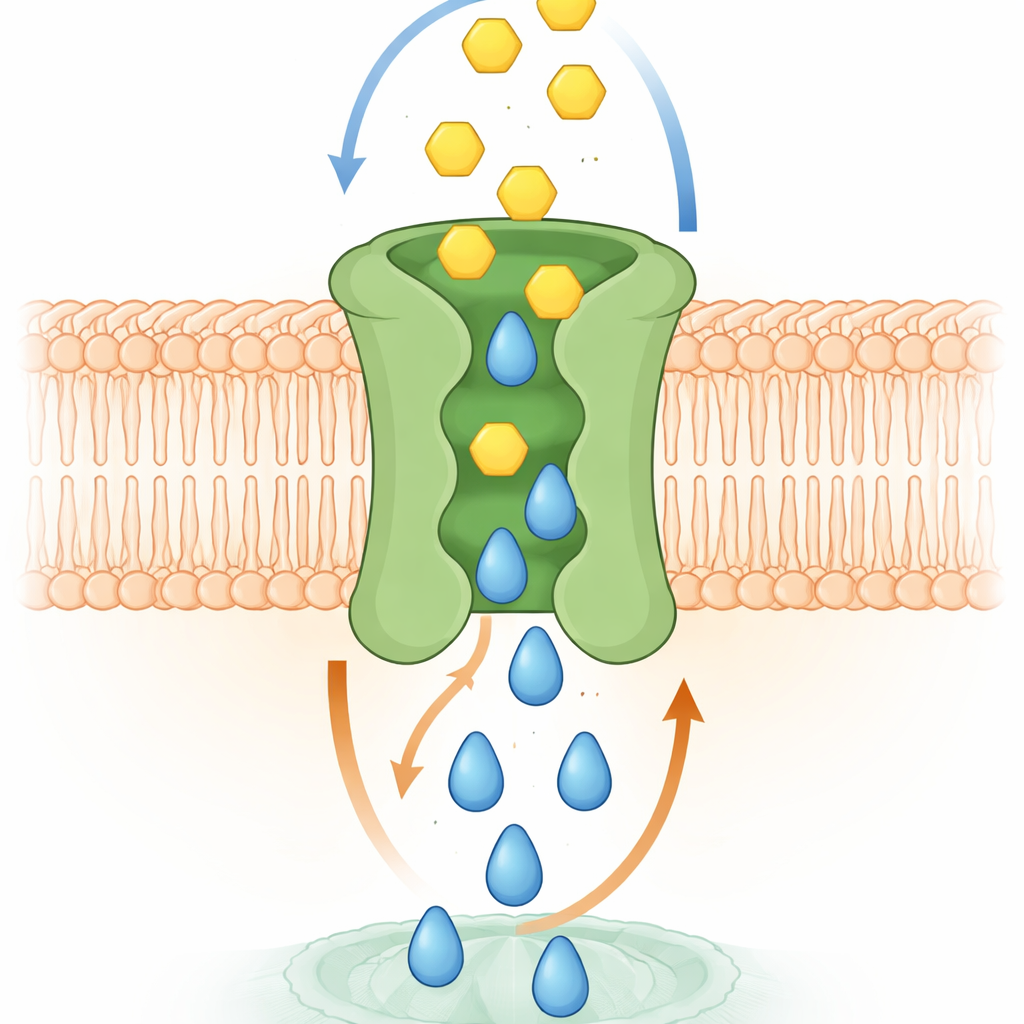
Jak prawdopodobnie działa ta molekularna zamiana
Symulacje komputerowe i eksperymenty strukturalne pomogły wyjaśnić mechanizm. Modele o wysokiej rozdzielczości SPNS2 w błonie pokazały, jak S1P przesuwa się w górę przez centralną jamę, wywołując subtelne zmiany kształtu, które otwierają tymczasowe kieszenie dla glukozy po stronie zewnętrznej. W miarę przesuwania się S1P na zewnątrz, glukoza może zająć miejsce w tych kieszeniach, a następnie przemieścić się w dół przez tę samą centralną ścieżkę w kierunku wnętrza komórki. Naukowcy zidentyfikowali konkretne aminokwasy kontaktujące glukozę w tych kieszeniach. Gdy te reszty były mutowane, wiązanie glukozy spadało, a transport zawodził, mimo że zmienione białka nadal trafiały na powierzchnię komórek. W żywych komórkach utrata tego sprzężonego transportu osłabiała procesy napędzane przez S1P, takie jak wzrost komórek, migracja potrzebna do zamknięcia przypominającej ranę szczeliny oraz zdolność warstw śródbłonka do tworzenia zwartej bariery — funkcje wymagające zarówno sygnału, jak i energii.
Dlaczego to ma znaczenie dla zdrowia i chorób
Ujawniając, że SPNS2 jest dwukierunkową bramą — wysyłającą S1P i jednocześnie wciągającą glukozę — praca ta łączy potężną cząsteczkę sygnałową z podstawowym zaopatrzeniem energetycznym w jednym kroku. Gdy SPNS2 uwalnia S1P, aby wywołać reakcje odpornościowe lub naczyniowe, równocześnie pomaga komórkom zaimportować dodatkowe paliwo potrzebne do napędzenia tych działań. Zakłócenia tego sprzężenia mogą przyczyniać się do hiperglikemii, utraty glukozy przez nerki i form dysregulacji glukozy niezależnych od insuliny. Ponieważ SPNS2 i sygnalizacja S1P wpływają także na rozprzestrzenianie raka, zapalenie i integralność naczyń, ukierunkowanie tej „bramy sygnał‑i‑cukier” może otworzyć nowe możliwości leczenia chorób metabolicznych, autoimmunologicznych oraz nowotworów, które polegają zarówno na nasilonej sygnalizacji, jak i zwiększonym poborze glukozy.
Cytowanie: Weigel, C., Hossen, M.L., Brown, R.D.R. et al. SPNS2 exports sphingosine-1-phosphate and imports glucose. Nat Commun 17, 3901 (2026). https://doi.org/10.1038/s41467-026-71659-7
Słowa kluczowe: transport glukozy, sfingozyna‑1‑fosforan, transporter błonowy, biologia śródbłonka, sygnalizacja metaboliczna