Clear Sky Science · he
SPNS2 מייצא ספינגוזין‑1‑פוספט ומייבא גלוקוז
שומר סף נסתר לסוכר ולסיגנלים תאיים
גופנו מנהל ללא הרף אלפי סיגנלים כימיים תוך שמירה על רמות סוכר בדם בטווח בטוח. המחקר הזה חושף שחקן בלתי צפוי שעוזר לשתי המשימות במקביל: חלבון זעיר בשם SPNS2 היושב בממברנות התאים. החוקרים מראים ש‑SPNS2 לא רק משחרר מולקולת שומן סיגנלית החשובה למערכת החיסון ולכלי הדם, אלא גם מסייע למשוך גלוקוז — הדלק העיקרי של הגוף — לתוך התאים. תפקיד כפול זה מקשר בין האופן שבו תאים מתקשרים זה עם זה לבין האופן שבו הם מתזוננים, עם השלכות לסכרת, מחלות לב וסרטן.
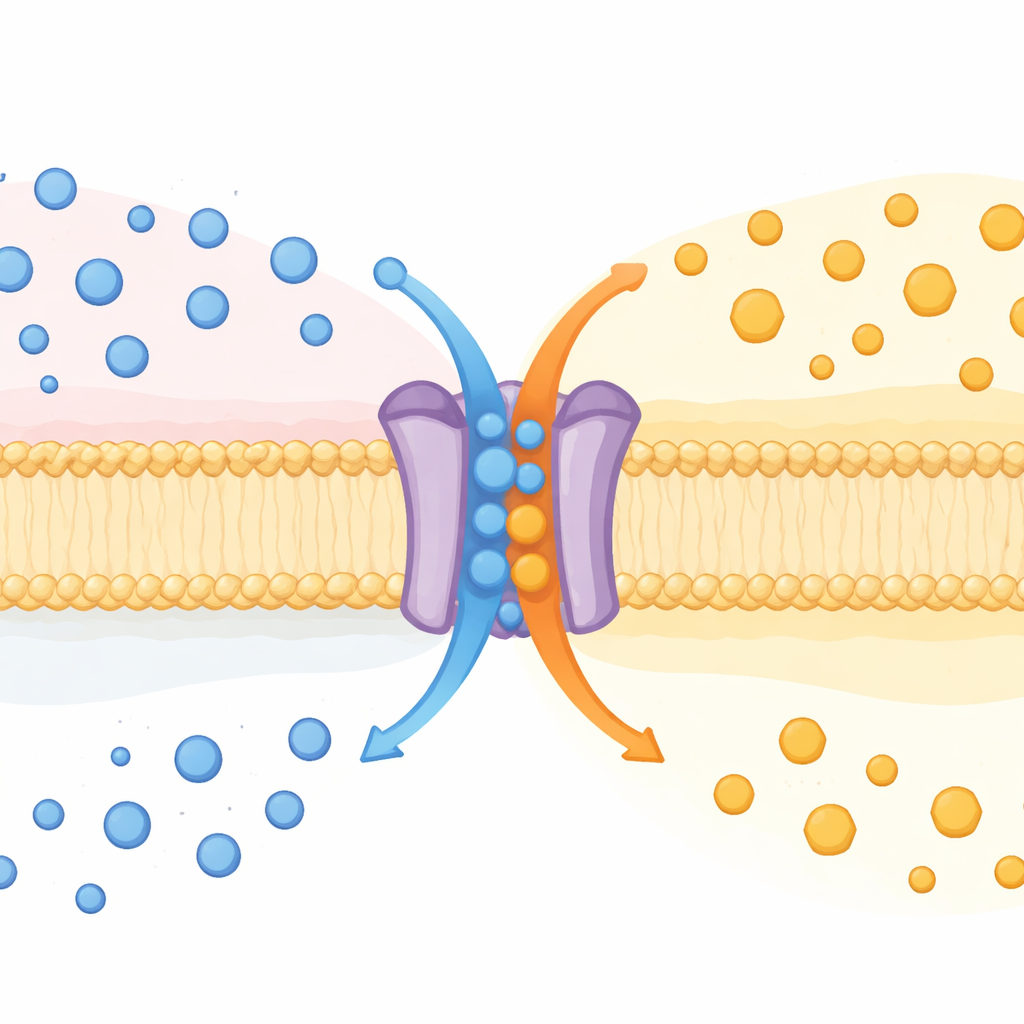
חלבון אחד, שתי משימות
SPNS2 היה ידוע מזה זמן כמוציא מולקולת שליח הנקראת ספינגוזין‑1‑פוספט (S1P) מתוך תאים. S1P נסובב בדם ובלימפה, מנחה תאים חיסוניים, מעצב כלי דם ומשפיע על דלקת. עד כה חשבו על SPNS2 כאקספורטר חד‑כיווני. באמצעות חקירה של עכברים חסרי הגן Spns2 ובסוגים רבים של תאים בתרבית, הראו המחברים ש‑SPNS2 למעשה מתנהג יותר כמו מכונת החלפה. הוא שולח S1P החוצה ובו‑זמנית מייבא גלוקוז, בדומה ל"אנטיפורטר" — משפחה של נשאים המחליפים חומר אחד בחומר אחר מעבר לממברנה.
מה קורה כש‑SPNS2 חסר
בעכברים שתוכנתו להחסר את SPNS2, רמות ה‑S1P בדם ובלימפה ירדו, בעוד ש‑S1P הצטבר ברקמות כמו כבד, כליה, ריאה ולב — בדיוק כפי שצפוי אם מייצא הושבת. אך מאזן הסוכר שלהם נפרע גם הוא. רמת הגלוקוז בדם עלתה, גלוקוז עודף הופיע בשתן ובצואה, ובמספר איברים נרשמו רמות פנימיות נמוכות יותר של גלוקוז. הדמיה עם מעקב אחרי חומר דמוי גלוקוז רדיואקטיבי גילתה שהעכברים אלו ספגו סוכר מהמעי כרגיל, אך רקמותיהם — ובמיוחד הכליות — היו חלשות בשימור גלוקוז מהמחזור הדם ומהשתן המסונן. יחד, ממצאים אלה הצביעו על פגם בכניסת גלוקוז לתאים ובמיחזורו, למרות רמות אינסולין ואותות הורמונליים נורמליים.
SPNS2 מושך דלק כשהוא דוחף סיגנלים החוצה
כדי לבדוק האם SPNS2 עצמו מעביר גלוקוז, הצוות שינה את רמותיו בתאים של כלי דם וסוגי תאים אחרים. כשהגבירו את SPNS2, תאים שחררו יותר S1P לנוזל שבו הם נמצאים ולקחו יותר גלוקוז, הפיקו יותר אנרגיה והראו נשימה ושריפת סוכר חזקה יותר. כשהמחקו או חסמו את SPNS2, התאים שמרו את ה‑S1P בפנים ולקחו פחות גלוקוז. השפעות אלה נשמרו גם כאשר נשאים קלאסיים של סוכר (כמו GLUT1 ו‑GLUT3) הועברו לחסימה, והן לא תלויות בקולטנים ל‑S1P על פני התא או באינסולין. ב"פרוטאוליפוזומים" מבוקרים בקפדנות — בועיות מעבדה מלאכותיות עם SPNS2 טהור בממברנה — החלבון יכול היה להעביר גלוקוז זוהר או רדיואקטיבי פנימה ישירות, אך ביעילות רק כאשר S1P היה נוכח בצד הפנימי. ממצא זה הראה כי SPNS2 עצמו יכול לפעול כנשא גלוקוז מקושר לייצוא S1P.
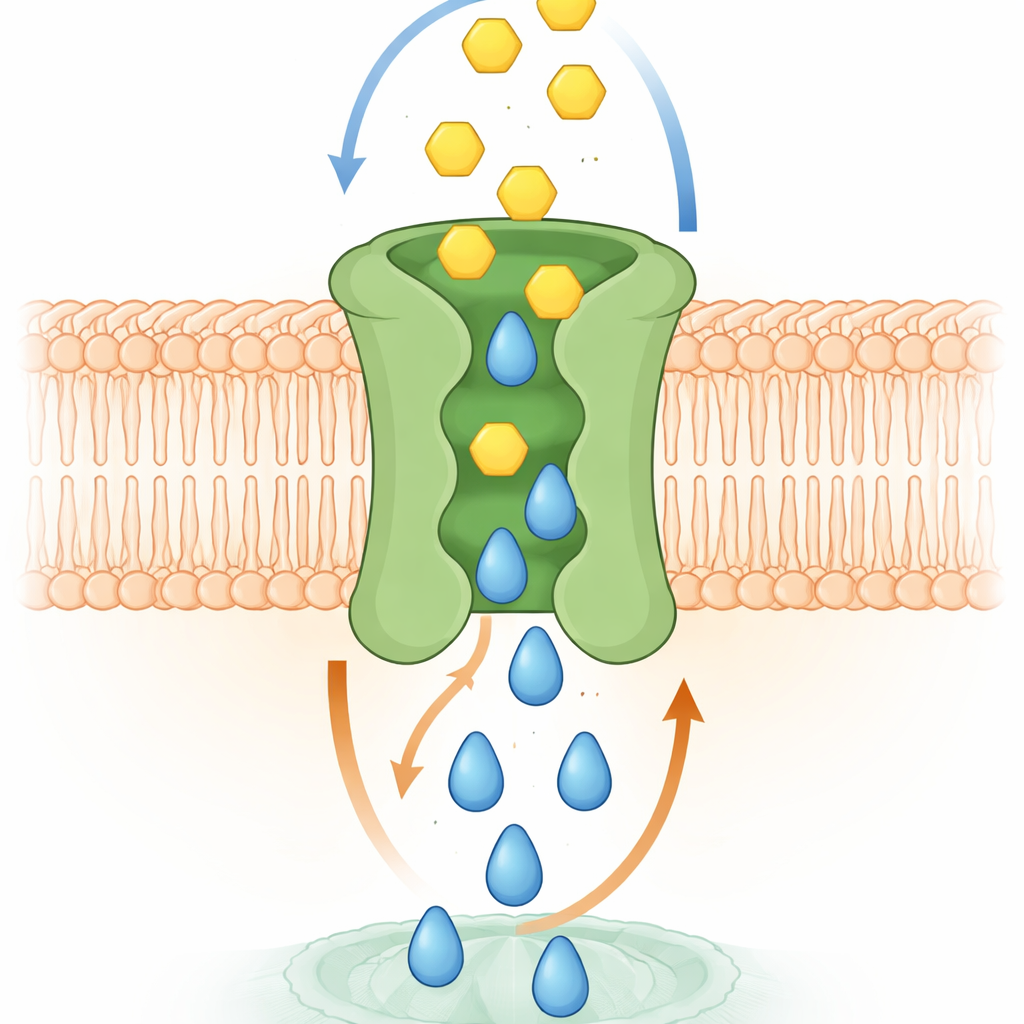
כיצד החלפת המולקולות עובדת ככל הנראה
סימולציות מחשב וניסויים מבניים עזרו להסביר את המנגנון. מודלים ברזולוציה גבוהה של SPNS2 בממברנה הראו את S1P מחליק כלפי מעלה דרך חלל מרכזי, ומעורר שינויים צורניים עדינים שפותחים כיסים זמניים לגלוקוז בצד החיצוני. ככל ש‑S1P נע כלפי החוץ, גלוקוז יכול לעגן בכיסים אלה ואז להחליק דרך אותו מסלול מרכזי כלפי פנים התא. החוקרים זיהו חומצות אמינו ספציפיות שנמצאות במגע עם הגלוקוז בכיסים אלה. כאשר שינו חומצות אלה במוטציות, קשירת הגלוקוז ירדה וההעברה נכשלה, אף על פי שהחלבונים המושרים עדיין הגיעו לפני השטח של התא. בתאים חיים, אובדן ההובלה המקושרת הזו החליש תהליכים מונעי S1P כגון צמיחת תאים, תנועה לסגירת פער דמוי פצע, ויכולת שכבות תאי אנדותל ליצור מחסום הדוק — פונקציות שדורשות גם אות וגם אנרגיה.
מדוע זה חשוב לבריאות ומחלה
על ידי חשיפת העובדה ש‑SPNS2 הוא שער דו‑כיווני — שולח S1P החוצה ובו‑זמנית מביא גלוקוז פנימה — עבודה זו מקשרת מולקולת סיגנל חזקה לאספקת אנרגיה בסיסית בשלב אחד. כאשר SPNS2 משחרר S1P כדי לעורר תגובות חיסוניות או וסקולריות, הוא באותו רגע עוזר לתאים לייבא דלק נוסף כדי להניע את הפעולות האלה. שיבושים בקישוריות הזו עשויים לתרום ליתר סוכר בדם, לאובדן גלוקוז בכליות ולצורות בלתי תלויות באינסולין של חוסר ויסות גלוקוז. מאחר ש‑SPNS2 וסיגנלינג של S1P גם מעצבים התפשטות סרטן, דלקת ושלמות כלי הדם, פגיעה או מיקוד ב"שומר הסף של סיגנל‑וסוכר" הזה עשויים לפתוח דרכים חדשות לטיפול במחלות מטבוליות, מצבים אוטואימוניים וגידולים שתלויים הן בסיגנלים מוגברים והן בספיגת גלוקוז מוגברת.
ציטוט: Weigel, C., Hossen, M.L., Brown, R.D.R. et al. SPNS2 exports sphingosine-1-phosphate and imports glucose. Nat Commun 17, 3901 (2026). https://doi.org/10.1038/s41467-026-71659-7
מילות מפתח: הובלת גלוקוז, ספינגוזין‑1‑פוספט, מוביל ממברנלי, ביולוגיה אנדותלית, סיגנלינג מטבולי