Clear Sky Science · tr
SPNS2 sfingozin‑1‑fosfatı dışarı çıkarır ve glukozu içeri alır
Şeker ve Hücresel Sinyaller için Gizli Bir Kapı Bekçisi
Vücudumuz binlerce kimyasal sinyali sürekli olarak dengelerken aynı zamanda kan şekerini güvenli bir aralıkta tutar. Bu çalışma her iki işlemi de aynı anda yapmaya yardım eden beklenmedik bir oyuncuyu ortaya koyuyor: hücre zarlarında yer alan küçük bir protein olan SPNS2. Araştırmacılar, SPNS2’nin yalnızca bağışıklık ve kan damarları için önemli olan bir yağ sinyal molekülünü serbest bırakmakla kalmayıp aynı zamanda vücudun birincil yakıtı olan glukozu hücrelerin içine çekmeye de yardımcı olduğunu gösteriyor. Bu ikili rol, hücrelerin birbirleriyle nasıl iletişim kurduğunu ve nasıl beslendiğini birbirine bağlıyor; tip 2 diyabet, kalp hastalıkları ve kanser için çıkarımları olabilir.
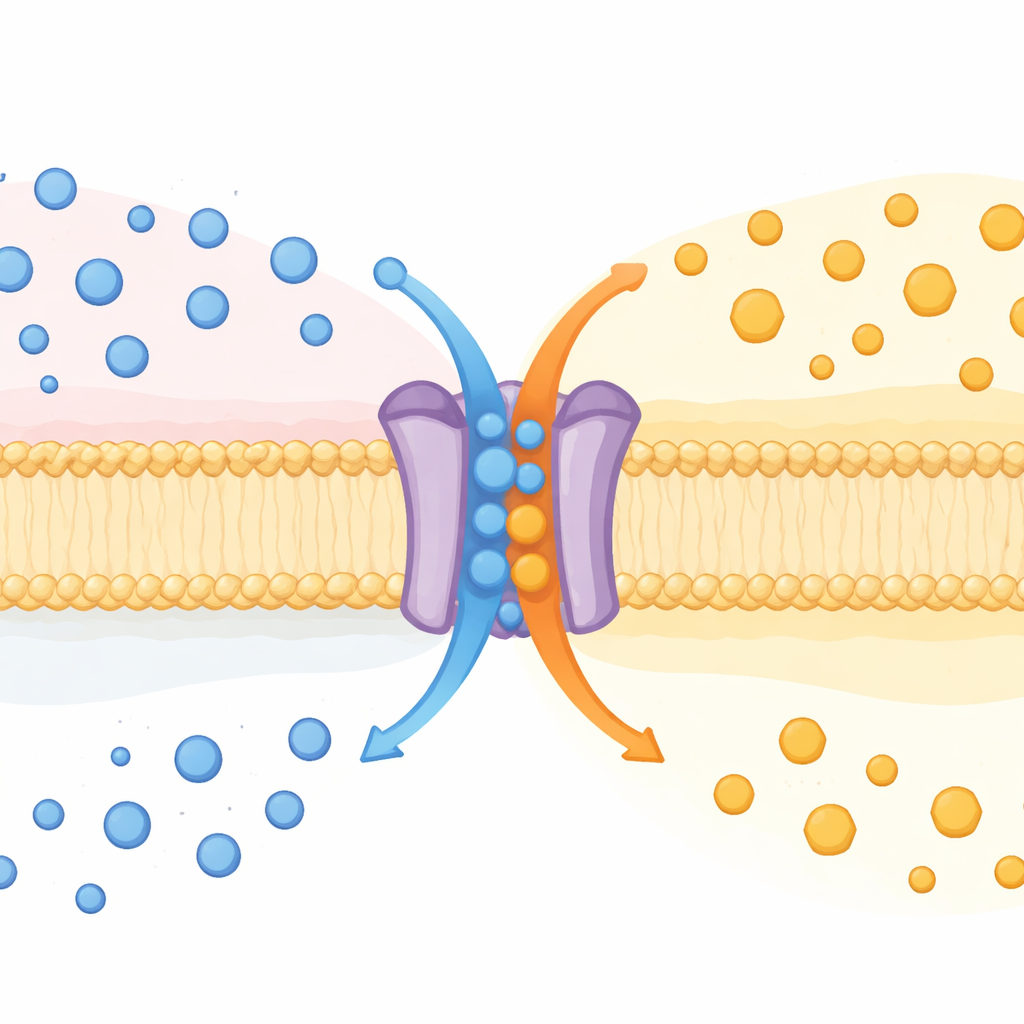
Tek Protein, İki Görev
SPNS2 uzun süredir sfingozin‑1‑fosfat (S1P) adlı haberci molekülü hücre dışına taşımakla biliniyordu. S1P kan ve lenf içinde dolaşır, bağışıklık hücrelerini yönlendirir, kan damarlarını şekillendirir ve iltihabı etkiler. Bugüne kadar SPNS2 tek yönlü bir ihracatçı olarak değerlendirilmişti. Spns2 geninden yoksun fareleri ve çeşitli kültür hücrelerini inceleyerek yazarlar, SPNS2’nin aslında daha çok bir değişim makinesi gibi davrandığını keşfettiler. S1P’yi dışarı gönderirken glukozu içeri alıyor; bu, maddeleri zar boyunca birbirleriyle takas eden “antiporter” sınıfı taşıyıcılara benzer bir davranıştır.
SPNS2 Eksik Olunca Ne Oluyor
SPNS2’den yoksun olacak şekilde genetik olarak değiştirilmiş farelerde kan ve lenfdeki S1P düzeyleri düştü, oysa karaciğer, böbrek, akciğer ve kalp gibi dokularda S1P birikti—bir ihracatçı etkisiz hale gelmişse bekleyeceğiniz şey tam da bu. Ancak şeker dengeleri de bozuldu. Kan glukozu yükseldi ve idrar ile dışkıda ekstra glukoz görüldü; birkaç organda içsel glukoz seviyeleri azaldı. Radyoaktif glukoza benzer bir işaretleyici ile yapılan görüntüleme, bu farelerin bağırsaktan şekeri normal şekilde emdiğini ancak dokularının—özellikle böbreklerinin—kan dolaşımından ve süzülmüş idrardan glukozu geri alamada zayıf olduğunu ortaya koydu. Bu bulgular, normal insülin seviyeleri ve hormon sinyallerine rağmen glukoza hücre içine alma ve yeniden kullanma konusunda bir kusur olduğunu gösteriyordu.
SPNS2 Sinyalleri Dışarı İtirken Yakıtı İçeri Çeker
SPNS2’nin gerçekten glukoz taşıyıp taşımadığını test etmek için ekip, kan damarı ve diğer hücre tiplerinde miktarını değiştirdi. SPNS2’yi artırdıklarında hücreler çevre sıvısına daha fazla S1P salgıladı ve daha fazla glukoz aldı; daha fazla enerji ürettiler ve oksidasyon ile şeker yakımında artış gösterdiler. SPNS2’yi sildiklerinde veya bloke ettiklerinde hücreler S1P’yi içeride tuttu ve daha az glukoz aldı. Bu etkiler klasik şeker taşıyıcıları (GLUT1 ve GLUT3 gibi) engellendiğinde bile sürdü ve hücre yüzeyindeki S1P reseptörlerine veya insüline bağlı değildi. Saflaştırılmış SPNS2’nin zarlarına yerleştirildiği dikkatle kontrol edilmiş yapay “proteoliposomlar”da—laboratuvarda yapılmış küçük kabarcıklarda—protein, floresanlı veya radyoaktif glukozu içeri doğru doğrudan taşıyabiliyordu; ancak bu verimliydi yalnızca iç tarafta S1P bulunduğunda. Bu, SPNS2’nin S1P ihracatına bağlı bir glukoz ithalatçısı olarak doğrudan hareket edebileceğini gösterdi.
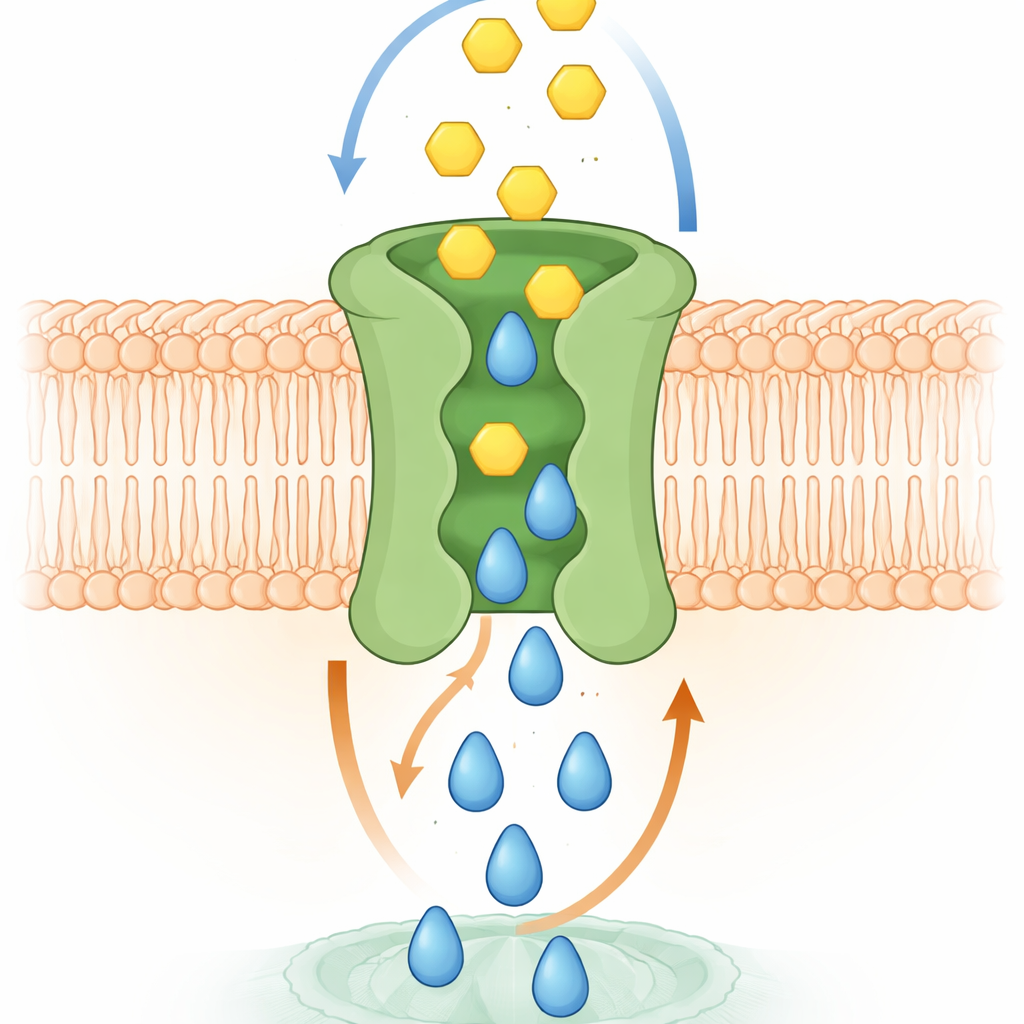
Moleküler Takas Muhtemelen Nasıl İşliyor
Bilgisayar simülasyonları ve yapısal deneyler mekanizmayı açıklamaya yardımcı oldu. Bir zar içinde SPNS2’nin yüksek çözünürlüklü modelleri, S1P’nin merkezi bir boşluktan yukarı doğru kaydığını gösterdi; bu da dış tarafta glukoz için geçici cepler açan ince şekil değişikliklerini tetikledi. S1P dışarı doğru hareket ederken glukoz bu ceplere yerleşebilir ve ardından aynı merkezi yol boyunca hücre içi tarafa doğru kayabilir. Araştırmacılar bu ceplerde glukozla temas eden belirli amino asitleri belirledi. Bu kalıntılar değiştirildiğinde glukoz bağlanması azaldı ve taşıma başarısız oldu; oysa değişmiş proteinler hâlâ hücre yüzeyine ulaşabiliyordu. Canlı hücrelerde bu eşleşmiş taşımanın kaybı, hücre büyümesi, yara benzeri bir boşluğu kapatmak için hareket etme ve endotel hücre katmanlarının sıkı bir bariyer oluşturma yeteneği gibi S1P kaynaklı süreçleri zayıflattı—bu işlevlerin her ikisi de hem sinyal hem de enerji gerektirir.
Sağlık ve Hastalık Açısından Neden Önemli
SPNS2’nin S1P’yi dışarı gönderirken glukozu içeri alan iki yönlü bir kapı olduğunu ortaya koyarak bu çalışma, güçlü bir sinyal molekülünü temel enerji kaynağıyla tek bir adımda ilişkilendiriyor. SPNS2 S1P’yi saldığında bağışıklık veya damar tepkilerini tetiklerken eş zamanlı olarak hücrelerin bu eylemleri gerçekleştirmek için ek yakıt almasına yardımcı oluyor. Bu eşleşmenin bozulması yüksek kan şekeri, böbrek yoluyla şeker kaybı ve insüline bağlı olmayan düzensiz glukoz yönetimi formlarına katkıda bulunabilir. SPNS2 ve S1P sinyallemesi ayrıca kanser yayılımı, iltihaplanma ve damar bütünlüğünü şekillendirdiğinden, bu “sinyal ve şeker” kapı bekçisini hedeflemek metabolik hastalıklar, otoimmün durumlar ve hem artmış sinyalizasyon hem de artmış glukoz alımına dayanan tümörler için yeni tedavi yolları açabilir.
Atıf: Weigel, C., Hossen, M.L., Brown, R.D.R. et al. SPNS2 exports sphingosine-1-phosphate and imports glucose. Nat Commun 17, 3901 (2026). https://doi.org/10.1038/s41467-026-71659-7
Anahtar kelimeler: glukoz taşınımı, sfingozin‑1‑fosfat, zar taşıyıcısı, endotelyal biyoloji, metabolik sinyalizasyon