Clear Sky Science · de
SPNS2 exportiert Sphingosin‑1‑phosphat und importiert Glukose
Ein verborgener Torwächter für Zucker und Zell‑Signale
Unser Körper jongliert ständig mit Tausenden chemischer Signale und hält zugleich den Blutzucker in einem sicheren Bereich. Diese Studie deckt einen unerwarteten Akteur auf, der beides zugleich unterstützt: ein kleines Protein namens SPNS2, das in Zellmembranen sitzt. Die Forschenden zeigen, dass SPNS2 nicht nur ein Signallipid freisetzt, das für Immunfunktionen und Gefäßsystem wichtig ist, sondern gleichzeitig Glukose — den wichtigsten Brennstoff des Körpers — in die Zelle hineinbefördert. Diese Doppelrolle verbindet die zelluläre Kommunikation mit der Versorgung der Zelle und hat Implikationen für Diabetes, Herzkrankheiten und Krebs.
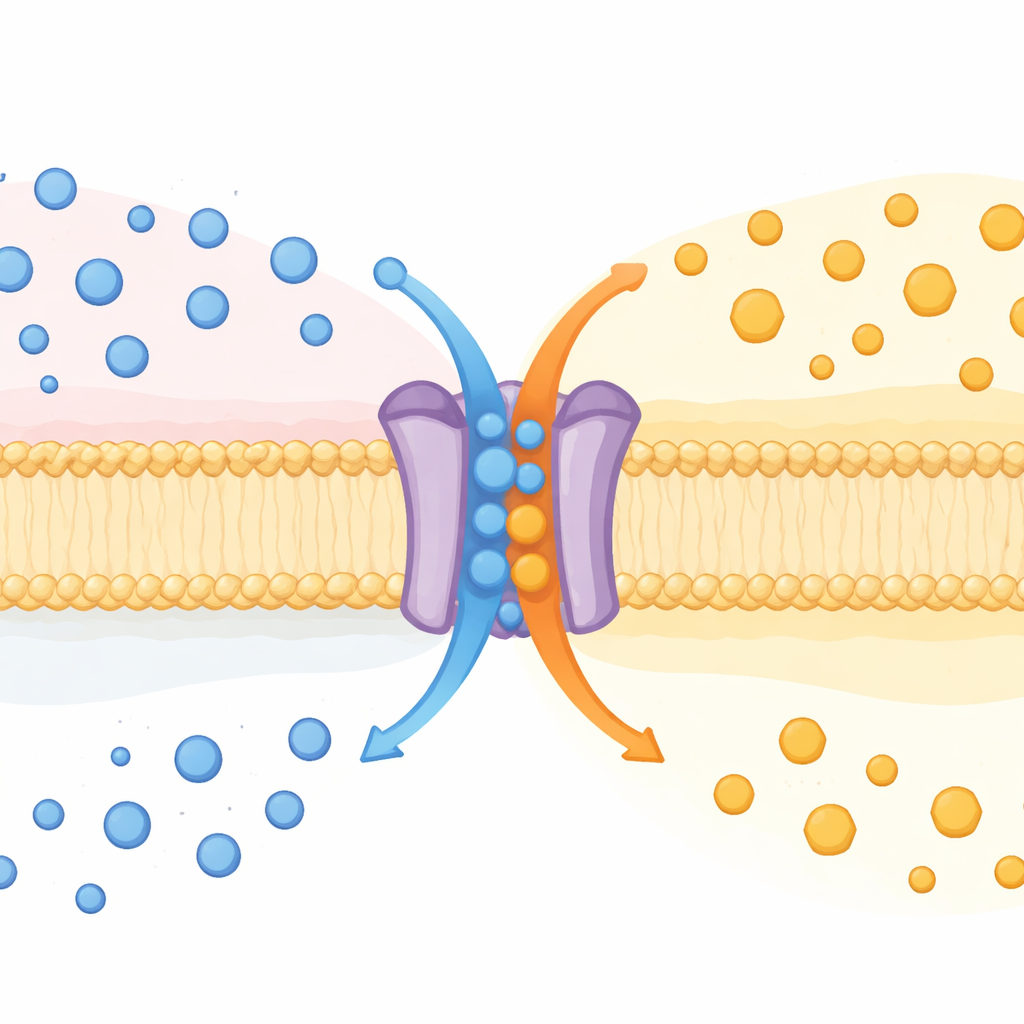
Ein Protein, zwei Aufgaben
SPNS2 ist seit Langem dafür bekannt, ein Botenmolekül namens Sphingosin‑1‑phosphat (S1P) aus Zellen zu transportieren. S1P zirkuliert im Blut und in der Lymphe, lenkt Immunzellen, formt Blutgefäße und beeinflusst Entzündungsprozesse. Bislang galt SPNS2 als ein‑seitiger Exporter. Durch Untersuchungen an Mäusen ohne das Spns2‑Gen sowie an zahlreichen kultivierten Zelltypen entdeckten die Autorinnen und Autoren, dass SPNS2 eher wie eine Tauschmaschine funktioniert. Es schickt S1P nach außen und bringt gleichzeitig Glukose hinein, ähnlich einem „Antiporter“, einer Klasse von Transportern, die eine Substanz gegen eine andere über Membranen austauschen.
Was passiert, wenn SPNS2 fehlt
In genetisch veränderten Mäusen ohne SPNS2 sanken die S1P‑Werte im Blut und in der Lymphe, während sich S1P in Geweben wie Leber, Niere, Lunge und Herz ansammelte — genau das, was man erwarten würde, wenn ein Exporter ausfällt. Doch auch das Zucker‑Gleichgewicht war gestört. Der Blutzucker stieg, zusätzliches Glukose erschien im Urin und Stuhl, und mehrere Organe zeigten niedrigere interne Glukosespiegel. Bildgebung mit einem radioaktiven, glukoseähnlichen Tracer zeigte, dass diese Mäuse Zucker aus dem Darm normal aufnahmen, ihre Gewebe — insbesondere die Nieren — aber schlecht darin waren, Glukose aus dem Blut und aus dem gefilterten Urin zurückzugewinnen. Zusammengenommen deuteten diese Befunde auf einen Defekt beim Eindringen von Glukose in Zellen und bei deren Wiederverwendung hin, trotz normaler Insulinspiegel und Hormonsignale.
SPNS2 zieht Brennstoff hinein, während es Signale hinausschiebt
Um zu prüfen, ob SPNS2 selbst Glukose transportiert, veränderte das Team dessen Menge in Blutgefäß‑ und anderen Zelltypen. Als sie SPNS2 erhöhten, setzten die Zellen mehr S1P in die Umgebung frei und nahmen mehr Glukose auf, produzierten mehr Energie und zeigten stärkere Atmung und Zuckerverbrennung. Bei Löschung oder Blockade von SPNS2 behielten die Zellen S1P ein und nahmen weniger Glukose auf. Diese Effekte blieben bestehen, selbst wenn klassische Zuckertransporter (wie GLUT1 und GLUT3) gehemmt wurden, und sie hingen weder von S1P‑Rezeptoren an der Zelloberfläche noch von Insulin ab. In sorgfältig kontrollierten künstlichen „Proteoliposomen“ — winzigen Laborblasen mit gereinigtem SPNS2 in ihrer Membran — konnte das Protein fluoreszenz- oder radioaktiv markierte Glukose direkt nach innen bewegen, aber nur effizient, wenn S1P auf der inneren Seite vorhanden war. Das zeigte, dass SPNS2 selbst als Glukoseimporter fungieren kann, gekoppelt an den S1P‑Export.
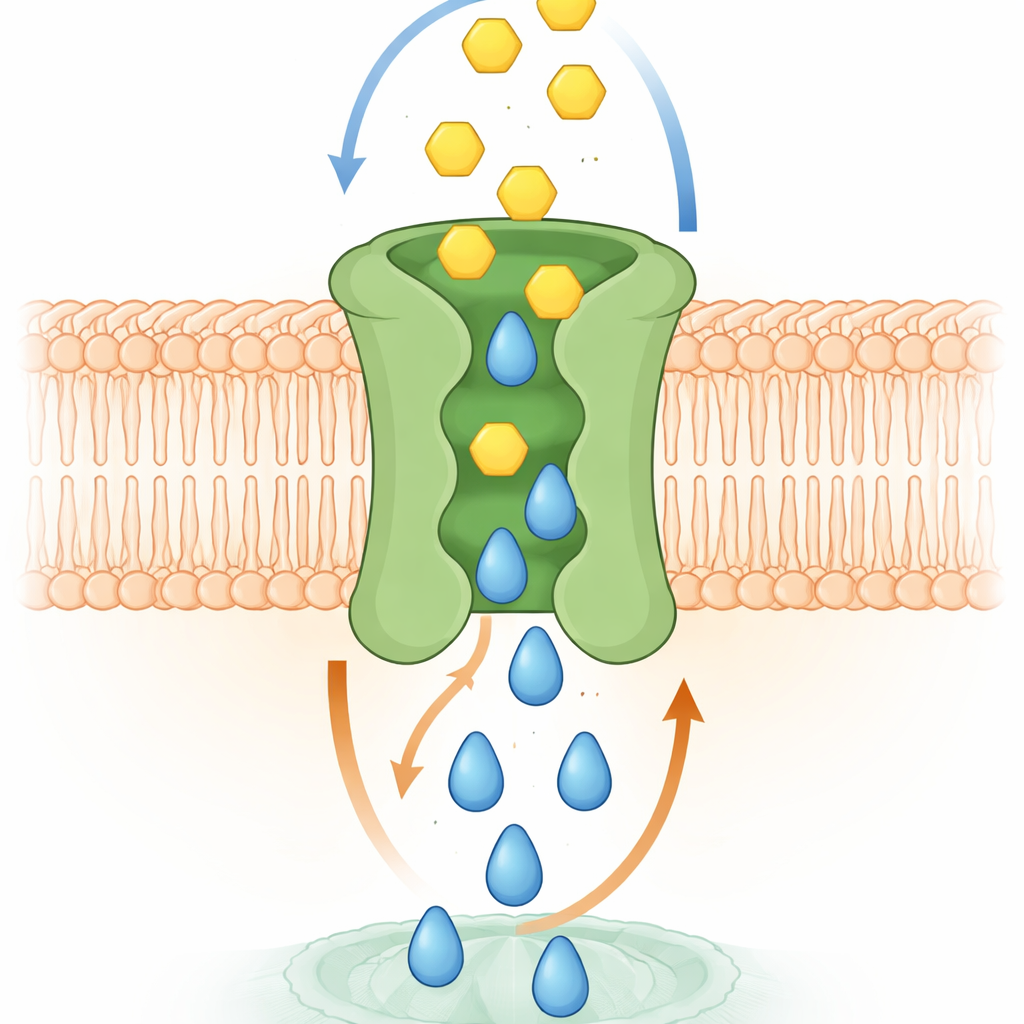
Wie der molekulare Tausch wahrscheinlich funktioniert
Computersimulationen und strukturelle Experimente halfen, den Mechanismus zu erklären. Hochaufgelöste Modelle von SPNS2 in einer Membran zeigten, wie S1P durch eine zentrale Höhlung nach oben gleitet und dabei subtile Formänderungen auslöst, die temporäre Taschen für Glukose an der Außenseite öffnen. Während S1P nach außen gelangt, kann Glukose in diesen Taschen andocken und dann durch denselben zentralen Weg in Richtung Zellinneres rutschen. Die Forschenden identifizierten spezifische Aminosäuren, die in diesen Taschen Kontakt mit Glukose aufnehmen. Wenn diese Reste mutiert wurden, nahm die Glukosebindung ab und der Transport schlug fehl, obwohl die veränderten Proteine noch die Zelloberfläche erreichten. In lebenden Zellen schwächte der Verlust dieses gekoppelten Transports S1P‑abhängige Prozesse wie Zellwachstum, die Bewegung zur Schließung einer wundenähnlichen Lücke und die Fähigkeit von Endothelzellschichten, eine dichte Barriere zu bilden — Funktionen, die sowohl Signalgebung als auch Energie erfordern.
Warum das für Gesundheit und Krankheit wichtig ist
Indem gezeigt wird, dass SPNS2 ein zweiseitiges Tor ist — das S1P aussendet, während es Glukose aufnimmt — verknüpft diese Arbeit ein mächtiges Signalmolekül unmittelbar mit der grundlegenden Energieversorgung. Wenn SPNS2 S1P freisetzt, um Immun‑ oder Gefäßreaktionen auszulösen, hilft es gleichzeitig den Zellen, zusätzlichen Brennstoff aufzunehmen, um diese Aktionen zu ermöglichen. Störungen in dieser Kopplung könnten zu erhöhtem Blutzucker, Zuckerverlust über die Niere und insulinunabhängigen Formen gestörter Glukoseregulierung beitragen. Da SPNS2 und die S1P‑Signalgebung auch die Ausbreitung von Krebs, Entzündungen und die Integrität von Blutgefäßen beeinflussen, könnte die gezielte Beeinflussung dieses „Signal‑und‑Zucker“‑Torwächters neue Wege zur Behandlung metabolischer Erkrankungen, Autoimmunerkrankungen und Tumoren eröffnen, die sowohl verstärkte Signalgebung als auch erhöhte Glukoseaufnahme nutzen.
Zitation: Weigel, C., Hossen, M.L., Brown, R.D.R. et al. SPNS2 exports sphingosine-1-phosphate and imports glucose. Nat Commun 17, 3901 (2026). https://doi.org/10.1038/s41467-026-71659-7
Schlüsselwörter: Glukosetransport, Sphingosin‑1‑phosphat, Membrantransporter, Endotheliale Biologie, Metabolische Signalübertragung