Clear Sky Science · it
SPNS2 esporta sfingosina-1-fosfato e importa glucosio
Un guardiano nascosto per zuccheri e segnali cellulari
I nostri corpi gestiscono costantemente migliaia di segnali chimici mantenendo al contempo la glicemia in un intervallo sicuro. Questo studio rivela un attore inaspettato che aiuta a fare entrambe le cose contemporaneamente: una piccola proteina chiamata SPNS2 che si trova nelle membrane cellulari. I ricercatori mostrano che SPNS2 non solo rilascia una molecola lipidica segnalatrice importante per l’immunità e i vasi sanguigni, ma allo stesso tempo facilita l’ingresso del glucosio — il principale combustibile del corpo — nelle cellule. Questo ruolo doppio collega il modo in cui le cellule comunicano tra loro con il modo in cui si alimentano, con implicazioni per diabete, malattie cardiache e cancro.
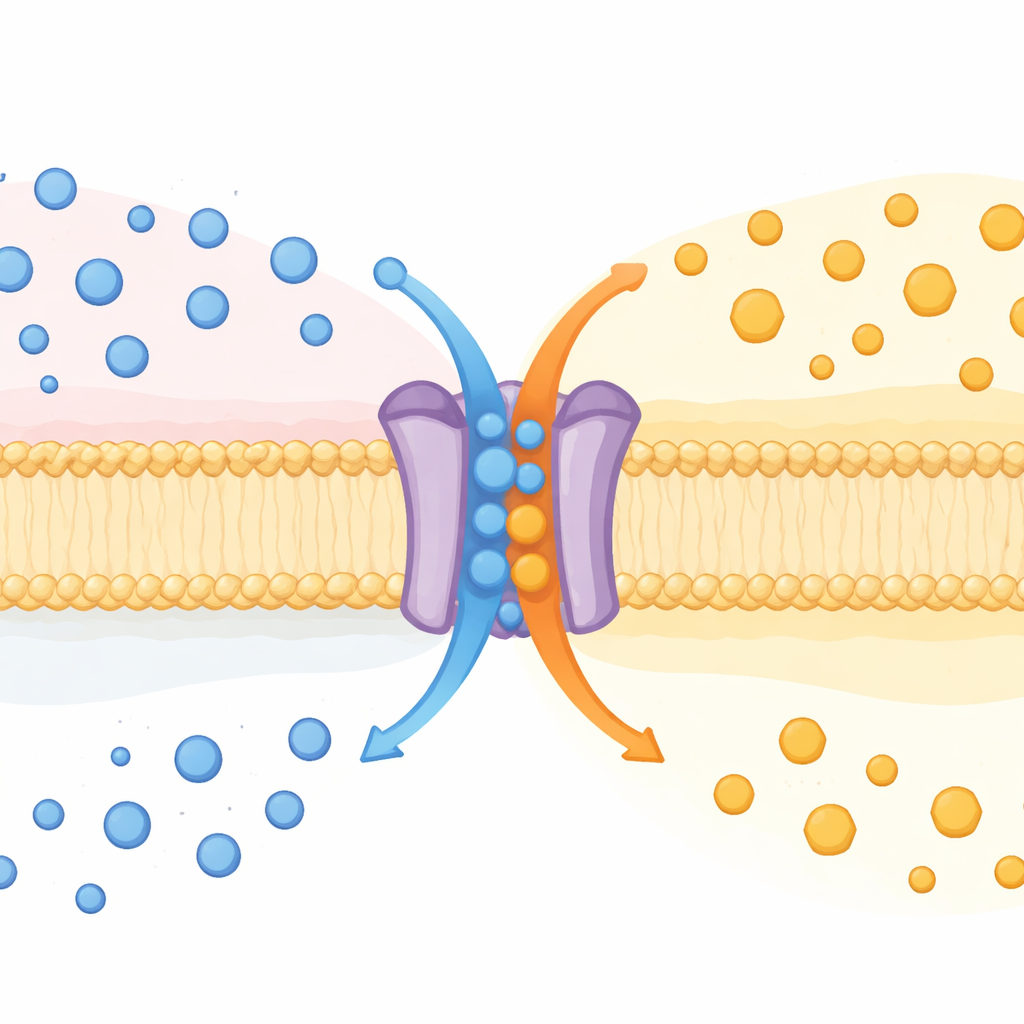
Una proteina, due compiti
SPNS2 è nota da tempo per trasportare una molecola messaggera chiamata sfingosina‑1‑fosfato (S1P) fuori dalle cellule. L’S1P circola nel sangue e nella linfa, indirizzando le cellule immunitarie, modellando i vasi sanguigni e influenzando l’infiammazione. Fino ad ora SPNS2 era considerata un esportatore unidirezionale. Studiando topi privi del gene Spns2, insieme a diversi tipi di cellule coltivate, gli autori hanno scoperto che SPNS2 si comporta in realtà più come una macchina di scambio. Espelle S1P mentre contemporaneamente introduce glucosio, in modo simile a un “antiporter”, una classe di trasportatori che scambiano una sostanza con un’altra attraverso le membrane.
Cosa succede quando SPNS2 manca
Nei topi ingegnerizzati per non esprimere SPNS2, i livelli di S1P nel sangue e nella linfa sono diminuiti, mentre l’S1P si è accumulato nei tessuti come fegato, rene, polmone e cuore — esattamente ciò che ci si aspetta se un esportatore fosse disattivato. Ma anche il loro equilibrio degli zuccheri era disturbato. La glicemia è aumentata e del glucosio in eccesso è comparso nelle urine e nelle feci, mentre diversi organi mostravano livelli interni di glucosio ridotti. Le immagini con un tracciante radioattivo simile al glucosio hanno rivelato che questi topi assorbivano normalmente lo zucchero dall’intestino, ma i loro tessuti — e in particolare i reni — erano inefficienti nel recuperare il glucosio dal circolo e dall’urina filtrata. Nel complesso, questi dati indicano un difetto nell’ingresso del glucosio nelle cellule e nel suo riutilizzo, nonostante livelli normali di insulina e segnali ormonali.
SPNS2 attrae carburante mentre espelle segnali
Per verificare se SPNS2 muove direttamente il glucosio, il gruppo ha manipolato i suoi livelli in cellule vascolari e in altri tipi cellulari. Quando hanno aumentato SPNS2, le cellule rilasciavano più S1P nel mezzo circostante e assorbivano più glucosio, producendo più energia e mostrando una respirazione e un consumo di zuccheri più intensi. Quando hanno eliminato o bloccato SPNS2, le cellule trattenevano l’S1P e assumevano meno glucosio. Questi effetti persistevano anche quando i trasportatori classici di zucchero (come GLUT1 e GLUT3) erano inibiti, e non dipendevano dai recettori per S1P sulla superficie cellulare né dall’insulina. In ‘proteoliposomi’ artificiali — piccole bolle di laboratorio con SPNS2 purificata inserita nella membrana — la proteina poteva trasferire direttamente glucosio marcato fluorescente o radioattivo verso l’interno, ma solo in modo efficiente quando l’S1P era presente sul lato interno. Ciò dimostra che SPNS2 può agire come importatore di glucosio collegato all’esportazione di S1P.
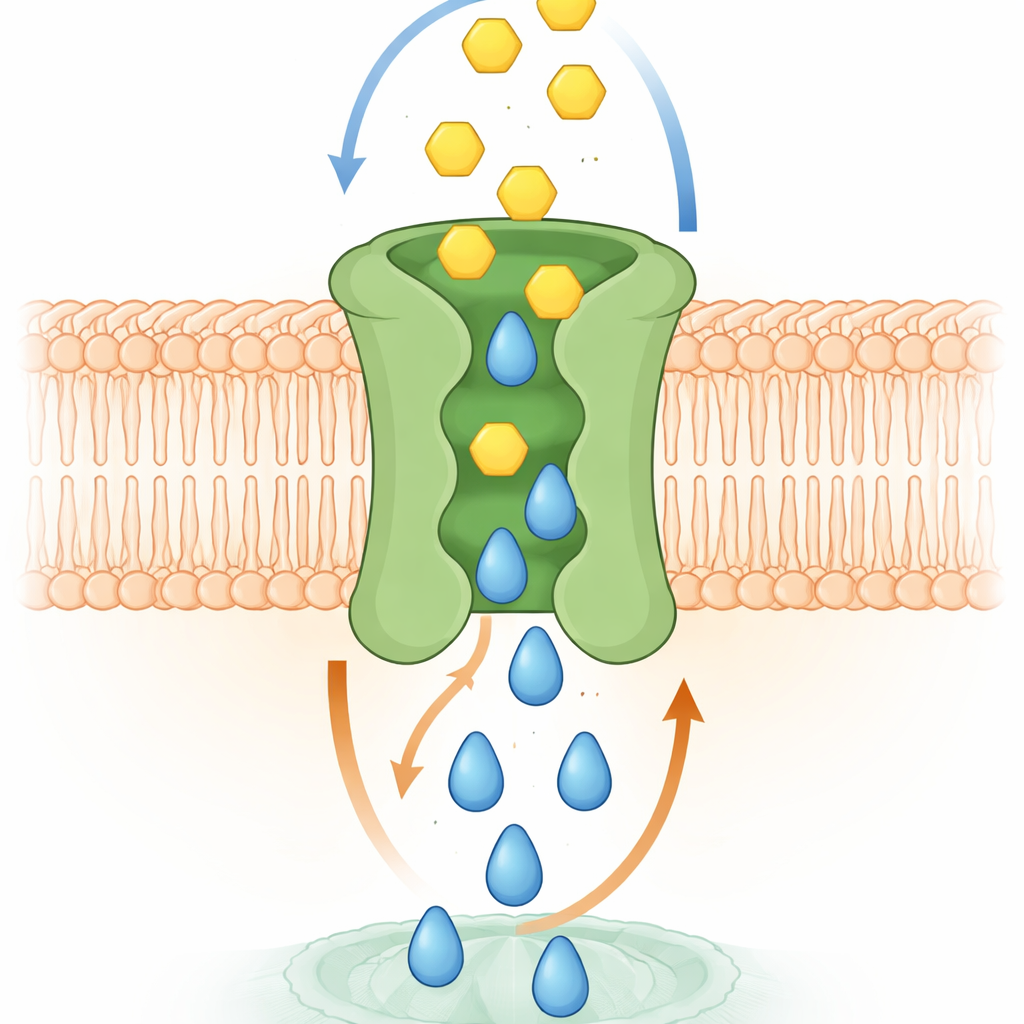
Come funziona probabilmente lo scambio molecolare
Simulazioni al computer ed esperimenti strutturali hanno aiutato a spiegare il meccanismo. Modelli ad alta risoluzione di SPNS2 in una membrana mostravano l’S1P scorrere verso l’alto attraverso una cavità centrale, provocando sottili cambiamenti di forma che aprono tasche temporanee per il glucosio sul lato esterno. Man mano che l’S1P si muove verso l’esterno, il glucosio può ancorarsi in queste tasche e poi scivolare lungo lo stesso percorso centrale verso l’interno della cellula. I ricercatori hanno identificato aminoacidi specifici che entrano in contatto con il glucosio in queste tasche. Quando questi residui sono stati mutati, il legame con il glucosio è diminuito e il trasporto è fallito, anche se le proteine modificate raggiungevano comunque la superficie cellulare. Nelle cellule vive, la perdita di questo trasporto accoppiato indeboliva processi guidati dall’S1P come la crescita cellulare, la migrazione per chiudere una lacuna simile a una ferita e la capacità degli strati di cellule endoteliali di formare una barriera ermetica — funzioni che richiedono sia segnalazione sia energia.
Perché questo è importante per salute e malattia
Rivelando che SPNS2 è una porta a doppio senso — che invia S1P mentre fa entrare il glucosio — questo lavoro collega una potente molecola segnalatrice al rifornimento energetico di base in un unico passaggio. Quando SPNS2 rilascia S1P per innescare risposte immunitarie o vascolari, contemporaneamente aiuta le cellule a importare carburante extra per alimentare quelle azioni. Le interruzioni di questo accoppiamento possono contribuire a iperglicemia, perdita renale di zucchero e forme di alterato controllo del glucosio indipendenti dall’insulina. Poiché SPNS2 e la segnalazione dell’S1P influenzano anche la diffusione del cancro, l’infiammazione e l’integrità dei vasi sanguigni, mirare a questo «guardiano del segnale e dello zucchero» potrebbe aprire nuove strade per trattare malattie metaboliche, condizioni autoimmuni e tumori che dipendono sia da una segnalazione aumentata sia da un maggiore assorbimento di glucosio.
Citazione: Weigel, C., Hossen, M.L., Brown, R.D.R. et al. SPNS2 exports sphingosine-1-phosphate and imports glucose. Nat Commun 17, 3901 (2026). https://doi.org/10.1038/s41467-026-71659-7
Parole chiave: trasporto del glucosio, sfingosina-1-fosfato, trasportatore di membrana, biologia endoteliale, segnalazione metabolica